Fehlgesteuerter Proteinabbau fördert Leukämien und Hirntumoren
Überraschende Verbindung zwischen Energiestoffwechsel und dem epigenetischen Code
Ein Enzym, das für den Abbau bestimmter Aminosäuren aus der Nahrung zuständig ist, spielt eine zentrale Rolle bei der Entstehung von Leukämien und bösartigen Hirntumoren. Dies veröffentlichten Wissenschaftler aus dem Deutschen Krebsforschungszentrum nun in der Fachzeitschrift Nature. Die Forscher entdeckten damit eine überraschende Verbindung zwischen dem Energiestoffwechsel und dem so genannten „epigenetischen Code“: Diese Markierungen am Erbgut der Krebsstammzellen entscheiden über die Aktivität der Gene und damit über viele Zellfunktionen. Die Blockade des Enzyms sehen die Autoren als vielversprechende Möglichkeit, Krebserkrankungen zu bekämpfen.
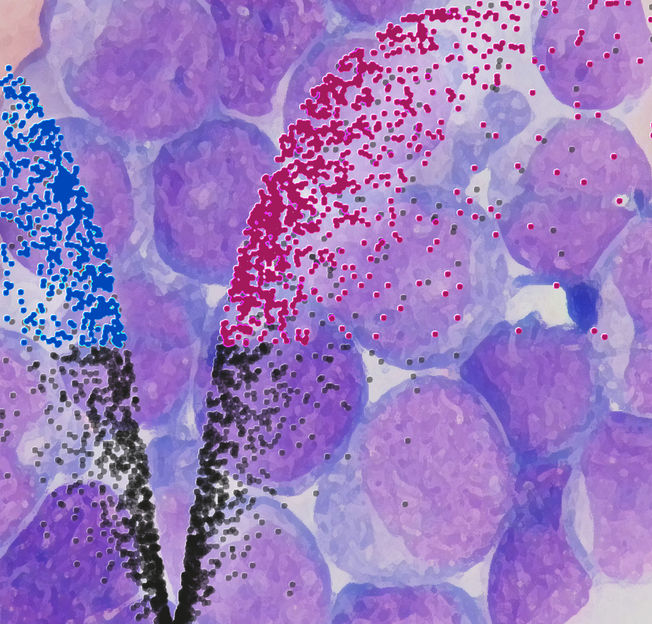
Krebsstammzellen mit einem charakteristischen Proteinexpressionsprofil lösen Blutkrebs aus.
© Simon Raffel/DKFZ
Die Akute Myeloische Leukämie, eine aggressive Form von Blutkrebs, kehrt nach zunächst erfolgreicher Therapie sehr häufig zurück. Dafür werden therapieresistente Stammzellen verantwortlich gemacht. Wissenschaftler um Andreas Trumpp, Deutsches Krebsforschungszentrum (DKFZ) und HI-STEM gGmbH, wollten den molekularen Hintergrund dieser Resistenz verstehen. Dazu verglichen sie in Patientenproben die Proteinzusammensetzung von AML-Stammzellen und Leukämiezellen ohne Stammzelleigenschaften.
Dabei fielen in den Stammzellen auffällig hohe Spiegel des Enzyms BCAT1 auf, die verdächtigerweise während eines Krebsrückfalls noch weiter anstiegen. Das sahen die Forscher als Hinweis darauf, dass BCAT1 mit der Therapieresistenz in Verbindung stehen könnte.
Krebsforscher hatten das Enzym BCAT1, das für den Abbau bestimmter Proteine aus der Nahrung zuständig ist, bereits seit längerem im Verdacht, bei der Entstehung bösartiger Tumoren eine Rolle zu spielen. So hatte das Team um Bernhard Radlwimmer vom DKFZ kürzlich erst gefunden, dass eine Überproduktion von BCAT1 die Aggressivität von bösartigen Hirntumoren und von Brustkrebs steigert.
Die beiden Forschungsgruppen schlossen sich nun zusammen, um herauszufinden, wie BCAT1 die Therapieresistenz der Leukämiestammzellen beeinflusst. Dabei kamen sie einem bislang unbekannten Prozess auf die Spur, in dem ein zentrales Molekül des Energiestoffwechsels eine entscheidende Rolle spielt. BCAT1 senkt den Spiegel dieses Schlüsselmoleküls, was dazu führt, dass das Erbgut vermehrt mit chemischen Markierungen versehen wird.
„Diese winzigen Methylgruppen, die an die DNA angeheftet werden, entscheiden darüber, welche Gene aktiv sind oder aber stumm bleiben und haben dadurch einen immensen Einfluss auf alle Zellfunktionen“, sagt Simon Raffel, einer der Erstautoren der Studie.
Dieses Ergebnis ließ die beiden DKFZ-Teams aufhorchen. Denn bei weiteren 30 Prozent der Fälle von Akuter Myeloischer Leukämie führen Defekte in anderen Enzymen zu derselben Konsequenz: Sie steigern die krebsfördernde Methylierung des Erbguts. Die AML ist für ein extrem heterogenes Muster an genetischen Veränderungen bekannt. Die fehlgesteuerte Methylierung jedoch, mit ihren drastischen Folgen für die gesamte Zelle, ist offenbar ein gemeinsames Kennzeichen dieser bösartigen Erkrankung.
Die Erkenntnis, dass BCAT1 als Treiber der krebsfördernden Methylierung in AML-Stammzellen und anderen Krebsstammzellen funktioniert, eröffnet neue therapeutische Optionen: „Eine Blockade des Enzyms mit einem zielgerichteten Wirkstoff könnte die Methylierung des Erbguts normalisieren und damit die Krebsausbreitung und die Therapieresistenz eindämmen“, sagt Andreas Trumpp.