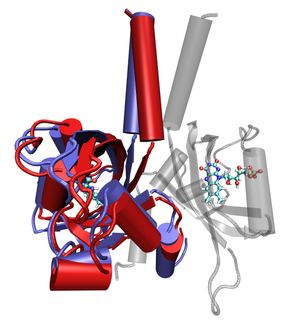
Kernspintomograf für einzelne Proteine
Dank einer verbesserten Auflösung kann ein Quantensensor einzelne Atome in Biomolekülen erkennen
Kernspintomografen, wie man sie aus dem Krankenhaus kennt, werden jetzt extrem feinfühlig. Ein Quantensensor, den ein Team um Jörg Wrachtrup, Professor an der Universität Stuttgart und Forscher des Stuttgarter Max-Planck-Instituts für Festkörperforschung, entwickelt hat, ermöglicht es, mit der Kernspintechnik sogar die Struktur einzelner Proteine Atom für Atom zu untersuchen. Das Verfahren könnte künftig helfen, Krankheiten im Frühstadium zu diagnostizieren, indem es erste defekte Proteine detektiert.
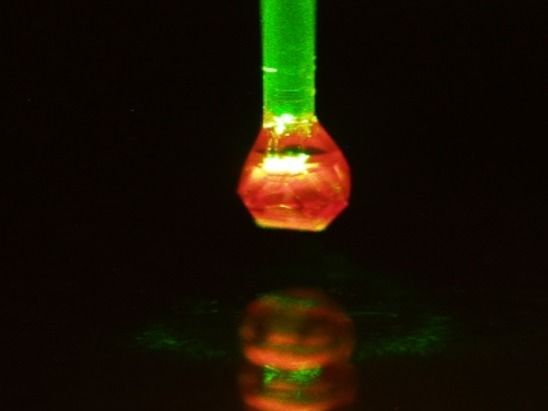
Über eine Glasfaser regt ein grüner Laser Stickstoffatome in einem Diamanten an, der daher rot fluoresziert. Wie stark ein Stickstoffatom am Rand des Diamantgitters leuchtet, erlaubt Rückschlüsse auf die magnetischen Signale aus einer Probe auf der Oberfläche des Sensors.
© Universität Stuttgart
Viele Krankheiten haben ihre Ursache in fehlerhaften Proteinen. Da Proteine wichtige biochemische Motoren sind, kann es dadurch zu Störungen im Stoffwechsel kommen. Ein Beispiel sind etwa defekte Prionen, die bei BSE oder der Creutzfeldt-Jakob-Krankheit Hirnschädigungen auslösen. Bei krankhaft veränderten Prionen weist die komplexe Molekülstruktur Fehler auf. Das Problem: Einzelne defekte Proteine können in einer Art Dominoeffekt bei benachbarten intakten Proteinen ebenfalls Fehler induzieren und dadurch eine Erkrankung auslösen. Es wäre daher für Mediziner sehr hilfreich, wenn sich bereits die ersten, noch vereinzelten Prionen mit der falschen Struktur aufspüren ließen. Die Struktur eines einzelnen Biomoleküls zu klären, war bislang aber nicht möglich.
Eine Miniaturisierung des aus der Medizin bekannten MRT
Ein Forscher-Team aus Stuttgart aber hat jetzt in der Fachzeitschrift Science ein Verfahren vorgestellt, mit dem sich künftig einzelne Biomoleküle sicher untersuchen lassen können. Das ist nicht nur für die Bekämpfung von Krankheiten, sondern auch für die chemische und biochemische Grundlagenforschung von Bedeutung.
Bei dem Verfahren handelt es sich gewissermaßen um die Miniaturisierung der aus der Medizintechnik bekannten Kernspinresonanztomografie (NMR), die in der klinischen Anwendung meist als MRT bezeichnet wird. Die NMR nutzt eine besondere Eigenschaft der Atome, den Spin. Der Spin lässt sich vereinfacht als Drehbewegung von Atomkernen und Elektronen um die eigene Achse verstehen, der die Teilchen zu winzigen, kreiselnden Stabmagneten macht. Wie sich diese Magneten verhalten, ist für jede Atomsorte beziehungsweise jedes chemische Element charakteristisch. So rotiert jedes Teilchen mit einer bestimmten Frequenz.
Mit einem kleinen NMR-Sensor lassen sich einzelne Moleküle vermessen
Bei der medizinischen Anwendung wird meist nur eine Sorte von Atomen im Körper detektiert – beispielsweise Wasserstoff. Je nach Wasserstoffgehalt in den verschiedenen Geweben, lässt sich das Körperinnere dann anhand unterschiedlicher Kontraste unterscheiden.
Bei der Strukturaufklärung von Biomolekülen hingegen kommt es darauf an, jedes einzelne Atom zu bestimmen und so Stück für Stück den Aufbau des Biomoleküls zu enträtseln. Entscheidend dafür ist, dass die NMR-Detektoren so klein sind, dass sie eine Auflösung im Nanometer-Maßstab zu erreichen und so empfindlich sind, dass sie einzelne Moleküle exakt vermessen können. Einen so kleinen NMR-Sensor haben die Forscher um Jörg Wrachtrup bereits vor gut vier Jahren konstruiert. Zwischen einzelnen Atomen konnten sie damit aber noch nicht unterscheiden.
Einzelne Atomsorten dank höherer Frequenzauflösung
Um eine atomgenaue Auflösung zu erreichen, müssen die Forscher nämlich die Frequenzsignale, die sie von den einzelnen Atomen eines Moleküls empfangen, unterscheiden können – etwa so wie ein Radio einen Rundfunksender ebenfalls anhand seiner charakteristischen Frequenz erkennt. Bei den Signalen der Atome eines Proteins handelt es sich um die Frequenzen, mit denen die atomaren Stabmagneten in dem Protein kreiseln. Diese Frequenzen liegen sehr dicht beieinander, so als würden sich die Sendefrequenzen von Radiostationen alle in einem sehr schmalen Bereich drängen. Erst jetzt haben die Stuttgarter Forscher eine Frequenzauflösung erreicht, mit der sie einzelne Atomsorten unterscheiden können.
„Wir haben einen Quantensensor entwickelt, der erstmals die Frequenzen verschiedener Atome ausreichend präzise wahrnehmen und ein Molekül damit quasi atomgenau auflösen kann“, sagt Jörg Wrachtrup. Damit lässt sich ein großes Biomolekül jetzt gewissermaßen abtasten. Bei dem Sensor, der als winzige NMR-Antenne dient, handelt es sich um einen Diamanten, in dessen Kohlenstoff-Gerüst dicht unter der Kristalloberfläche ein Stickstoffatom eingebaut ist. Die Stelle, an der das Stickstoffatom sitzt, nennen die Physiker NV-Zentrum: N für Stickstoff, und V für das englische vacancy, das auf ein fehlendes Elektron im Diamantgitter direkt neben dem Stickstoffatom hinweist. Ein solches NV-Zentrum nimmt die Kernspins von Atomen wahr, die sich dicht am NV-Zentrum befinden.
Die Frequenz, mit der das magnetische Moment eines gerade gemessenen Atoms kreiselt, überträgt sich auf das magnetische Moment im NV-Zentrum, was sich durch eine Farbänderung mit einem speziellen Lichtmikroskop wahrnehmen lässt.
Der Quantensensor speichert Frequenzsignale
Die hohe Empfindlichkeit erreicht der Quantensensor, weil er Frequenzsignale eines Atoms speichern kann. Eine einzige Messung der Frequenz eines Atoms wäre für den Quantensensor zu schwach und möglicherweise zu verrauscht. Dank des Speichers aber kann der Sensor über längere Zeit viele Frequenzsignale aufnehmen und sich so auf die Schwingungsfrequenz eines Atoms sehr scharf einstellen – so wie man mit einem hochwertigen Weltempfänger eng nebeneinander liegende Rundfunkkanäle sauber voneinander trennen kann.
Neben der hohen Auflösung, bringt diese Technik noch andere Vorteile mit sich: Sie arbeitet bei Raumtemperatur und benötigt kein Vakuum wie andere hochempfindliche NMR-Verfahren, die in der biochemischen Forschung eingesetzt werden. Diese werden zudem in der Regel nahe am absoluten Nullpunkt der Temperatur von minus 273,16 Grad Celsius betrieben, wozu eine aufwendige Kühlung mit Helium nötig ist.
Ein künftiges Anwendungsgebiet: die Hirnforschung
Jörg Wrachtrup sieht für seinen fein auflösenden Quantensensor gleich mehrere mögliche zukünftige Anwendungsgebiete. „Es ist denkbar, dass man künftig schon im Frühstadium von Erkrankungen einzelne auffällig veränderte Proteine detektiert, die bislang übersehen wurden.“ Darüber hinaus arbeitet Wrachtrup zusammen mit einem Industrieunternehmen an einem etwas größeren Quantensensor, mit dem künftig die schwachen Magnetfelder des Gehirns wahrgenommen werden könnten. „Wir nennen diesen Sensor Brain-Reader. Er soll dazu beitragen, die Arbeitsweise des Gehirns zu entschlüsseln – und wäre eine sehr gute Ergänzung zu den herkömmlichen elektrischen Ableitungen der EEGs“ – der Elektroenzephalogramme. Für den Brain-Reader arbeitet Wrachtrup zusammen mit dem Industriepartner bereits an einer Halterung und einem Gehäuse, damit sich das Gerät im Alltag einfach tragen und bedienen lässt. Bis es soweit ist, braucht es aber noch mindestens zehn Jahre Forschungsarbeit.
Originalveröffentlichung
Nabeel Aslam, Matthias Pfender, Philipp Neumann, Rolf Reuter, Andrea Zappe, Felipe Fávaro de Oliveira, Andrej Denisenko, Hitoshi Sumiya, Shinobu Onoda, Junichi Isoya und Jörg Wrachtrup; "Nanoscale nuclear magnetic resonance with chemical resolution"; Science; 1. Juni 2017