Mit voller Kraft auf Erregerjagd
Mechanismus aufgeklärt, wie Zellen mithilfe von Proteinfilamenten Kraft erzeugen und sich effektiv bewegen
Anzeigen
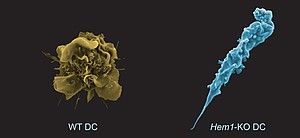
Die Zellen des menschlichen Körpers besitzen in ihrem Inneren ein flexibles Gerüst, das Zytoskelett, welches unter anderem aus Aktinfilamenten besteht und sich in stetigem Auf- und Abbau befindet. So können sich Zellen verformen oder bewegen. Diese Fähigkeit ist zum Beispiel für die Embryonalentwicklung, die Wundheilung und ein funktionierendes Immunsystem wichtig. Dabei müssen Zellen Energie und Kraft aufwenden, um sich durch Gewebe zu bewegen. Beispielsweise dringen Immunzellen in alle Bereiche unseres Körpers vor, um Krankheitserreger zu finden und zu bekämpfen. Umgekehrt können auch manche Erreger das Zytoskelett missbrauchen, um in Zellen einzudringen. Forscher des Helmholtz-Zentrums für Infektionsforschung (HZI) und der Technischen Universität Braunschweig haben nun die molekularen Grundlagen dafür aufgeklärt, wie Zellen sich effektiv vorwärtsbewegen können durch die Ausbildung von schubkräftigen Ausstülpungen der Zellmembran. Die Forscher konnten mit der CRISPR/Cas-Technologie erstmals die genaue Funktion einer speziellen Proteinfamilie, der Formine, bei der Ausbildung dicht verzweigter Aktinnetzwerke bestimmen. Die Braunschweiger Wissenschaftler kooperierten dabei eng mit der Medizinischen Hochschule Hannover (MHH) und der Universität Leipzig.
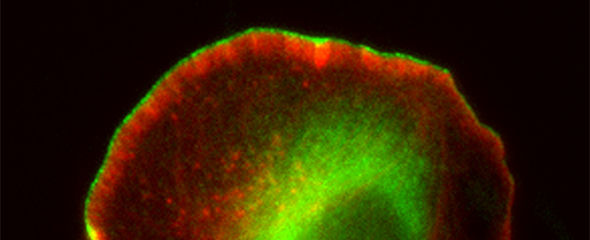
Melanomzelle bei der Wanderung, deren Bewegung nach oben links durch Formin-Proteine (grün) unterstützt wird.
©HZI /Frieda Kage
„Wenn sich Zellen durch Gewebe des Körpers bewegen, bilden sie dazu verschiedene Ausstülpungen an ihrer Vorderseite aus: segelartige Lamellipodien, fingerförmige Filopodien, aber auch bläschenartige Ausstülpungen“, sagt Klemens Rottner, Leiter der HZI-Arbeitsgruppe „Molekulare Zellbiologie“ und Professor am Institut für Zoologie der Technischen Universität Braunschweig. Das Zytoskelett der Zellen spielt dabei eine entscheidende Rolle. Es ist allerdings im Gegensatz zum Knochenskelett kein starres Stützsystem, sondern ein dynamisches Geflecht. Um ihre Form zu verändern oder sich auszubreiten, brauchen Zellen spezielle Mikrofilamente ‑ winzige, nur nanometerdicke Fasern aus dem Strukturprotein Aktin. Durch das Zusammenspiel der Aktinfilamente mit speziellen Myosin-Proteinen wird Zellbewegung möglich. „Die Aktin-Myosin-Filamente sind gewissermaßen die Muskeln der Zelle“, sagt Rottner.
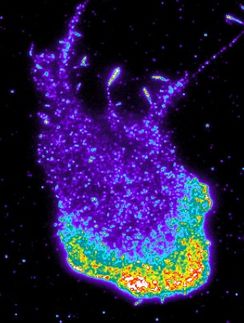
Im Detail betrachtet besteht ein Lamellipodium aus quervernetzten und parallel ausgerichteten Bündeln von Aktinfilamenten, die von einer dünnen Zellmembran umschlossen sind. Diese Aktinfilamente sind am Vordersaum der Ausstülpung in der Zellmembran verankert und schieben sie durch den stetigen Anbau von Aktinbausteinen vorwärts, während sie an ihrer Rückseite fortwährend abgebaut werden. Durch diesen kontinuierlichen Umbau von Aktinfilamenten bewegt sich die Zelle vorwärts.
Bisher war bekannt, dass ein bestimmter Proteinkomplex für den Aufbau des Aktinnetzwerks in den Lamellipodien verantwortlich ist – der sogenannte Arp2/3-Komplex. Die Forscher konnten nun eine weitere wichtige Komponente nachweisen: An den schnell wachsenden Enden der Aktinfilamente binden Proteine aus der Familie der Formine. „Die Rolle dieser Proteine in Lamellipodien war bislang nicht klar. Man dachte, sie würden lediglich die Geschwindigkeit steuern, mit der Bausteine an die Filamente des Netzwerks angebaut werden“, sagt Rottner. Jedoch fanden die Autoren der Studie heraus, dass diese Proteine vor allem die Filamentdichte und die Stabilität des Aktinnetzwerks regulieren. Anders als der Arp2/3-Komplex scheinen diese Formine zudem das wachsende Aktinfilament mit der Zellmembran zu verbinden, wodurch die entstehende Kraft direkt auf die Membran übertragen werden kann und somit eine effiziente Vorwärtsbewegung der Zelle gewährleistet wird.
Für seine Untersuchungen hat das Forscherteam mittels CRISPR/Cas-Technologie Formine sowohl in Tumor- als auch in Bindegewebszellen von Mäusen ausgeschaltet. „Diese moderne molekularbiologische Methode erlaubte uns, effizient und kostengünstig die Bildung zweier funktionsverwandter Formine gleichzeitig und vollständig auszuschalten“, sagt Frieda Kage, Erstautorin der Studie und Wissenschaftlerin im Team von Rottner. „So konnten wir beweisen, dass diese Formine nicht essenziell für die Ausbildung der Lamellipodien selbst sind, denn durch den Arp2/3-Komplex wird das Aktinnetzwerk trotzdem gebildet“, ergänzt die Nachwuchswissenschaftlerin. „Allerdings war das Netzwerk viel weicher, weil sowohl die Dichte als auch die räumliche Anordnung der Filamente verändert waren.“
Klemens Rottner fasst zusammen: „Nur in der Kombination des Arp2/3-Proteinkomplexes mit Forminen können die Zellen stabile, dicht verzweigte Aktinnetzwerke ausbilden. Wenn die Formine fehlen, werden die Zellen in ihrer Beweglichkeit sehr geschwächt, weil sie sich durch das zu weiche Aktinnetzwerk nicht effizient vorwärtsschieben können.“ Die im Bereich von Nano-Newtonliegenden Vorschubkräfte der Zellen mit und ohne Formine konnten von den Forschern direkt gemessen werden. Dazu nutzten sie ein AFM-Rasterkraftmikroskop in Kooperation mit Prof. Josef Käs vom Institut für Experimentelle Physik I der Universität Leipzig. „In den Zellen, denen Formine fehlten, konnten wir eine Reduktion der Vorschubkräfte um 75 Prozent messen“, sagt Rottner. „Diese drastisch reduzierte Kraftentwicklung erklärt, warum Zellen ohne diese Formine nur sehr langsam migrieren“, ergänzt Kage.
Interessanterweise sind diese Formine mit bestimmten Krebsarten wie Karzinomen und Melanomen eng assoziiert: Große Forminmengen gehen bei Patienten häufig mit aggressiver Metastasenbildung und der Invasion der Krebszellen in andere Gewebe einher. Die Daten der neuen Studie erklären mechanistisch, warum sich diese Zellen besser bewegen. „Da vor allem auch Immunzellen Kräfte aufwenden müssen, um zu Krankheitserregern zu gelangen, spielt für uns die Erforschung solcher Bewegungsprozesse eine entscheidende Rolle bei der Abwehr von Infektionskrankheiten. Wir müssen diese Prozesse genau verstehen, um mögliche neue Ansatzpunkte für Therapien zu finden“, sagt Klemens Rottner. „Zudem nutzen viele Bakterien und Viren die Polymerisationskräfte von Aktinfilamenten, entweder um in Zellen einzudringen, sich in diesen zu bewegen, oder auch, um noch nicht betroffene Nachbarzellen zu infizieren.“
Die Ergebnisse der aktuellen Studie dienen als Ausgangsbasis für Versuche mit verschiedensten Krankheitserregern wie Salmonellen, Shigellen und Listerien, da diese Erreger dafür bekannt sind, sich der durch das Aktinzytoskelett erzeugten Kräfte der Wirtszelle zu bedienen. Die hier untersuchten Formine gezielt in einer frühen Phase des Kontakts von Erreger und Wirtszelle zu beeinflussen, könnte einen aussichtsreichen Ansatz darstellen, um Infektionsprozesse zu unterbinden, hoffen die Wissenschaftler.