Flimmerhärchen-Defekt auf der Spur
Mögliches Schlüssel-Gen für die Behandlung von COPD und anderen chronischen Lungenerkrankungen entdeckt
Anzeigen
Die Atemluft wird knapp, wenn Flimmerhärchen ihre Aufgabe nicht mehr erfüllen. Krankheiten, wie chronische Atemwegsinfektionen und schwere Atembeschwerden, wie die chronisch obstruktive Lungenerkrankung (COPD), geben Forschern noch immer Rätsel auf. Wie genau es auf Ebene der Gene zu einem Defekt der Flimmerhärchen kommt, war bisher weitgehend unklar.
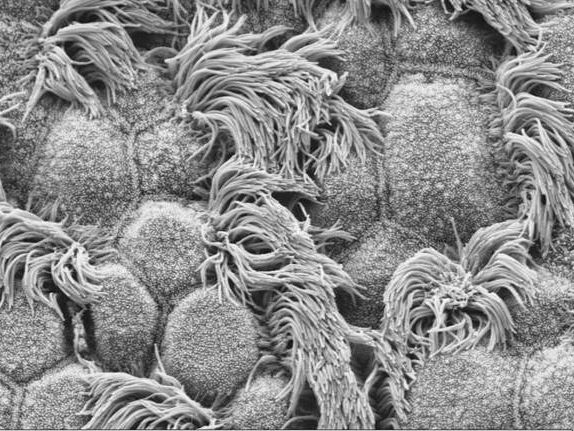
Flimmerhärchen bei gesunder Maus.
Nemajerova / Central Microscopy Imaging Center, Stony Brook University
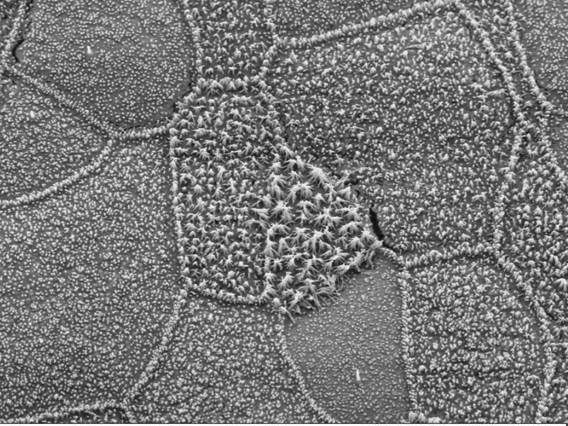
Unter dem Elektronenmikroskop wird sichtbar, dass Mäuse ohne das Protein p73 weniger und kürzere Flimmerhärchen in ihren Atemwegen haben als gesunde Mäuse.
Nemajerova / Central Microscopy Imaging Center, Stony Brook University
Ein internationales Forscherteam unter Leitung der Göttinger Wissenschaftlerin Dr. Muriel Lizé, Leiterin der Arbeitsgruppe Molekulare und Experimentelle Pneumologie am Institut für Molekulare Onkologie und an der Klinik für Kardiologie und Pneumologie der Universitätsmedizin Göttingen (UMG) und Mitglied des Göttinger Zentrums für molekulare Biowissenschaften (GZMB), hat jetzt einen zentralen molekularen Faktor gefunden, der die Bildung der Flimmerhärchen in den Atemwegen kontrolliert. Die Ergebnisse der Forscher zeigen, dass das Protein p73 in Zellen ein Netzwerk von Genen reguliert, das für die Bildung der Flimmerhärchen verantwortlich ist. Die neuen Erkenntnisse können dazu beitragen, die Ursachen für chronische Lungenerkrankungen beim Menschen besser zu verstehen.
Flimmerhärchen, auch Zilien genannt, sind mikroskopisch kleine Fortsätze von Körperzellen. In unserem Körper bedecken sie in großer Zahl bestimmte Oberflächen, die man als „Flimmerepithel“ bezeichnet. Solche Flimmerepithele gibt es in den Atemwegen, bei Frauen in den Eileitern und bei Männern im Hoden. Eine einzelne Zelle kann Hunderte Zilien ausbilden. Wie Tausende winzige Ruder führen die Zilien rhythmische Schläge aus und bewegen damit Flüssigkeit. Bei den so genannten Ciliopathie-assoziierten Krankheiten wie der primären ciliären Dyskinesie (PCD) sind die Flimmerhärchen nicht voll funktionsfähig. In den Atemwegen etwa führt dies dazu, dass sich Flüssigkeit ansammelt und Fremdkörper oder Krankheitserreger nicht mehr abtransportiert werden können. Chronische Atemwegsinfektionen und schwere Atembeschwerden, wie die chronisch obstruktive Lungenerkrankung (COPD), sind die Folge.
Verschnupfte Mäuse
Auf die Spur für die Ursache eines möglichen Flimmerhärchen-Defekts brachte das Göttinger Forscherteam eine Beobachtung. Dr. Muriel Lizé und ihren Kollegen fiel auf, dass auch Mäuse mit einem Gendefekt, der bisher noch nie mit einer primären ciliären Dyskinesie (PCD) in Verbindung gebracht worden war, typische Symptome für eine PCD zeigten: Bei diesen Tieren war jenes Gen mutiert, das den Bauplan für das Protein p73 liefert. Das Protein p73 ist vor allem dafür bekannt, dass es Krebs unterdrückt und Prozesse in der Entwicklung steuert.
„Mäuse ohne funktionsfähiges p73 zeigen vielfältige Symptome, die sich nicht mit den bisher bekannten Funktionen von p73 erklären ließen“, sagt Dr. Lizé, Senior-Autorin der Publikation. Genauere Untersuchungen zeigten, dass Tiere ohne das p73-Protein an Schnupfen, Entzündungen der Nasennebenhöhlen und an Lungenemphysemen litten. „Das alles sind Symptome, die wir von Mäusen kennen, bei denen die Flimmerhärchen nicht voll funktionsfähig sind“, so die Molekularbiologin. Unter dem Elektronenmikroskop stießen die Forscher auf bemerkenswerte Veränderungen. „Das Flimmerepithel war vollkommen verkümmert, wir fanden fast keine Flimmerhärchen. Und die wenigen vorhandenen waren deutlich verkürzt“, sagt Dr. Dietmar Riedel vom Max-Planck-Institut für biophysikalische Chemie in Göttingen.
Forschungsergebnisse im Detail
Ist tatsächlich das Protein p73 für die defekten Flimmerhärchen verantwortlich? Um diese Frage zu klären, führten die Forscher ein ausgeklügeltes Experiment durch. Sie züchteten Epithelzellen aus den Atemwegen von Mäusen im Reagenzglas an einer Grenzfläche von Flüssigkeit und Luft. Dieser Reiz führt dazu, dass die Zellen auch im Reagenzglas Flimmerhärchen bilden. Und tatsächlich zeigte sich das gleiche Muster wie in den Atemwegen der Mäuse: Zellen ohne p73 brachten deutlich weniger und kürzere Flimmerhärchen hervor als Zellen mit dem Protein.
Offenbar wirkte sich das Fehlen von p73 direkt auf die Ausbildung der Flimmerhärchen aus und verursachte so die schweren Atemwegserkrankungen. „Das war wirklich überraschend, denn bisher hatte man das Protein p73 noch nie mit einer Funktion in den Atemwegen in Verbindung gebracht“, sagt Dr. Lizé.
In weiteren Untersuchungen gingen die Göttinger Forscher der Frage nach, welche Rolle das Protein p73 bei der Entwicklung von Flimmerhärchen spielt. Bekannt war bisher: Das Protein p73 wirkt in der Zelle als sogenannter Transkriptionsfaktor: Es steuert, welche Gene aktiv sind, indem es an bestimmte DNA-Sequenzen in diesen Genen bindet. Die Forscher vermuteten daher, dass das Protein p73 die Flimmer-härchen-Bildung kontrolliert, indem es bestimmte Gene beeinflusst.
Weit über 50 Gene, die unter der Kontrolle von p73 stehen und für das Wachstum von Flimmerhärchen unmittelbar wichtig sind, konnten die Göttinger Wissenschaftler zusammen mit der Forschergruppe von Dr. Stefan Bonn vom Deutschen Zen-trum für neurodegenerative Erkrankungen (DZNE) ermitteln. Unter diesen Genen findet sich auch der Faktor FoxJ1, der zentrale Regulator der Flimmerhärchen-Bildung. Außerdem ist von acht der Gene bekannt, dass sie bei Ciliopathie-assoziierten Erkrankungen beim Menschen eine Rolle spielen. „Mit p73 haben wir einen Faktor identifiziert, der ein ganzes Netz von Genen kontrolliert, die für ein funktionsfähiges Flimmerepithel wichtig sind. Dies bietet einen neuen Ansatzpunkt, um Therapien für Krankheiten wie PCD und COPD zu entwickeln und zu verbessern“, sagt Dr. Lizé.
Originalveröffentlichung
Nemajerova A, Kramer D, Siller SS, Herr C, Shomroni O, Pena T, Gallinas Suazo C, Glaser K, Wildung M, Steffen H, Sriraman A, Oberle F, Wienken M, Hennion M, Vidal R, Royen B, Alevra M, Schild D, Bals R, Dönitz J, Riedel D, Bonn S, Take-maru KI, Moll UM, Lizé M.; "TAp73 is a central transcriptional regulator of airway multiciliogenesis"; Genes Dev.; 2016 Jun 2. [Epub ahead of print]
























































