Strahlenschäden: Die gefährliche Spur langsamer Elektronen
Wie Radioaktivität biologischen Zellen zusetzt
Wie Radioaktivität biologische Zellen schädigt, wissen Forscher nur zum Teil. Im Fokus aktueller Untersuchungen steht die Wirkung so genannter Sekundärteilchen. Dringt Strahlung in den Körper ein, schlägt sie Elektronen aus biologischen Molekülen heraus. Diese stoßen auf weitere Biomoleküle und schädigen diese. Auch das Erbgutmolekül DNA ist davon betroffen, was im Extremfall zu Krebs führen kann. Aber auch für die gezielte Zerstörung von Krebszellen werden Strahlung und die mit ihr verbundenen Sekundärteilchen genutzt. Unter diesen Sekundärteilchen ließen Forscher langsame Elektronen lange Zeit unberücksichtigt, weil deren Energie nicht ausreicht, um ein Molekül zu ionisieren. Seit aber bekannt ist, dass die langsamen Elektronen DNA-Moleküle trotzdem effektiv schädigen können, erforschen Physiker die Entstehung solcher Sekundärelektronen intensiver. Nun haben Forscher des Max-Planck-Instituts für Kernphysik in Heidelberg in Zusammenarbeit mit Kollegen von der Universität Innsbruck erstmals einen Prozess untersucht, bei dem ein zunächst schnelles Elektron ein Molekül trifft und drei Sekundärelektronen auftreten. Dadurch vervielfacht sich die Menge der freien Elektronen. Weil sich viele davon langsam bewegen, könnten die nun beobachteten Teilchenreaktionen eine wichtige Rolle bei der Entstehung von Strahlenschäden spielen.

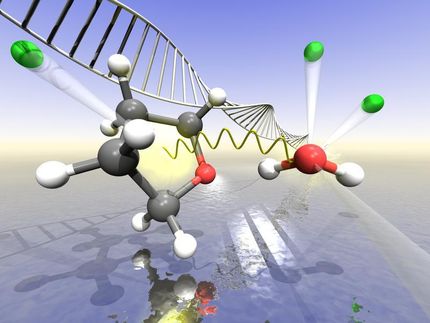
Protokoll eines Zerfalls: Wenn ein Elektron ein Argonatom in einem zweiatomigen Molekül trifft (links), schlägt es aus diesem ein Sekundärelektron heraus und wird dabei von seiner Bahn abgelenkt. Das Argonatom nimmt dabei Energie auf und gibt diese an das andere Atom weiter (rote Zickzack-Linie). Daraufhin wird auch dieses Atom ionisiert, sodass sich die beiden Argonionen gegenseitig abstoßen. Bei dem Prozess entstehen zwei zusätzliche langsame Elektronen. Die schädliche Wirkung von Elektronenstrahlen, wie sie beim radioaktiven Beta-Zerfall entstehen, wird so vervielfacht.
© Alexander Dorn / MPI für Kernphysik
Die Heidelberger und Innsbrucker Physiker um Xueguang Ren untersuchten anhand eines einfachen Modellsystems aus zwei schwach aneinander gebundenen Argonatomen, wie Sekundärelektronen entstehen. Auf diese sogenannten Argondimere schossen sie Elektronen.
Vom Stoß mit einem Elektron wird das Argondimer regelrecht zerfetzt. Die elektrisch geladenen Bruchstücke – negative Elektronen und positive Atomrümpfe – fliegen explosionsartig auseinander. Mit einem eigens konstruierten Reaktionsmikroskop gelang es den Heidelberger Forschern nun erstmals, nicht nur die Energie von davonfliegenden Ionen zu messen, was dem bisherigen Stand der Technik entspricht, sondern auch die der Elektronen, die wegen ihrer höheren Energie wesentlich schwerer auf den Detektor zu lenken sind. Mit den gemessenen Energien aller beteiligten Teilchen waren die Physiker erstmals in der Lage, die Reaktionsmechanismen in ihrem Modellsystem zu identifizieren und Details der Reaktionsabläufe zu studieren.
Zwei Zerfallsprozesse lassen sich voneinander unterscheiden
Ähnlich einer Billardkugel gibt das Elektron einen Teil seiner Energie an seinen direkten Stoßpartner – eines der beiden Argonatome – ab und wird dabei von seiner ursprünglichen Bahn abgelenkt. Der Reaktionspartner verliert dadurch ein Elektron, er wird also ionisiert. Gleichzeitig wird er energetisch angeregt, das heißt er speichert einen Teil der Energie. Diese überträgt er dann an das zweite Argonatom, das dadurch ebenfalls ionisiert wird. Die beiden Argonionen stoßen sich nun wegen ihrer positiven Ladung gegenseitig ab und entfernen sich voneinander. Insgesamt fliegen also fünf Teilchen wie in einer Explosion auseinander: das eingestrahlte Elektron, zwei Argonionen sowie die zwei vom Argondimer freigesetzten Elektronen. Das Ganze wird als Interatomarer Coulomb-Zerfall (engl. Interatomic Coulomb Decay, abgekürzt: ICD) bezeichnet.
Den ICD konnten das Heidelberger Team von einem zweiten Prozess, dem sogenannten Strahlenden Ladungstransfer (engl. radiative charge transfer, abgekürzt: RCT) unterscheiden. Beim RCT wird das erste Argonatom doppelt ionisiert, verliert also zwei Elektronen. Es nimmt dann ein Elektron vom zweiten Argonatom auf, das so ebenfalls ionisiert wird. Das Ergebnis ist das gleiche: die beiden Ionen und drei Elektronen streben auseinander. Allerdings wird die Energie bei den beiden Reaktionsvarianten unterschiedlich auf die fünf Teilchen verteilt.
Für den ICD machten die Heidelberger Forscher eine interessante Entdeckung: Je mehr Energie das eingestrahlte Elektron an das Argonatom abgibt, desto langsamer wird die Energie auf das Nachbaratom übertragen.
Die Anzahl schädlicher Elektronen wird vervielfacht
Dies stellten die Forscher anhand auf folgende Weise fest: Das Argondimer vibriert, sodass sich die Atome periodisch voneinander entfernen und wieder annähern. Bei langsamer Energieübertragung kann sich aufgrund der Vibration der Abstand zwischen den Atomen ändern, während die Energie fließt. Bei schnellem Transfer hingegen bleibt der Abstand während des Energietransfers gleich, weil in der kurzen Zeit keine Vibration stattfindet.
Der Abstand der beiden Argonatome zum Zeitpunkt der Reaktion lässt sich aus der Energie der davonfliegenden Argonionen rekonstruieren. Weicht dieser vom Gleichgewichtsabstand des neutralen Argondimers ab, dann hat ein langsamer ICD stattgefunden, ansonsten ein schneller.
Die Heidelberger und Innsbrucker Physiker betreiben Grundlagenforschung, bei der es um das Studium der Reaktionsmechanismen geht. Dennoch misst das Teammitglied Alexander Dorn der neuen Methodik auch eine Bedeutung für die Strahlenbiologie zu. „Solche Prozesse, wie wir sie jetzt untersucht haben, vervielfachen die Anzahl von relativ langsamen Elektronen, die biologische Schäden hervorrufen können“, erklärt der Physiker. Und mehr noch: „Bei bisherigen Untersuchungen ähnlicher Art wurde Röntgenstrahlung auf Modellsysteme gelenkt“, erklärt er. „Wir haben nun die Bestrahlung mit Elektronen untersucht.“ Dies sei nah an der Realität, da radioaktive Strahlung auf ihrem Weg durch den Körper eben solche Elektronen freisetze, die dann auf biologisch aktive Moleküle träfen.