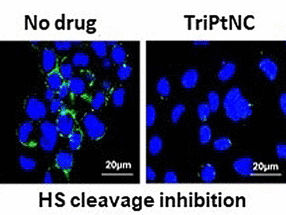
Aufnahmemechanismus für Zytostatika entdeckt
Vor gut anderthalb Jahren haben Forscher am Max-Delbrück-Centrum für Molekulare Medizin (MDC) und Leibniz-Institut für Molekulare Pharmakologie (FMP) die molekulare Identität von VRAC entdeckt. Bei VRAC handelt es sich um einen Volumen-regulierten Anionen-Kanal, der negativ geladene Ionen (Anionen) und Aminosäuren in die Zelle hinein- und wieder herauslässt. VRAC, der von dem Protein LRRC8A und mindestens einem Verwandten gebildet wird, soll auch bei der Zellteilung und bei Krebs eine Rolle spielen.
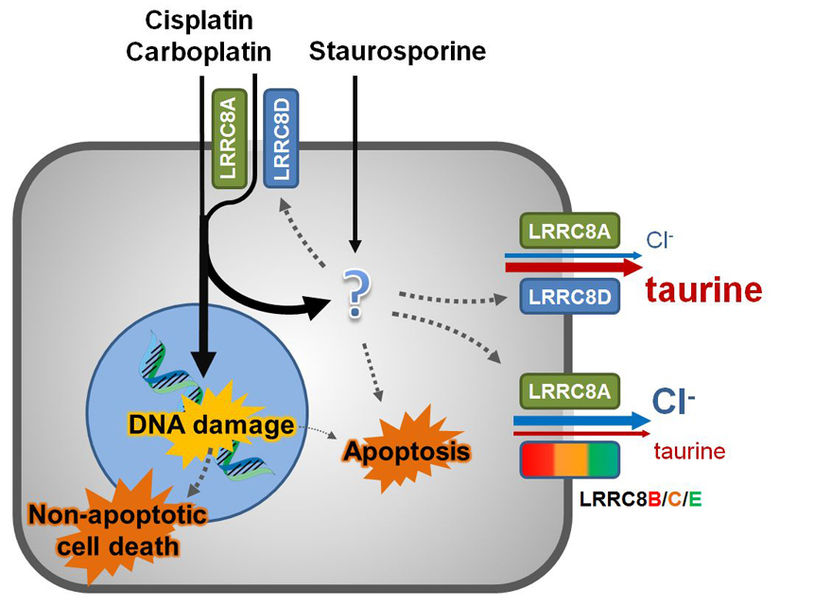
Die Chemotherapeutika Cisplatin und Carboplatin sowie der proapoptotische Naturstoff Staurosporin gelangen in kleinen Mengen durch passive Diffusion über die Plasmamembran in die Zelle. Die Platin-basierten Wirkstoffe induzieren DNA-Schäden, die zu nicht-apoptotischem Zelltod und – in geringerem Umfang – zu Apoptose führen; haben aber auch eine mechanistisch bisher schlecht verstandene direkte proapoptotische Wirkung. VRACs werden wiederum durch proapoptitische Stimuli geöffnet. Durch LRRC8A und LRRC8D gebildete Kanäle transportieren hauptsächlich zelleigene Osmolyte wie Taurin, dienen aber auch als zusätzlicher Weg für die Aufnahme der Platin-basierten Wirkstoffe, aber nicht für das größere Staurosporin. Cis- und Carboplatin befördern somit ihre eigene Aufnahme in die Zelle über die Aktivierung von VRACs.
Thomas Jentsch, FMP/MDC
VRAC entscheidend für die Wirkstoffaufnahme
Wie bedeutsam VRAC gerade für Krebserkrankungen ist, konnten die Forscher in einer anschließenden Studie gemeinsam mit niederländischen Kollegen zeigen. An Zelllinien wurde untersucht, welche Rolle VRAC und seine Untereinheiten beim Transport von Cisplatin und Carboplatin in die Zelle spielen. Das Ergebnis hat die Forscher selbst überrascht: VRAC oder vielmehr seine Bausteinproteine LRRC8A und LRRC8D sind zu 50 Prozent für den Aufnahmemechanismus der beiden weit verbreiteten Zytostatika verantwortlich. Anders ausgedrückt: Ohne diese beiden Untereinheiten kommt nur noch wenig Wirkstoff in die Zelle hinein. Aus Sicht der Forscher lassen sich damit Therapieresistenzen ein Stück weit erklären.
In ihren Experimenten hatte die Arbeitsgruppe von Thomas Jentsch die Anionen-Kanal bildenden Proteine nacheinander ausgeschaltet. Waren LRRC8A und LRRC8D an der Reihe, konnten die Zellen kaum noch Krebsmittel aufnehmen. „Es gibt zwar schon seit Langem eine Hypothese, dass VRAC bei der Apoptose eine wesentliche Rolle spielt. Aber dass das Druckventil auch als Aufnahmemechanismus für Zytostatika dient, war eine echte Überraschung“, sagt Thomas Jentsch.
Gestörte Apoptose verstärkt Therapieresistenz
Die Hypothese zur Apoptose konnte in der Studie ebenfalls bestätigt werden. War das für VRAC lebenswichtige Protein LRRC8A außer Gefecht gesetzt, funktionierte der natürliche Zelltod nicht mehr richtig.
Den Forschern zufolge ist das apoptotische Geschehen völlig unabhängig von dem Aufnahmemechanismus zu sehen. Jentsch spricht von einem doppelten Mechanismus. „Die Unterdrückung der Apoptose liegt vermutlich daran, dass bei Fehlen des volumen-regulierenden VRAC die beim programmierten Zelltod beobachtete Zellschrumpfung nicht mehr funktioniert. Dies hat mit dem Mechanismus der Medikamentenaufnahme nichts zu tun“, betont der Berliner Ionenkanalforscher.
Der nun neu entdeckte Aufnahmemechanismus konnte in der Studie sogar klinisch untermauert werden. Forscher um Sven Rottenberg vom Krebsforschungszentrum Amsterdam hatten in einem Genom-weiten Screen auf zelluläre Zytostatikaresistenz ebenfalls LRRC8D als relevantes Gen identifiziert und die genetischen Daten von Eierstockkrebspatientinnen, die mit Cisplatin oder Carboplatin behandelt worden waren, mit der Überlebenszeit verglichen. Die Tumordatenbankanalyse zeigte: Je weniger LRRC8D im Tumor exprimiert war, desto kürzer überlebten die Frauen.
Ergebnisse mit klinischer Relevanz
Begünstigt das Fehlen des VRAC-Proteins also Therapieresistenzen? „Die Daten sprechen dafür, dass LRRC8A und LRRC8D auch klinisch relevante Resistenzgene sind, wobei der Befund aber noch durch prospektive Studien erhärtet werden muss“, sagt Grundlagenforscher Jentsch. Und was dann? Rein theoretisch könne man vielleicht Aktivatoren finden, um das angeschlagene Druckventil wieder zu mobilisieren, meint Jentsch. In der Screening-Unit am FMP werde bereits danach gefahndet.
Neben den beiden klinisch relevanten Mechanismen förderte die Studie auch noch einen bislang unbekannten physiologischen Mechanismus zu Tage. Demnach ist die VRAC-Untereinheit LRRC8D immens wichtig für den Transport der Aminosäure Taurin, die eine wichtige Rolle als organischer Osmolyt bei der Volumenregulation spielt, aber auch wichtige Rezeptoren im Gehirn stimuliert. Durch die Ausschaltung von LRRC8D wird es nun möglich sein, gezielt physiologische und pathologische Rollen der Taurin-Freisetzung durch VRAC zu untersuchen. Insgesamt hat die Studie einmal mehr bewiesen, wie schnell Grundlagenforschung zu klinisch bedeutsamen Ergebnissen führen kann.
Originalveröffentlichung
R. Planells‐Cases, D. Lutter, C. Guyader, N. M. Gerhards, F. Ullrich, D. A. Elger, A. Kucukosmanoglu, G. Xu, F. K. Voss, S. Momsen Reincke, T. Stauber, V. A. Blomen, D. J. Vis, L. F. Wessels, T. R. Brummelkamp, P. Borst, S. Rottenberg, T. J. Jentsch; "Subunit composition of VRAC channels determines substrate specificity and cellular resistance to Pt‐based anti‐cancer drugs"; EMBO; 2015