Nanopartikel aufspüren: Neue Kombination von Messmethoden
Biologische Proben beinhalten oft unzählige verschiedene Bio-Nanopartikel. Eine an der TU Wien entwickelte Methodenkombination schafft es nun, sie zu trennen und hochsensitiv zu detektieren.
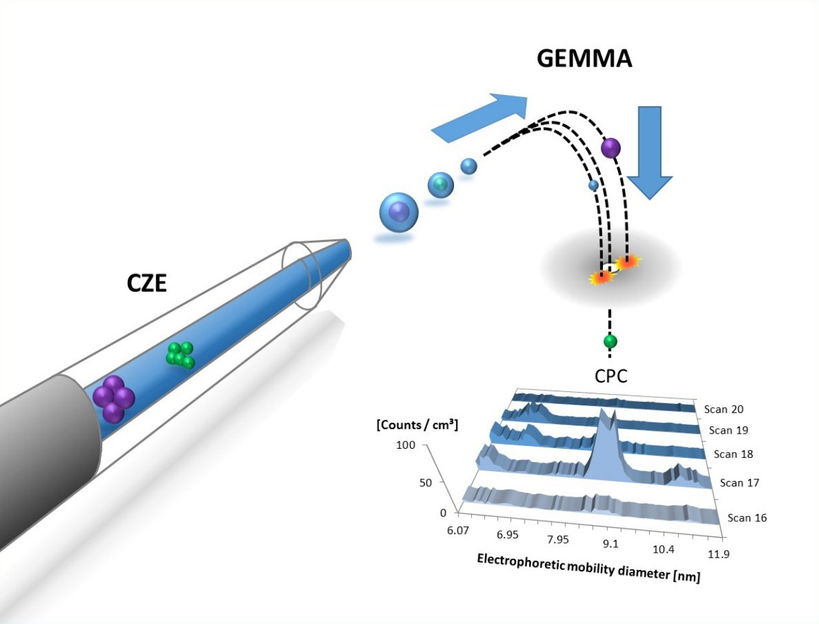
Die Substanz, die untersucht werden soll, wird durch eine Kapillare (links) geleitet (Capillary zone electrophoresis, CE), dann versprüht und in gasförmigem Zustand einem elektrischen Feld ausgesetzt.
TU Wien
Ob ein Impfstoff aus den richtigen Bestandteilen zusammengesetzt ist oder ob Lebensmittel bestimmte Nanopartikel enthalten, lässt sich oft nur durch sehr komplexe Messungen feststellen. An der TU Wien wurde nun ein neues Kombinationsverfahren entwickelt, das unterschiedliche bestehende Technologien verknüpft und damit eine genauere Analyse von Bio-Nanopartikeln im Bereich von fünf bis zweihundert Nanometern ermöglicht.
Gemische aus vielen unterschiedlichen Partikeln
„Der Bedarf nach Analysemethoden für vom Menschen hergestellte Bio-Nanopartikel ist sehr groß“, sagt Prof. Günter Allmaier vom Institut für Chemische Technologien und Analytik der TU Wien. „In vielen Bereichen, von der Medizin bis zur Nahrungsmittelindustrie, hat man es oft mit komplexen Mischungen zu tun – dazu können etwa Antikörper zählen, Viren, oder Proteinaggregate.“ Das Ziel ist, die vielen verschiedenen Partikel genau zu sortieren, zuverlässig zu detektieren und zu quantifizieren.
An der TU Wien gelang es nun, zwei ganz unterschiedliche Analysemethoden zu verbinden: Die Kapillarzonenelektrophorese (CZE), bei der die geladenen Partikel einer Flüssigkeit in einer dünnen Kapillare voneinander getrennt werden, und eine Art der Gasphasen-Elektrophorese (GEMMA), bei der Partikel in der Gasphase nach ihrer Größe sortiert werden können. „Der entscheidende Schritt bei unserer Arbeit war es, diese beiden Methoden direkt zu verknüpfen. Die Trennung der Nanopartikel findet bei uns also sowohl in der flüssigen als auch in der gasförmigen Phase statt“, erklärt Günter Allmaier.
Sortieren nach Ladung und Größe
Zunächst kommt eine kleine Menge der partikelenthaltenden Flüssigkeit in eine Kapillarröhre, an die eine Spannung angelegt wird. Je nach ihrer elektrischen Ladung wandern die einzelnen Komponenten unterschiedlich schnell durch die Kapillare – positiv geladene Teilchen in die eine, negativ geladene in die andere Richtung. Je stärker ein Partikel geladen ist, umso schneller wandert es. Zu unterschiedlichen Zeitpunkten tritt daher ein unterschiedlich zusammengesetztes Gemisch an Nanopartikeln aus. „Sobald die Teilchen die Kapllare verlassen, wird die Lösung versprüht, ladungsreduziert und mit Hilfe von eines differentiellen Mobilitätsanalysators in der Gasphase weiteranalysiert“, erklärt Günter Allmaier.
Im ersten Schritt, in der Flüssigkeit, werden die Partikel hauptsächlich anhand ihrer elektrischen Ladung, dem Molekulargewicht und der Form getrennt. Im zweiten Schritt, wenn die Nanopartikel in der Gasphase vorliegen, werden die Teilchen dann in erster Linie nach ihrem Durchmesser sortiert.
Die Teilchen der gasförmigen Probe werden in einem möglichst geradlinigen, verwirbelungsfreien Luftstrom mitgeführt. Im rechten Winkel zu ihrer Bewegungsichtung wird ein elektrisches Feld angelegt, das die Teilchen ablenkt. Wie stark sie dabei ihre Richtung ändern, hängt einerseits von ihrer Masse, andererseits aber auch ganz wesentlich von ihrer Größe ab. Am Ende werden die Teilchen mit einem Partikelzähler detektiert, der die Teilchen unabhängig von ihrer chemischen Natur zählt.
Gefahren erkennen, Qualität sichern
„Die beiden Methoden, die wir online verbinden konnten, ergänzen sich ganz hervorragend“, sagt Günter Allmaier. Allerdings war es eine Herausforderung, eine Flüssigphasenanalysenmethode mit einer Gasphasenmethode zu verknüpfen. Die Technik hebt die Analytik von biologischen, polymerbasierenden aber auch anorganischen Nanopartikeln nun auf eine neue Qualitätsebene. „Das ist wichtig für die strukturelle Beurteilung von Nanoobjekten, für die Qualitätssicherung in der industriellen Produktion und für die Risikobeurteilung von Nanopartikeln“, betont Allmaier.