Teamplayer in der Zelle
Neue Einblicke in die Energiegewinnung des Hitzeschock-Proteins Hsp90
Viele Enzyme funktionieren nur mit einer Art Co-Trainer. Wie diese Zusammenarbeit im Detail aussehen kann, zeigen Wissenschaftler der Technischen Universität München (TUM) mit einer neuen Methode exemplarisch am Hitzeschock-Protein Hsp90.

FRET-Aufbau im Labor
Bild: Christoph Ratzke / TUM
Interaktion von Hsp90 mit P23
Bild: Björn Hellenkamp / TUM

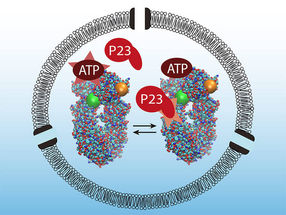
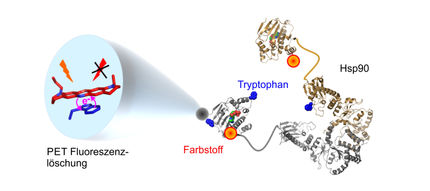
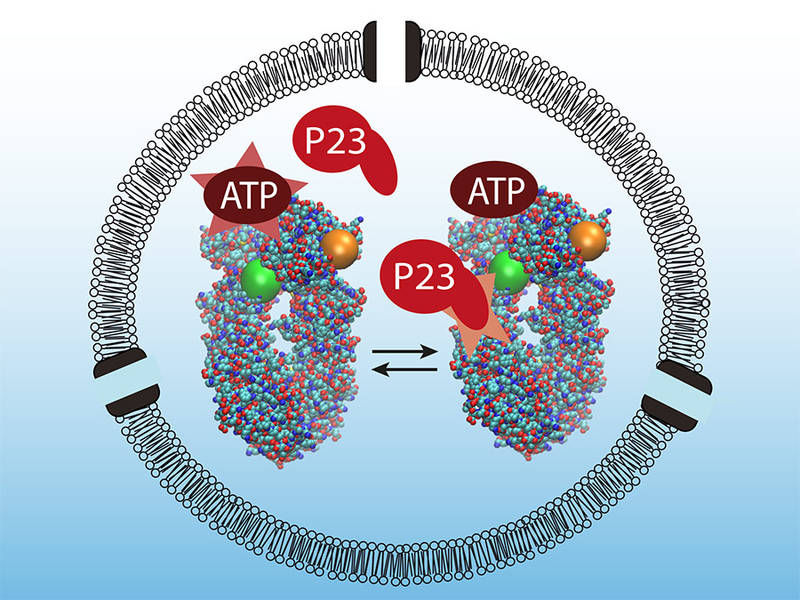
Wie für ein erfolgreiches Fußballspiel müssen auch in der Zelle alle Beteiligten perfekt aufeinander abgestimmt agieren. Ein typisches Beispiel für solch eine Zusammenarbeit liefert das Hitzeschock-Protein Hsp90, das die korrekte Faltung anderer Proteine kontrolliert. Gemeinsam mit einem zweiten Molekül, dem Co-Chaperon P23, kann es den Energieträger ATP spalten, um Energie für seine Arbeit zu gewinnen.
Doch während normale Enzym-Reaktionen oft gut zu verfolgen sind, weil sich das Protein dabei meist deutlich verformt, verläuft das Zusammenspiel mit P23 und ATP über unauffälligere Zustandsänderungen.
Einem Team unter Führung von Professor Thorsten Hugel, Leiter des Fachgebiets Molekulare Maschinen an der TU München und Mitglied des Exzellenzclusters Nanosystems Initiative Munich (NIM), ist es mit einer ausgeklügelten Methode nun erstmals gelungen, diese Reaktion im Detail zu beobachten, Schritt für Schritt an einem einzelnen Hsp90-Molekül, dem Protein P23 und ATP.
Liveübertragung der molekularen Abläufe
Dazu entwickelten sie die sogenannte FRET (Förster-Resonanzenergietransfer) Methode für ihre Zwecke weiter. Sie funktioniert mit Hilfe mehrerer unterschiedlich fluoreszierender Farbstoffmoleküle, die an bestimmte Stellen der beteiligten Komponenten binden. Wird der Komplex mit Licht einer definierten Wellenlänge angeregt, können die Farbstoffe in einer Art Kettenreaktion fluoreszieren. Das zurückkommende Fluoreszenzlicht zeigt den Wissenschaftlern auf den Nanometer genau den Abstand zwischen den markierten Stellen.
Um herauszufinden, wie genau die drei Komponenten Hsp90, P23 und ATP zusammenspielen, beobachten die Biophysiker die Positionen und die Abfolge der Bindungen zwischen den einzelnen Molekülen über einige Minuten. Aus den daraus gewonnen Daten können sie Rückschlüsse auf kleinste strukturelle Veränderungen, sowie auf die biologische Wirkung des Gesamtkomplexes ziehen.
Energiegewinnung nur im Team
Auf diese Weise konnten die Münchner Wissenschaftler im Detail zeigen, dass das Protein P23 die Bindung des ATP und somit die Energiegewinnung erheblich verstärkt. Belegen konnten sie auch, dass die beiden Substanzen nur im Team so effektiv an Hsp90 binden, dass die Spaltung des ATP zielgerichtet genutzt werden kann.
„Ohne P23 läuft das Hitzeschock-Enzym quasi im Leerlauf “, beschreibt Björn Hellenkamp, Doktorand in der Arbeitsgruppe Hugel, die Ergebnisse. „Kommt P23 dazu, ist es, als würde ein Gang eingelegt. Die Energie wird freigesetzt und die Reaktion bewegt sich klar in eine Richtung. Hier spricht man von Direktionalität.“
In Zukunft möchten die Biophysiker genauer untersuchen, wozu das Hsp90 die gewonnene Energie einsetzt. Zudem erlaubt ihnen die neu etablierte Methode auch, andere Multikomponentensysteme zu untersuchen, deren Mechanismen aufgrund zu geringer Konformationsänderungen bisher verborgen blieben.