Wie Umwelt und Genetik unsere Erbanlagen beeinflussen
Erste europäische Studie vorgelegt
Seit langem diskutiert die Wissenschaft darüber, wie groß der Einfluss der Umwelt auf die Gene ist. Ein europäisches Konsortium (EURATRANS) unter Leitung von Prof. Norbert Hübner (Max-Delbrück-Centrum, MDC) hat den umgekehrten Weg beschritten. Es ging erstmals der Frage nach, inwieweit bestimmte genetische Veranlagungen die Genregulation beeinflussen und versucht so zu erklären, warum bestimmte Umwelteinflüsse unterschiedlich wirken, etwa, warum Salz bei manchen Menschen den Blutdruck stark erhöht, bei anderen nicht. Mit ihrer Studie schlagen sie zudem einen neuen Wege zur Untersuchung dieser Phänomene ein, indem sie unterschiedliche genetische Analysemethoden miteinander verknüpfen.
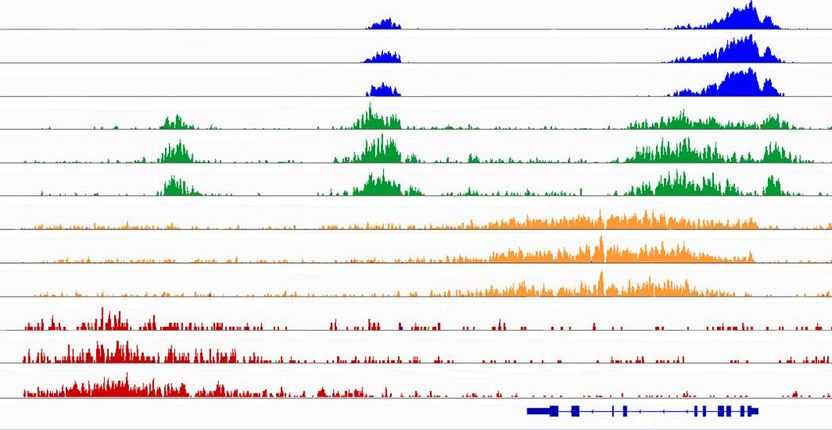
Die Graphik zeigt verschiedene Histonmodifikationen einer zufällig ausgewählten Region des Genoms von je drei Laborratten mit einem aktivierten Gen und einem nicht aktivierten Bereich (rot).
Graphik: Christin Mieth/Copyright: MDC
Der Mensch hat hunderte verschiedene Zellen, zum Beispiel Blut-, Nieren-, Leber-, oder Herzzellen. Alle Zellen – bis auf die roten Blutzellen – haben einen Zellkern, in dem die Erbsubstanz DNA mit ihren rund 20.000 Genen verpackt ist. Obwohl die Zellen alle dieselbe genetische Ausstattung haben, sind in den unterschiedlichen Zelltypen aber unterschiedliche Gene aktiv oder inaktiv. Wie die Gene gesteuert werden, wird seit langem intensiv erforscht.
„Epigenetik - Bindeglied zwischen Genen und Umwelt“
In diesem Zusammenhang ist vor einigen Jahren ist ein neuer Begriff in der Genetik aufgekommen: die Epigenetik. „Epigenetische Faktoren sind das Bindeglied zwischen Genen und Umwelt“, erläutert Dr. Carola Rintisch (MDC) dieses Phänomen. Zusammen mit Dr. Matthias Heinig (MDC und Max-Planck-Institut für Molekulare Genetik, Berlin) ist sie Erstautorin dieser Studie. Epigenetische Faktoren regulieren die Aktivität von Genen, ohne dabei die Abfolge der Genbausteine zu verändern. „Deshalb lag es nahe, auch zu untersuchen, inwieweit die Gene epigenetische Faktoren beeinflussen können“, so Dr. Rintisch weiter.
Im Mittelpunkt der Studie standen dabei die bei Histonen auftretenden Veränderungen (Modifikationen). Diese Histonmodifikationen zählen zu den epigenetischen Faktoren. Histone sind die Spulen, um die der DNA-Faden gewickelt ist. Je nachdem wie locker oder dicht die DNA um die Histone gepackt ist, können Gene abgelesen werden oder nicht. Den Verpackungszustand steuern Enzyme, die kleine Moleküle (Methylgruppen) an bestimmte Stellen in den Histonen binden. Die durch die unterschiedliche Methylierung hervorgerufenen Histonmodifikationen sind für die Genregulation entscheidend. Aber noch ist die Rolle der Histone und ihre Verpackungszustände wenig verstanden.
Ziel – Anfälligkeit für Krankheiten erkennen
Um den genetischen Einfluss auf die Histone zu untersuchen verglichen die Forscher die Genome zweier Rattenstämme – ein Stamm mit normalem Blutdruck – der andere Stamm mit Herz-Kreislauf-Krankheiten und Stoffwechselstörungen – mit den von ihnen erstellten Histonmodifizierungskarten. Schon dabei konnten sie Unterschiede in der Histonveränderung der beiden Stämme feststellen. Zur Ermittlung der genetischen Faktoren, die die Histonveränderungen auslösen, wurden weitere 30 Rattenstämme untersucht, die alle aus den zwei Ausgangsstämmen hervorgegangen sind und jeweils ein „genetisches Mosaik“ der beiden Rattenstämme besitzen.
Dr. Wei Chen vom Berliner Institut für Medizinische Systembiologie (BIMBS) des MDC sequenzierte anschließend die aufbereiteten Proben von Herz- und Lebergewebe der Tiere (ChIP-Sequenzierung). Vor allem im Herzgewebe ermittelten die Forscher zahlreiche Genregionen (QTLs – Quantitative Trait Loci), die die Histonveränderung und damit die Genaktivität beeinflussen.
„Unsere öffentlich zugänglichen Datensätze könnten dazu beitragen Genvariationen zu erkennen, die auf eine Anfälligkeit für Herz-Kreislauf und Stoffwechselerkrankungen hindeuten“, erklärt Prof. Hübner. „Zugleich haben wir mit unserer Vorgehensweise einen neuartigen Weg aufgezeigt, neue Verbindungen zwischen genetischer Ausstattung (Genotyp) und Umwelt (Erscheinungsbild Phänotyp) aufzudecken“.




















































