ERC-Grant für Bio-Materialforschung
Anzeigen
Mit Lasertechnologie will Aleksandr Ovsianikov an der TU Wien Mikrostrukturen mit eingebetteten lebenden Zellen bauen. Er erhält dafür einen der begehrtesten Europäischen Forschungspreise: Den ERC Starting Grant.

Dr. Aleksandr Ovsianikov

Ein Laser härted das flüssige Material genau am Fokuspunkt aus.
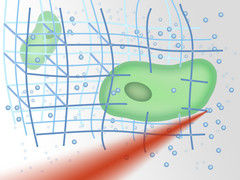
Ein dreidimensionales Netz kann hergestellt werden, das die Zellen festhält.

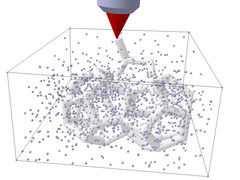
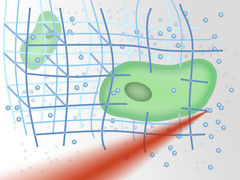
Das Verhalten von Zellen hängt stark von der Umgebung ab, in der sie sich befinden. Um Zellen zu untersuchen und zu beeinflussen ist es daher höchst wertvoll, sie in eine maßgeschneiderte Umgebung einbauen zu können. Aleksandr Ovsianikov entwickelt ein Laser-gesteuertes Verfahren, mit dem man Zellen gezielt in feine Strukturen einweben kann – ähnlich wie in natürlichem biologischen Gewebe, wo sie von der sogenannten „extrazellulären Matrix“ umgeben sind. Wichtig ist das für die Züchtung von neuem Gewebe, für die Suche nach neuen Medikamenten oder für die Stammzellenforschung. Für dieses Projekt erhielt Ovsianikov nun einen ERC-Grant des European Research Council (ERC), der mit knapp 1,5 Millionen Euro dotiert ist.
High-Tech-Strukturen für die biomedizinische Forschung
„Zellen auf einer ebenen Fläche anzusiedeln, ist nicht schwer. Doch solche Zellkulturen benehmen sich anders als Zellen in einer dreidimensionalen Struktur“, erklärt Alexandr Ovsianikov. Im Gegensatz zur klassischen 2D Zell-Kultur in der Petrischale gibt es zur Zeit keine Standards für 3D-Systeme. Eine solche 3D-Struktur muss durchlässig sein, damit die Zellen mit allen notwendigen Stoffen versorgt werden können. Die Geometrie und die chemischen oder mechanischen Eigenschaften der Struktur sollen präzise angepasst werden können, um die Reaktion der Zellen auf die äußeren Bedingungen studieren zu können. Außerdem soll die 3D-Struktur rasch in großer Anzahl herstellbar sein, denn um verlässliche Ergebnisse zu erzielen muss man Experimente an Zellen oft an vielen Zellkulturen gleichzeitig durchführen.
Genau diese Anforderungen kann die Forschungsgruppe „Additive Manufacturing Technologies“ der TU Wien bestens erfüllen: Das interdisziplinäre Team entwickelt seit Jahren spezielle Fertigungstechniken, mit denen sich dreidimensionale Strukturen mit einer Präzision im Mikrometer-Bereich herstellen lassen.
Laser verhärtet Flüssigkeit
Zu Beginn schwimmen die Zellen in einer Flüssigkeit, die hauptsächlich aus Wasser besteht. Beigemischt sind zellverträgliche Moleküle, die auf eine ganz bestimmte Weise mit Licht reagieren: Ein fokussierter Laserstrahl lässt genau an den gewünschten Stellen chemische Doppelbindungen brechen. Eine chemische Kettenreaktion führt dann dazu, dass sich die Moleküle zu einem Polymer verbinden.
Um diese Reaktion auszulösen, müssen zwei Photonen des Laserlichts gleichzeitig absorbiert werden. Nur dort, wo das Laserlicht fokussiert ist, gibt es ausreichend viele Photonen für diesen Prozess. Material außerhalb dieses Bereichs wird dadurch nicht beeinflusst. „Dadurch können wir mit extrem hoher Präzision bestimmen, an welchen Stellen sich die Moleküle verkleben sollen und ein festes Netzwerk bilden“, erklärt Ovsianikov.
Indem man den Fokus des Laserstrahls gezielt durch die Flüssigkeit lenkt, entsteht eine feste Struktur, in der die lebenden Zellen von Anfang an eingebaut sind. Die übrigen Moleküle, die nicht zu Polymeren verklebt wurden, können danach einfach weggewaschen werden. So kann man eine Struktur aus Hydrogelen bauen, ähnlich der extrazellulären Matrix, die unsere eigenen Zellen im lebenden Gewebe umgibt. Ideen aus der Natur werden im Labor imitiert und technologisch nutzbar gemacht: Diese Taktik – die Biomimetik - ist gerade in der Materialwissenschaft heute sehr gefragt. „Diese Technologie könnte in bestimmten Fällen auch Tierversuche unnötig machen, und dabei viel schnellere und aussagekräftigere Ergebnisse liefern“, hofft Ovsianikov.
Hoffnungsgebiet Stammzellenforschung
Ein besonders spannendes Anwendungsgebiet ist die Stammzellenforschung: „Wir wissen heute, dass sich Stammzellen je nach Umgebung zu unterschiedlichen Gewebetypen weiterentwickeln können“, sagt Aleksandr Ovsianikov. „So entwickeln sie sich etwa auf festerem Untergrund zu Knochenzellen, auf weicherem Untergrund zu Nervenzellen.“ In der Laser-generierten 3D-Struktur kann man die Steifigkeit des Untergrundes von Anfang an genau bestimmen und so möglicherweise ganz gezielt unterschiedliche Gewebetypen hervorbringen.























































