Lebens- und fortpflanzungsfähige Taufliegen ohne Histon H3.3
Anzeigen
Histone, die DNA verpackende Proteine, greifen anders in die Zellfunktion ein als bisher angenommen. Für das Ablesen der Gene braucht es das Histon H3.3 nicht. Molekularbiologen der Universität Zürich weisen nach, dass sich Taufliegen ohne dieses Histon entwickeln und fortpflanzen können. Ebenso funktioniert die Zellteilung ohne eine bisher für wichtig gehaltene Histonmodifikation.
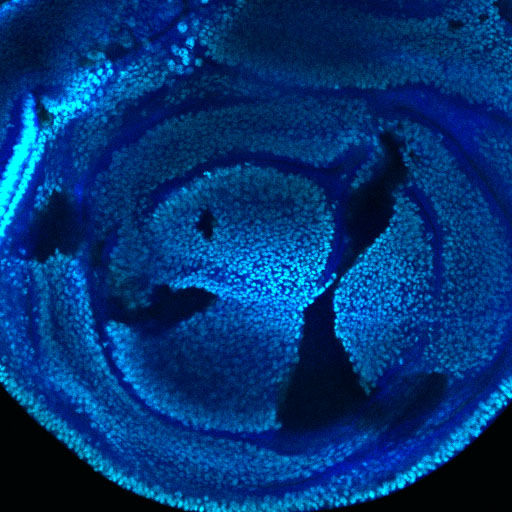
Flügel-Imaginalscheibe einer Taufliege: Die schwarzgefärbten Zellen können keine Histonmodifikation am Lysin vornehmen. Dennoch können sie sich teilen und Gene ablesen. Die dunkelblaue Färbung markiert die nicht-mutanten Zellen, Cyan markiert die Modifikation am Lysin.
UZH
Histone sind Proteine im Zellkern. Dort sind sie in Komplexen mit DNA vorhanden und vermutlich an allen Prozessen, die an der DNA stattfinden, regulatorisch beteiligt. Beispiele für diese Prozesse sind die Transkription, d.h. die RNA-Synthese, und die Verdoppelung der DNA im Zuge der Zellteilung. Die Funktion der einzelnen Histone bei den verschiedenen Prozessen konnte bisher nur indirekt erschlossen werden. Die Molekularbiologen Konrad Basler und Martina Hödl von der Universität Zürich untersuchten erstmals die Funktion von zwei Histonen und einer Histonmodifikation und kamen dabei zu überraschenden Resultaten: Lebens- und fortpflanzungsfähige Organismen entwickeln sich auch ohne das als H3.3 bezeichneten Histon. Von einer bestimmten Histon-Modifikation nahm man zudem an, dass sie für das Einschalten der Gene in der Transkriptionsphase ausschlaggebend sei. Wie die Forschenden nachweisen können, trifft auch diese Annahme nicht zu. Die gängigen Modelle über Aufgabe und Funktion bestimmter Histone und ihrer Modifikationen während der Transkriptions- und der Zellteilungsphasen müssen somit revidiert werden.
Lebensfähige Taufliegen trotz fehlendem Histon H3.3
Für ihre Fragestellung verwendeten der Molekularbiologe Konrad Basler und seine Postdoktorandin Martina Hödl die Taufliegen Drosophila melanogaster, deren Genom vollständig entschlüsselt ist. In einem ersten Experiment tauschten die Wissenschaftler in den Zellen die beiden Histon-Varianten H3.2 und H3.3 gegeneinander aus. In normalen, d.h. nicht manipulierten Zellen wird Histon H3.2 nur in einer bestimmten Phase der Zellteilung, der sogenannten S-Phase, exprimiert. Histon H3.3 dagegen ist dauernd aktiviert. Deshalb ging man bisher davon aus, dass Histon H3.3 in der Transkription, insbesondere beim Ablesen der Gene, eine wichtige Rolle spielt. Ohne Histon H3.3 müsste daher die RNA-Synthese eingeschränkt sein, lautet die gängige Lehrmeinung. «In unserem Experiment entwickeln sich aus Zellen, die kein H3.3 besitzen, Taufliegen, die unter Laborbedingungen lebens- und fortpflanzungsfähig sind», fasst Hödl das konträr zum bisherigen Verständnis stehende Resultat zusammen. «Organismen, die sich aus Zellen ohne H3.2 entwickeln, leben ebenfalls, sterben aber im ersten Larvenstadium», so Hödl weiter.
An- und Abschalten der Gene ohne Histonmodifikation
Histone werden von verschiedenen Enzymen an verschiedenen Stellen im Protein modifiziert. In einem zweiten Experiment untersuchten Basler und Hödl deshalb die Rolle der Aminosäure an der vierten Stelle im Protein, einem Lysin. Von diesem Lysin wird angenommen, dass seine Modifizierbarkeit bei der Transkription eine Schlüsselrolle für das An- und Abschalten der Gene spielt. Die Wissenschaftler ersetzten folglich dieses Lysin in allen Histon H3-Genen mit nicht modifizierbaren Aminosäuren und erlebten eine zweite grosse Überraschung. «Zellen ohne diese spezifische Histonmodifikation sind in der Lage sich normal zu teilen», erläutert Basler, fügt aber einschränkend hinzu: «Allerdings tun sie dies wesentlich langsamer als nicht veränderte Zellen.» Die Modifikation an diesem Lysin ist somit nicht essentiell für das Anschalten der Gene in der Transkriptionsphase.
Die Resultate zeigen, dass das Aktivieren von Genen und die Vererbung der Fähigkeit, Gene zu aktivieren, anders funktionieren als bisher angenommen. Offensichtlich ist der Transkriptionsprozess ausgesprochen robust aufgebaut. Gemäss Basler wurde die Rolle dieser häufig vorkommenden Histonmodifikation für die Zellfunktion in den vergangenen Jahren überschätzt.

























































