Arzneimittelinnovation 2024
43 neue Medikamente und 22 Zulassungserweiterungen in 2024: Zwei neue Reserveantibiotika
Pharmaunternehmen haben 2024 in Deutschland 43 Medikamente mit neuem Wirkstoff auf den Markt gebracht. Das ist die vierthöchste Zahl der vergangenen 20 Jahre und ein deutlicher Anstieg gegenüber 2023, als es 30 Neueinführungen gab. Dazu kamen noch einmal 22 Medikamente, deren Anwendungsgebiet die Hersteller auf weitere Krankheiten ausdehnen konnten. Dazu sagt vfa-Präsident Han Steutel: „Deutschland braucht Innovationen auf allen Feldern der Gesellschaft. Im Gesundheitssystem bleibt die Pharmaindustrie ein Fortschrittsmotor. Ihre Markteinführungen und Zulassungserweiterungen dieses Jahres werden vielen Patientinnen und Patienten zugutekommen.”

Deutsche Kliniken und Arztpraxen an der Erprobung von 72 Prozent dieser Medikamente beteiligt (Symbolbild).
Computer-generated image
Breite Verteilung auf die Anwendungsgebiete
Die 43 Medikamente mit neuem Wirkstoff, die 2024 in Deutschland eingeführt wurden, verteilen sich wie folgt auf verschiedene Anwendungsgebiete:
- Krebserkrankungen: 12
- Immunologische Erkrankungen: 10
- Infektionskrankheiten: 6
- Stoffwechselkrankheiten: 3
- Neurologische Krankheiten (ohne Krebs und Autoimmunkrankheiten): 2
- Gynäkologische Krankheiten (ohne Krebs und Infektionskrankheiten): 2
- Herz-Kreislauf-Erkrankungen: 1
- Muskelerkrankungen: 1
- Knochenerkrankungen: 1
- Blutungskrankheiten: 1
- Bildgebende Verfahren: 1
- Sonstige: 3
Zu den „Immunologischen Erkrankungen“ werden Autoimmunkrankheiten, allergische Erkrankungen und angeborene Immundefekte gezählt.
Krebserkrankungen
Besonders viele Neueinführungen gab es 2024 für Krebspatient:innen: Elf Medikamente kamen zur Bekämpfung unterschiedlicher Tumorarten heraus, zudem eins zur Linderung einer Neutropenie (eines Mangels an bestimmten weißen Blutkörperchen) nach Chemotherapie.
Sechs der elf Medikamente gehören zu den Kinase-Inhibitoren. Sie blockieren jeweils eine oder mehrere der zahlreichen Kinasen, die in Zellen als Schalter bei der Steuerung der Zellteilung dienen. Bei vielen Krebserkrankungen sind sie so mutiert, dass sie eine rasche Zellvermehrung fördern.
Reserveantibiotika
Neue Antibiotika, die auch bei multiresistenten Bakterien wirksam sind, werden dringend gebraucht. In diesem Jahr haben Unternehmen zwei solche Medikamente herausgebracht. Bei beiden schützt ein zweiter Wirkstoff den eigentlichen antibiotischen Wirkstoff, indem er ein Enzym der Bakterien „ausknockt“, das sonst den antibiotischen Wirkstoff zerstören würde. Als Reserveantibiotika sind beide Medikamente dazu gedacht, nur dann eingesetzt zu werden, wenn wirklich multiresistente Bakterien die Krankheitsursache sind.
„Um auf Dauer mit der Verbreitung neuer Resistenzen Schritt zu halten, sind zwei neue Antibiotika pro Jahr nicht genug“, kommentiert Steutel. „Deshalb ist zu hoffen, dass sich die EU in ihrer Pharmagesetzgebung 2025 dazu entschließen kann, Anreize für die Entwicklung von mehr neuen Antibiotika zu setzen.“
Schutzimpfungen
2024 kamen zwei Impfstoffe neu auf den Markt – gegen Tollwut und gegen das Atemwegsvirus RSV. Die RSV-Vakzine ist der erste Impfstoff auf messenger-RNA-Basis, der Schutz vor einer anderen Krankheit als Covid-19 bietet.
Medikamente gegen seltene Erkrankungen
Als selten werden Krankheiten in der EU bezeichnet, wenn nicht mehr als fünf von 10.000 EU-Bürger:innen darunter leiden. Ist das bei einem Medikament gegeben, und fehlt es außerdem an einer zufriedenstellenden Behandlungsoption oder ist es bisherigen Medikamenten signifikant überlegen, kann ihm die europäische Arzneimittelagentur auf Antrag den „Orphan Drug Status“ zuerkennen. Das hat sie bei insgesamt 18 der neu eingeführten Medikamente (42 Prozent) getan. Insgesamt kamen aber sogar 27 Medikamente (63 Prozent) zur Behandlung seltener Erkrankungen heraus. Dazu Steutel: „Das zeigt das anhaltende Engagement der Branche dafür, dass auch Patientinnen und Patienten nicht unversorgt bleiben, deren Krankheit nicht häufig vorkommt.“
Gleich drei der Medikamente dienen der Behandlung von Menschen mit paroxysmaler nächtlicher Hämoglobinurie (PNH) – einer Krankheit, bei der das Immunsystem u.a. rote Blutkörperchen angreift. Zwei Medikamente kamen gegen Myastenia gravis heraus. Patient:innen mit dieser Krankheit leiden an Muskelschwäche, weil Attacken des Immunsystems die Übertragung von Nervensignalen auf die Muskeln beeinträchtigen.
Herstellungsarten
Ungewöhnlich ist am Jahrgang 2024, dass 30 und damit 70 Prozent der neuen Wirkstoffe ganz oder teilweise chemisch-synthetisch hergestellt werden. 2022 und 2023 waren es nur 41 Prozent bzw. 33 Prozent. „Daran sieht man, dass auch die Chemie weiter große Bedeutung für Arzneimittelinnovationen hat“, so Steutel. 13 (28 Prozent) der neuen Medikamente enthielten gentechnisch hergestellte Protein-Wirkstoffe (in einem Fall gekoppelt mit einem chemischen Wirkstoff). Gen- oder Zelltherapien kamen 2024 keine dazu; erst 2025 dürften weitere eingeführt werden.
Der Beitrag Deutschlands
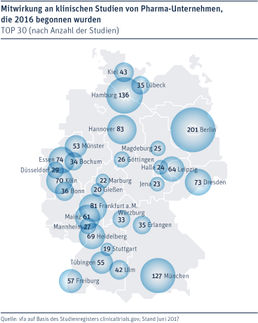
Nur bei einem der 43 neuen Medikamente wurde der Wirkstoff unter Beteiligung deutscher Labors entwickelt – für ein Medikament gegen paroxysmale nächtliche Hämoglobinurie. Aber deutsche Krankenhäuser oder Arztpraxen waren an der Erprobung von 31 Medikamenten (72 Prozent) in klinischen Studien beteiligt. „Doch mit dieser Quote sollte sich Deutschland künftig nicht zufriedengeben“, kommentiert Steutel. „Es sollte seine Attraktivität für klinische Studien wieder so steigern, dass Unternehmen bei möglichst vielen ihrer Medikamente hiesige medizinische Einrichtungen einbeziehen – es sei denn, es ginge um Tropenkrankheiten. Mit dem Medizinforschungsgesetz hat die Bundesregierung die Weichen dafür richtig gestellt; doch viel hängt davon ab, ob die nächste Regierung es auch vollständig umsetzt.“
Fortschritte auch durch Zulassungserweiterungen
Pharmaunternehmen haben nicht nur neue Medikamente auf den Markt gebracht: Gleich 22-mal haben sie auch vorhandene Medikamente gegen zusätzliche Krankheiten anwendbar gemacht, indem sie nach einschlägigen klinischen Studien Zulassungserweiterungen erwirkt haben. Die meisten solchen Erweiterungen betrafen Krebserkrankungen.