Krebsbekämpfung mit kombinierten Immuntherapien
Neue Kombination aus Impfstoff und Immun-Checkpoint-Inhibitoren als vielversprechender Ansatz zur Verbesserung der Krebsbekämpfung
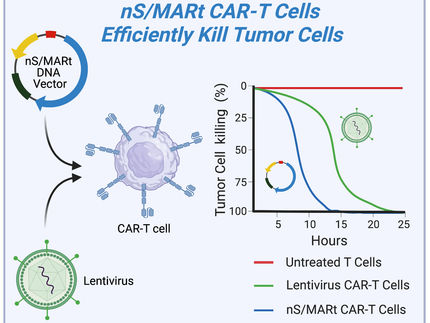
Laut einer neuen Studie von Immunologen der Universität Konstanz könnte ein neuer Krebsimpfstoff die positive Wirkung bestehender Immuntherapie-Medikamente verstärken und die Erfolgsquote der Behandlungen von 20% auf 75% steigern. Der Impfstoff, der ein neues Immunstimulans enthält, das auch für den Einsatz beim Menschen geeignet ist, konnte die in der Studie behandelten Mäuse teilweise von Tumoren befreien. Die Studie zeigte zudem, dass die Kombination des Impfstoffs mit einem Immun-Checkpoint-Inhibitor – einem etablierten Immuntherapie-Medikament mit einer Erfolgsquote von bis zu 20% beim Menschen – den Anteil an Mäusen, die auf die Behandlung ansprechen, deutlich erhöhen kann, so dass der Tumor in 75% der Fälle verschwindet. Die Ergebnisse deuten darauf hin, dass dieser neue Ansatz, bei dem ein Impfstoff in Kombination mit etablierten Medikamenten zum Einsatz kommt, eine wirksame Immuntherapie gegen Krebs sein könnte, die in zukünftigen klinischen Studien getestet werden sollte. Veröffentlicht wurden die Ergebnisse am 18. Mai 2021 in Nature Communications.
Symbolbild
Photo by National Cancer Institute on Unsplash
Die Krebstherapie hat in den letzten Jahren durch eine bestimmte Art der Immuntherapie, die sogenannte „Immun-Checkpoint-Inhibition“, einen großen Durchbruch erlebt. Immun-Checkpoint-Inhibitoren wirken, indem sie das natürliche Herunterfahren der körpereigenen Immunantwort stoppen und stattdessen dazu führen, dass der Körper die Tumorzellen weiterhin angreift. Dies hat sich bei bestimmten Krebsarten, wie Melanomen und Plattenepithelkarzinomen der Haut, Lungenkrebs, Nierenkrebs und Leberkrebs, als wirksam erwiesen.
Aber nicht alle Krebspatienten sprechen auf diese Immuntherapie an. Beispielsweise können lediglich 20% der Melanom-Patienten geheilt werden. Warum viele von ihnen nicht gut auf die Behandlung ansprechen, kann damit erklärt werden, dass der Körper erst selbst eine Immunantwort einleiten muss, die die Medikamente dann verlängern. Wenn der Körper seine Tumorzellen nicht als fremd erkennt, haben die Immun-Checkpoint-Inhibitoren keine Immunzellen als Ansatzpunkt.
Jetzt entwickelte das Team des Immunologen Prof. Dr. Marcus Groettrup an der Universität Konstanz eine Technik, die eine solche Immunantwort gegen den Tumor auslöst. Der mikropartikelbasierte Krebsimpfstoff, der das für die Anwendung beim Menschen zugelassene Immunstimulans Riboxxim verwendet, kann die körpereigene T-Zell-Antwort hervorrufen, die für die Wirksamkeit von Immun-Checkpoint-Blockade-Medikamenten notwendig ist.
„Ein großes Manko bei Krebsimpfstoffen ist die Verfügbarkeit von Immunstimulanzien, die beim Menschen eingesetzt werden können“, sagt Marcus Groettrup, Seniorautor der Studie. „Unser klinisch einsetzbarer Impfstoff führt in Kombination mit der Immun-Checkpoint-Blockade zu einer Steigerung des Anteils der Mäuse, die von bestehenden Tumoren geheilt werden können, auf 75 Prozent.“
Ein für Menschen sicherer Krebsimpfstoff
Ziel der Studie war es, einen partikelbasierten Krebsimpfstoff zu entwickeln, der eine effektive Immunantwort gegen Tumore auslöst und der für die klinische Anwendung geeignet ist.
Das Team erzeugte Partikel mit einer Größe von 1 Mikrometer (oder 0,001 mm), die ein Tumorprotein und Riboxxim enthielten – ein Molekül, das das Immunsystem zu einer Antwort anregt. Riboxxim wird von dem Unternehmen Riboxx Pharmaceuticals in Dresden hergestellt.
Bei Mäusen, denen eine Einzeldosis des Impfstoffs auf Mikropartikelbasis injiziert wurde, wurde eine starke Anti-Tumor-Immunantwort ausgelöst, die auch nach acht Wochen noch nachweisbar war. Selbst sehr geringe Dosen des Impfstoffs konnten eine im Vergleich zu anderen Immunstimulanzien starke Immunantwort auslösen.
Das Team testete den Impfstoff mit einer Reihe von Krebsproteinfragmenten, zum Beispiel denen von Prostatakrebs, Brustkrebs und Melanomen. Bei Mäusen wurde eine starke zelluläre Immunantwort gegen alle diese Antigenfragmente erzielt, was darauf hindeutet, dass der neue Ansatz bei einer Vielzahl von Krebsarten angewendet werden könnte.
Eine synergetische Kombination
Aufgrund der natürlichen Herunterregulierung der körpereigenen Immunantwort kehrten die Tumore jedoch 30 Tage nach der Impfung allmählich zurück. Wurde der Impfstoff allerdings mit einem Immun-Checkpoint-Inhibitor kombiniert, hielt die positive Wirkung an und die Tumore wurden besiegt.
„Wir konnten eine klinisch anwendbare Krebsimmuntherapie entwickeln, die komplementär zur gängigen Immuntherapie wirkt“, sagt Dennis Horvath, der zusammen mit Julia Körner Erstautor der Studie ist. Horvath is Doktorand am Exzellenzcluster „Centre for the Advanced Study of Collective Behaviour‟ (CASCB) der Universität Konstanz. Er nutzt diesen Impfansatz auch, um die Wirkung von sozialem Stress auf die Immunantwort von Mäusen zu untersuchen und zu testen, ob eine Immunsuppression durch Stress den therapeutischen Erfolg einer Immuntherapie einschränkt.
Basierend auf den Ergebnissen der Studie schlagen die Forschenden vor, diese vielversprechenden präklinischen Ergebnisse in die klinische Anwendung zu überführen. „Das könnte einen sehr positiven Einfluss auf die Immuntherapie bei bestimmten Krebsarten haben“, so Groettrup.
Das in dieser Studie entwickelte Therapiekonzept wird derzeit von Projektpartnern in Nimwegen (Niederlande) in einer ersten Phase-1-Studie getestet, um herauszufinden, ob es auch beim Menschen ähnlich wirksam ist.