Live bei der Zellteilung zugeschaut
Höchstauflösende Einblicke in lebende Zellen
Bakterien als einzellige Lebewesen vermehren sich normalerweise durch eine binäre Zellteilung, also die Vervielfältigung des gesamten einzelligen Organismus. Dies erlaubt eine besonders schnelle Vervielfältigung, wie die von Krankheitserregern bekannte exponentielle Vermehrung, und erfordert die Auftrennung und Verteilung von zwei identischen Kopien des bakteriellen Erbguts. Eine wichtige Rolle bei der Zellteilung spielt für eine Bakterienzelle dabei die Position, an der sie sich teilt und dabei die Erbinformationen verteilt. Für viele Bakterienarten wie beispielsweise das Stäbchenbakterium Escherichia coli ist dieser Prozess gut erforscht: Als Steuerungseinheit fungiert hier eine Gruppe von Proteinen, die als das Min-System bezeichnet wird und in Bakterien normalerweise dafür sorgen, dass sich die Zellen genau in der Mitte teilen. An der Christian-Albrechts-Universität zu Kiel (CAU) beschäftigt sich die Arbeitsgruppe Mikrobielle Biochemie und Zellbiologie um Professor Marc Bramkamp unter anderem mit bakteriellen Organisations- und Reproduktionsmechanismen, anhand derer sie allgemeingültige Prinzipien der biologischen Musterbildung untersuchen. Diese Musterbildung ist in der Biologie von zentraler Bedeutung, etwa bei der Entstehung komplexer vielzelliger Lebewesen.
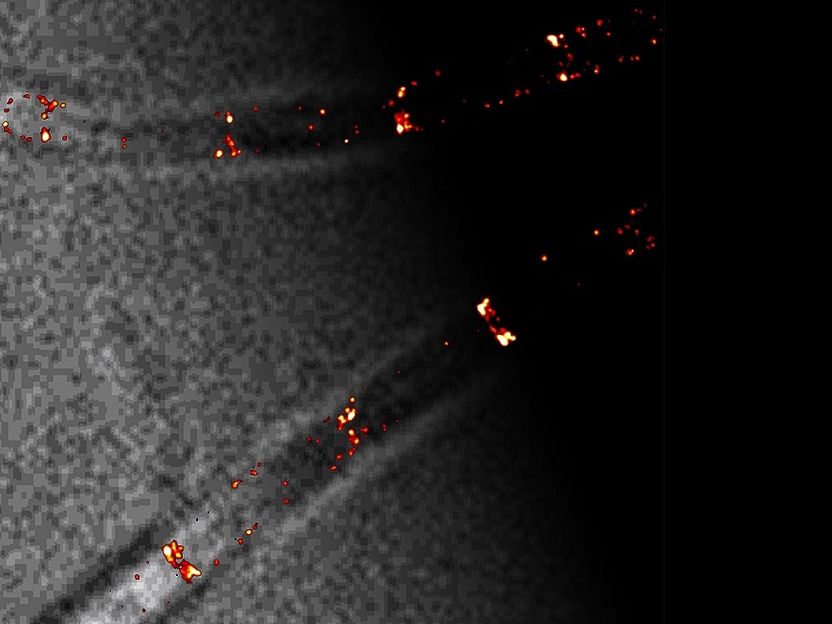
Bestimmte fluoreszierend markierte Proteine des Min-Systems (in rot) sind an ihren Positionen in einer B. subtilis-Zelle zu erkennen. Die mit Hilfe der Einzelmolekül-Lokalisationsmikroskopie erreichte Protein-Lokalisationen ist etwa zehnmal genauer als mit herkömmlicher Lichtmikroskopie.
© Prof. Marc Bramkamp
In einer neuen Forschungsarbeit konnten Bramkamp und sein Team vom CAU-Institut für Allgemeine Mikrobiologie am Beispiel des Bakteriums Bacillus subtilis neue Erkenntnisse darüber gewinnen, wie die Proteine des Min-Systems infolge evolutionärer Anpassungen ihre Funktionsweise in der Zellteilung anpassen können. Dank neuartiger hochauflösender Bildgebungsverfahren und der Anwendung mathematischer Modellierungen konnten sie zeigen, dass das Min-System bei B. subtilis nicht die Positionierung der Zellteilung reguliert, sondern diese nach einer erfolgreichen Teilung stoppt - anders als bei vielen anderen Stäbchenbakterien. Die neuen Ergebnisse veröffentlichten die Kieler Forschenden gemeinsam mit Kooperationspartnern an der Ludwig-Maximilians-Universität München im wissenschaftlichen Fachzeitschrift mBio.
Unterschiedliche Dynamik der Zellteilungs-Proteine
Um nachvollziehen zu können, wie die Proteine des Min-Systems in B. subtilis-Zellen agieren, wählte das Kieler Forschungsteam zunächst einen zweistufigen Ansatz. Ergebnisse aus vorangegangen Experimenten ließen vermuten, dass die an der Zellteilung beteiligten Proteine nicht statisch sind, sondern sich je nach Aktivitätszustand dynamisch in der Zelle bewegen. Die Forschenden haben sie daher im Experiment zunächst mit einem fluoreszierenden Eiweiß markiert. Mit einem speziell ausgestattetem Fluoreszenzmikroskop konnten sie dann die Bewegungen der Proteine in der Zelle in Echtzeit verfolgen. „Bei E. coli gibt es eine sogenannte Oszillation der Min-Proteine. Ihr Vorkommen wandert dabei in wenigen Sekunden von einem Ende der Zelle zum anderen. Daher ist die Verteilung in der genauen Mitte der Zelle am geringsten. Genau dort entsteht dann in E. coli das Septum, also eine neu entstehende Trennwand“, erklärt Dr. Helge Feddersen, wissenschaftlicher Mitarbeiter in Bramkamps Gruppe. „Bei B. subtilis konnten wir mit unseren Messungen jedoch keine solche Oszillation feststellen. Unsere Beobachtungen zeigten aber, dass die Min Proteine von den Zellpolen zur Mitte wandern, sobald dort die Zellteilung beginnt. Eine Dynamik der Proteine ist in B. subtilis also erhalten, aber das System legt nicht die Zellmitte fest“, so Feddersen weiter.
Um eine genaue Vorstellung von der Geschwindigkeit der Proteine in der Zelle zu bekommen, wandte das Kieler Team in einem zweiten Schritt ein Verfahren zur lokalen Entfernung der fluoreszierenden Markierung an. Die Fluoreszenz wurde also beispielsweise gezielt bei den Proteinen, die sich am Teilungs-Septum der Zelle befanden, mittels eines Lasers durch Bleichung dauerhaft ausgeschaltet. Trotzdem fanden sich kurz darauf an derselben Position erneut fluoreszierende Proteine - diese konnten also nur von einem anderen Ort der Zelle dorthin nachgewandert sein. „Daraus konnten wir ganz genau ableiten, mit welcher Geschwindigkeit sich die Min-Proteine bei B. subtilis in der Zelle bewegen. Diese quantitativen Daten sind sehr wichtig, um ein mathematisches Modell der Min Dynamik zu erstellen“, fasst Feddersen das wichtigste Ergebnis zusammen. Um die in den lebendigen Zellen beobachteten Vorgänge zu bestätigen, haben die Kieler Forschenden mit der Arbeitsgruppe des Physikers Professor Erwin Frey an der LMU zusammengearbeitet. In einem theoretischen Modell konnten die Münchener Kooperationspartner die Bewegungsmuster des Min-Systems auch theoretisch bestätigten – ein wichtiges Zeichen, dass bereits in den Beobachtungen alle für die Funktion wesentlichen Teile des Proteinsystems erkannt wurden.
Höchstauflösende Einblicke in lebende Zellen
Dass die neuen Erkenntnisse über die abweichende Funktion des Min-Systems bei B. subtilis erst jetzt gefunden wurden, liegt auch daran, dass die Auflösung in der Bildgebung für solche Beobachtungen bisher nicht ausreichte. An der CAU steht mit der Einzelmolekül-Lokalisations-Mikroskopie seit kurzem eine hochleistungsfähige Technologie zur Verfügung, welche die bisher beste Auflösung in lebenden Zellen ermöglicht. Damit ist es möglich, auf der Nanometer-Skala einzelne Moleküle wie die Min Proteine in lebenden Zellen zu lokalisieren. Anders als bei statischen Verfahren lässt sich so zudem die Dynamik verfolgen, also die Bewegung einzelner Proteine im Zeitverlauf nachvollziehen. „Erst mit unserem höchstauflösenden Mikroskop konnten wir nun im nächsten Schritt feststellen, dass es zu einer Clusterbildung bei den Zellteilungs-Proteinen von B. subtilis kommt“, betont Bramkamp, Leiter der Arbeitsgruppe Mikrobielle Biochemie und Zellbiologie. „Mit der neuen Mikroskopie-Technologie ist die CAU in der biologischen Bildgebung nun exzellent aufgestellt. Im Rahmen der Zentralen Mikroskopie (ZM) am Biologiezentrum steht sie auch anderen Nutzerinnen und Nutzern aus diversen Disziplinen an der Landesuniversität zur Verfügung“, so Bramkamp, wissenschaftlicher Leiter der ZM an der Kieler Universität.
„Diese in der Biologie noch selten genutzte Technik hat uns in der nun vorgelegten Arbeit gezeigt, dass ein scheinbar bekanntes Proteinsystem bei dem konkret untersuchten Bakterium möglicherweise wesentlich anders funktioniert, als bisher angenommen“, so Bramkamp weiter. Obwohl also beispielsweise bei E. coli und B. subtilis dieselben Proteinsysteme vorliegen, führen sie völlig andere Funktionen aus. „Wir vermuten, dass das Min-System bei B. subtilis bewirkt, dass die Zellteilung nach einem erfolgreichen Durchgang blockiert wird – es beeinflusst also den aktiven Zellteilungsapparat und sorgt dafür, dass dieser nach erfolgreicher Teilung nicht weiterarbeitet“, fasst Bramkamp zusammen. Der Grund für diese Anpassung liegt möglicherweise darin, dass B. subtilis eine besondere Überlebensstrategie verfolgt und - im Gegensatz etwa zu E. coli - gegen schädliche Umwelteinflüsse resistente Dauerstadien in Form von Sporen bildet. Damit sich diese Sporen ausbilden können, muss sich die Zelle nahe am Zellpol teilen - also der Stelle, an der normalerweise keine Teilung stattfinden soll. Diese Anforderung erreicht B. subtilis also offenbar durch die Modifikation des Min-Systems und ermöglicht so diese einfache Form der Zelldifferenzierung bei der Sporulation.