Durchbruch in der Entwicklung neuer anti-entzündlicher Therapien
Neuartiger Behandlungsansatz wirkt auch bei Patienten mit chronischen Darmentzündungen
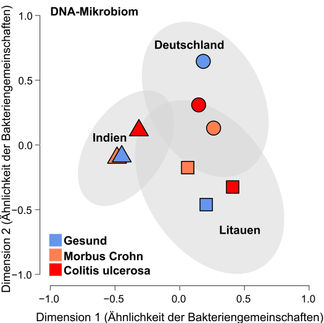
chronisch-entzündliche Darmerkrankungen (CED) wie Morbus Crohn und Colitis ulcerosa führen zu dauerhaft wiederkehrendem Durchfall, Fieber und Schmerzen sowie schwerwiegenden psychischen Belastungen. In Deutschland sind rund 320.000 Menschen von CED betroffen. Bei ihnen führt eine gestörte Immunantwort zu einer Entzündung im Magen-Darm-Trakt, die in Schüben immer wieder aufflammt. Es gibt nur wenige zugelassene Medikamente für diese Erkrankungen und diese wirken bei weitem nicht bei allen Betroffenen, sondern jeweils nur bei einigen. Es besteht daher ein großer Bedarf an Therapien, die über neue Wirkmechanismen die chronischen Darmentzündungen bekämpfen. Forschende des Exzellenzclusters „Precision Medicine in Chronic Inflammation“ haben vor einiger Zeit ein Fusionsprotein konstruiert, das zum jetzt untersuchten Wirkstoffkandidaten „Olamkicept“ weiterentwickelt wurde. Es unterdrückt über einen neuen Mechanismus die Entzündung im Darm – doch bisher konnte dies nur in verschiedenen Tiermodellen gezeigt werden. In einer vor kurzem im Fachmagazin Gastroenterology veröffentlichten Studie weist das Team um Professor Stefan Schreiber, Sprecher des Exzellenzcluster PMI, Direktor des Instituts für klinische Molekularbiologie (IKMB) der Christian-Albrechts-Universität und des Universitätsklinikums Schleswig-Holstein (UKSH), Campus Kiel, und Direktor der Klinik für Innere Medizin I des UKSH, Campus Kiel, nach, dass Olamkicept auch bei Patienten mit chronischen Darmentzündungen den entscheidenden Signalweg blockiert und so die Entzündung erfolgreich dämpfen kann.

Prof. Dr. Stefan Schreiber, Sprecher des Exzellenzclusters „Precision Medicine in Chronic Inflammation“ (PMI), Direktor des Instituts für Klinische Molekularbiologie, CAU und UKSH, und Direktor der Klinik für Innere Medizin I, UKSH, Campus Kiel.
J. Haacks, Uni Kiel
Neuer Wirkmechanismus über IL-6-Trans-Signalweg
Olamkicept wirkt über einen speziellen Signalweg eines wichtigen Botenstoffs des Immunsystems, des sogenannten Interleukin (IL)-6. Dieses Signalmolekül wird bei einer Entzündung vom Körper vermehrt ausgeschüttet und hilft bei der Regulation der ablaufenden Immunprozesse. Wenn jedoch ein Medikament alle Wirkungen von IL-6 blockiert, dämpft dies zwar sehr erfolgreich die Entzündung, aber gleichzeitig kann es zu schweren Nebenwirkungen kommen. Durch die Blockade von IL-6 kann das Immunsystem so stark unterdrückt werden, dass der Körper deutlich anfälliger gegenüber Infektionen wird. Dies ist bei bereits erhältlichen Antikörpern gegen IL-6 oder seinen spezifischen Rezeptor der Fall.
„Das Besondere an Olamkicept ist, dass es gezielt nur einen Teil der IL-6-Wirkung über den sogenannten IL-6-Trans-Signalweg hemmt. Vorangegangene Forschungsarbeiten deuten darauf hin, dass der klassische IL-6-Signalweg vor allem bei der Immunabwehr beispielsweise gegen Krankheitserreger eine Rolle spielt. Wir gehen davon aus, dass der Trans-Signalweg hingegen besonders bei chronischen Entzündungen aktiv ist“, erklärt Co-Autor Professor Philip Rosenstiel, Vorstandsmitglied im Exzellenzcluster PMI und Direktor des IKMB. „Indem wir gezielt nur den Trans-Signalweg blockieren, bleibt der für eine gesunde Immunreaktion wichtige klassische IL-6-Signalweg ungestört“, erklärt Rosenstiel.
Beim „klassischen“ Signalweg bindet IL-6 spezifisch an seinen Rezeptor, der nur auf der Oberfläche bestimmter Zellen, wie beispielsweise Immun- oder Leberzellen, vorkommt. Gemeinsam binden sie dann an ein weiteres Oberflächenprotein auf derselben Zelle, das sogenannte gp130-Protein, und lösen so eine Reaktion in der Zelle aus. Aber der IL-6-Rezeptor kommt auch in löslicher Form im Blut vor. Beim alternativen IL-6-Trans-Signalweg bindet IL-6 an diesen im Blut zirkulierenden Rezeptor und dann an gp130, das auf allen Zellen vorkommt. So kann IL-6 theoretisch auf jede Zelle im Körper wirken.
Von der Grundlagenforschung bis zur Arzneimittelentwicklung
Diesen alternativen Signalweg hatte Professor Stefan Rose-John, Clustermitglied und Direktor des Biochemischen Instituts der CAU, vor mehr als 20 Jahren entdeckt und Pionierarbeit in dessen Erforschung geleistet. Gemeinsam mit Kolleginnen und Kollegen hatte er darauf basierend das Fusionsprotein „sgp130Fc“ entwickelt, den Prototyp von Olamkicept. Es fängt den Komplex aus IL-6 und löslichem Rezeptor aus dem Blut ein und blockiert dadurch den Trans-Signalweg, ohne die positiven Wirkungen von IL-6 über den „klassischen“ Weg zu stören.
Zur Verbesserung seiner Wirkung und zur großtechnischen Herstellung wurde das Protein von der Kieler Biotechnologiefirma CONARIS Research Institute AG zum Medikamentenkandidaten Olamkicept weiterentwickelt. Die pharmazeutische Firma Ferring betreibt zusammen mit CONARIS und der chinesischen Pharmafirma I-Mab Biopharma die Entwicklung von Olamkicept als Arzneimittel. Die gerade veröffentlichten Ergebnisse sind Teil eines größeren Programms, das auch Placebo-kontrollierte Wirksamkeitsuntersuchungen umfasst.
Wirkmechanismus bei Patienten bestätigt
In zahlreichen Tiermodellen haben sgp130Fc und Olamkicept bereits ihre Wirksamkeit bewiesen und bekämpften erfolgreich chronische Entzündungen, ohne das Immunsystem zu unterdrücken. Die schweren Nebenwirkungen einer Therapie, die IL-6 blockiert, blieben aus. Nun hat das Kieler Forschungsteam das Medikament erstmals an einer kleinen Gruppe von Patientinnen und Patienten mit Colitis Ulcerosa oder Morbus Crohn getestet und untersucht, was genau das Medikament im menschlichen Körper bewirkt. „Der Wirkstoff tut beim Menschen mechanistisch wirklich genau das, was er soll. Der IL-6-Trans-Signalweg wird blockiert, die Entzündung dadurch gedämpft. Dieser Nachweis ist ein wichtiger Meilenstein in der Entwicklung des Medikaments von Labor bis in die Klinik“, so Schreiber.
„Bei wie vielen Patientinnen und Patienten das Medikament aber wie gut helfen wird und wie die Nebenwirkungen ausfallen, müssen umfassende klinische Studien an einer großen Anzahl von Patientinnen und Patienten zeigen“, betont Schreiber. Solch eine verblindete und Placebo-kontrollierte klinische Studie der Phase II zum Nachweis von Wirksamkeit und Verträglichkeit bei Patientinnen und Patienten mit Colitis ulcerosa haben Ferring und I-Mab Biopharma kürzlich durchgeführt. Mit Ergebnissen dieser bereits in Auswertung befindlichen Studie sei im Juli 2021 bei der Jahrestagung der „European Crohn‘s and Colitis Organisation“ (ECCO) zu rechnen.
Originalveröffentlichung
Stefan Schreiber*, Konrad Aden*, Joana P. Bernardes*, Claudio Conrad*, …Stefan Rose-John+, Georg H. Waetzig+, Philip Rosenstiel+: "Therapeutic IL-6 trans-signalling inhibition by olamkicept (sgp130Fc) in patients with active inflammatory bowel disease"; Gastroentereology; 2021; *shared first authorship. + shared last authorship