Proteinsequenz fördert Verzweigung von Nervenzellen
Molekül könnte bei der Entwicklung von Zellersatztherapien helfen
Anzeigen
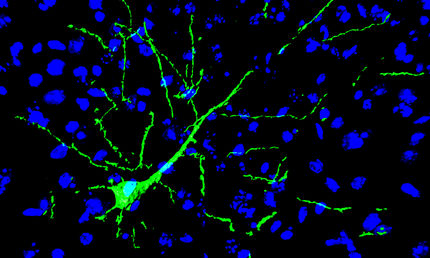
Eine kurze Sequenz des Proteins Tenascin-C kann Nervenzellen dazu anregen, neue Verzweigungen zu bilden. Das fanden Forscher der Ruhr-Universität Bochum und der Technischen Universität Dortmund heraus, die im Rahmen der Universitätsallianz Ruhr kooperieren. Sie beobachteten die Effekte, nachdem sie das Eiweißmolekül zu kultivierten Maus-Nervenzellen hinzugegeben hatten. Die Ergebnisse könnten dazu beitragen, Therapien für den Ersatz von Nervenzellen zu entwickeln.
Molekül aus dem Zellzwischenraum
„Das Gehirn ist besonders sensibel gegenüber Erkrankungen und Verletzungen“, sagt Marvin Jarocki vom Bochumer Lehrstuhl für Zellmorphologie und Molekulare Neurobiologie, den Prof. Dr. Andreas Faissner leitet. „Die regenerative Medizin bemüht sich daher um Zellersatztherapien.“
Eine Forschungsrichtung konzentriert sich auf künstliche Ergänzungsstoffe, sogenannte bioaktive Peptide. Bei ihnen handelt es sich um kurze Eiweißmoleküle, die gezielt Signalwege von Zellen und so deren Entwicklung beeinflussen können. Zusammen mit Substanzen, die die natürliche Zellumgebung imitieren, sollen sie die Regeneration geschädigter Hirnbereiche therapeutisch unterstützen. Ein solches bioaktives Peptid fanden die Forscher in dem Protein Tenascin-C, einem Strukturmolekül der extrazellulären Matrix, die den Zwischenraum zwischen den Zellen bildet.
In Zellkulturstudien getestet
Gemeinsam mit Prof. Dr. Ralf Weberskirch und Dr. Omar Sallouh von der Dortmunder Fakultät Chemie und Chemische Biologie reproduzierten die Bochumer Forscher das Peptid im Reagenzglas. Anschließend analysierte Marvin Jarocki seine Funktion in Zellkulturexperimenten mit embryonalen Maus-Nervenzellen. Durch Zugabe des Peptids vermehrte sich die Zahl der Verzweigungspunkte, der einzelnen Fortsätze und damit die Gesamtlänge der Fasern pro Nervenzelle, während die Wachstumsrate der Fasern unverändert blieb.
Das Team identifizierte auch einen möglichen Signalweg, der die verzweigungsfördernde Wirkung des Peptids erklären könnte. Die Forscher untersuchten, welche mRNA-Moleküle, also welche Protein-Baupläne, vermehrt in den Zellen vorkamen. Sie fanden eine erhöhte Menge von mRNA-Molekülen für bestimmte Rezeptoren der Zellmembran, nämlich Integrin, Alpha V und Integrin Beta 1. Diese standen mit erhöhten Werten bestimmter Signalmoleküle in der Zelle in Zusammenhang, welche wiederum einige verzweigungsfördernde Gene – FOXP2 und Cntn-3 genannt – regulieren.