Bakterien überdauern als blinde Passagiere
Wie Magen-Darmkeime ihr Infektionsprogramm von akut auf chronisch umschalten
Jedes Jahr lösen Bakterien der Gattung Yersinia mehrere Tausend Magen-Darminfektionen in Deutschland aus. In den meisten Fällen schafft es das menschliche Immunsystem, die Bakterien zu beseitigen. Doch bei einem Teil der Betroffenen stellt sich eine chronische Infektion ein, die langfristig die Ausbildung von Autoimmunerkrankungen fördern kann. Wissenschaftler des Helmholtz-Zentrums für Infektionsforschung (HZI) in Braunschweig haben nun aufgedeckt, mit welchem Trick sich die Yersinien vor dem Immunsystem verstecken: Sie drosseln die Produktion eines Giftstoffes, mit dem sie während einer akuten Infektion die Entzündung des befallenen Gewebes anheizen. So geht die Entzündung zurück und die Bakterien entziehen sich der Aufmerksamkeit des Immunsystems.
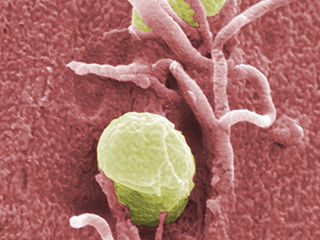
Bakterien der Art Yersinia pseudotuberculosis dringen in menschliches Gewebe ein.
© HZI / Manfred Rohde
Der bekannteste Vertreter unter den Yersinien ist der Erreger der Pest, Yersinia pestis, der durch Flohbisse übertragen werden kann. Andere Arten wie Yersinia enterocolitica und Yersinia pseudotuberculosis gelangen meist über verunreinigte Nahrungsmittel, zum Beispiel rohes Schweinefleisch, in den menschlichen Körper und können schwere Durchfallerkrankungen oder Erbrechen auslösen. Auf diesem Wege entledigt sich der Körper schon eines Großteils der Erreger, die übrige Aufräumarbeit leistet das Immunsystem. Allerdings kann eine Yersinien-Infektion auch chronisch werden und dann sogar Autoimmunerkrankungen wie reaktive Arthritis begünstigen. Wie die Bakterien aber über Jahre hinweg im Körper überdauern können, ohne vom Immunsystem aufgespürt zu werden, und wie sie dabei Immunreaktionen gegen körpereigenes Gewebe fördern, ist bislang nicht eindeutig geklärt.
In der akuten Infektionsphase produzieren einige Yersinien unter anderem einen Giftstoff, der als CNFY bezeichnet wird und den sie in die Zellen des Wirtes abgeben. Dort blockiert er die Zellteilung, was wiederum dazu führt, dass die Zellen immer größer werden und von den Yersinien leichter attackiert werden können. „Mithilfe von CNFY beschleunigen die Yersinien die Ausbreitung der Infektion und der Entzündung im Gewebe, bis die infizierten Zellen schließlich absterben“, sagt Prof. Petra Dersch, die am HZI die Abteilung „Molekulare Infektionsbiologie“ leitet.
Mäuse überstehen eine Yersinien-Infektion meist schnell und unbeschadet. Rund zehn Prozent der Fälle führen zum Tod, während etwa zehn Prozent chronisch werden. Petra Dersch und ihr Forscherteam am HZI haben die Mäuse mit chronischem Verlauf und die zugehörigen Yersinien mittels modernster Sequenziermethoden genau unter die Lupe genommen: Eine Transkriptomanalyse hat dabei entlarvt, welche Gene in den Bakterien und den Mäusen aktiv sind und welche nicht. „Wir haben herausgefunden, dass die Produktion von CNFY in den persistierenden, also den überdauernden Yersinien herunterreguliert ist“, sagt Dersch. „Ohne CNFY sieht das Immunsystem die Bakterien nicht mehr, die Entzündungsreaktion geht zurück und die Mäuse überleben. Mit diesem Trick konnten sich die Yersinien monatelang im Blinddarm der Mäuse verstecken.“
Gewebeanalysen am Mikroskop offenbarten ebenfalls einen Unterschied zwischen akut und chronisch infizierenden Yersinien: In akuten Infektionsphasen bilden die schnell wachsenden Bakterien Mikrokolonien, die für das Immunsystem auffälliger sind. Dagegen kommen die persistierenden Bakterien einzeln vor und sind so noch schwerer zu finden. In Zusammenarbeit mit Dr. Till Strowig, Leiter der HZI-Nachwuchsgruppe „Mikrobielle Immunregulation“, haben die Wissenschaftler außerdem nachgewiesen, dass Yersinien sogar die mikrobielle Gemeinschaft im Darm verändern. „Eine Yersinien-Infektion verschiebt die Zusammensetzung der Mikrobiota im Darm deutlich zugunsten entzündungsfördernder Bakterienarten“, sagt Dersch.
Ein Zusammenhang zwischen Yersinien-Infektionen und entzündlichen Autoimmunerkrankungen wie reaktiver Arthritis ist bereits lange bekannt, allerdings ist der Mechanismus dahinter noch immer ein Rätsel. „Unsere Transkriptomanalysen haben gezeigt, dass das Immunsystem der chronisch infizierten Mäuse dauerhaft sehr leicht aktiv ist“, sagt Petra Dersch. „In der Folge könnten Antikörper gegen körpereigenes Gewebe gebildet werden, denn die Oberflächenstrukturen der Zellen ähneln zum Teil denen der Bakterien. Das könnte auch das gehäufte Auftreten von Arthritis bei Yersinia-Patienten erklären.“