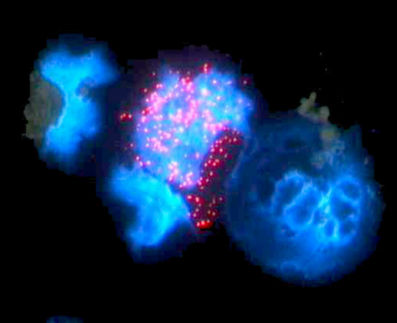
Zellen erobern den Raum: Wissenschaftler entwickeln elastische dreidimensionale Mikrostrukturen für die Zellkultur
Trotz ihrer Bedeutung für die biologische Forschung hat die klassische Zellkultur ihre Grenzen: Im Gewebe leben Zellen im räumlichen Verband, während sie in der Kulturschale nur in zwei Dimensionen wachsen können. Wissenschaftler am Karlsruher Institut für Technologie (KIT) haben jetzt ein Verfahren vorgestellt, mit dem sie beliebig strukturierte dreidimensionale und flexible Substrate herstellen können. Die Methode eröffnet neue Möglichkeiten für die Erforschung der Zellbewegung und -differenzierung.
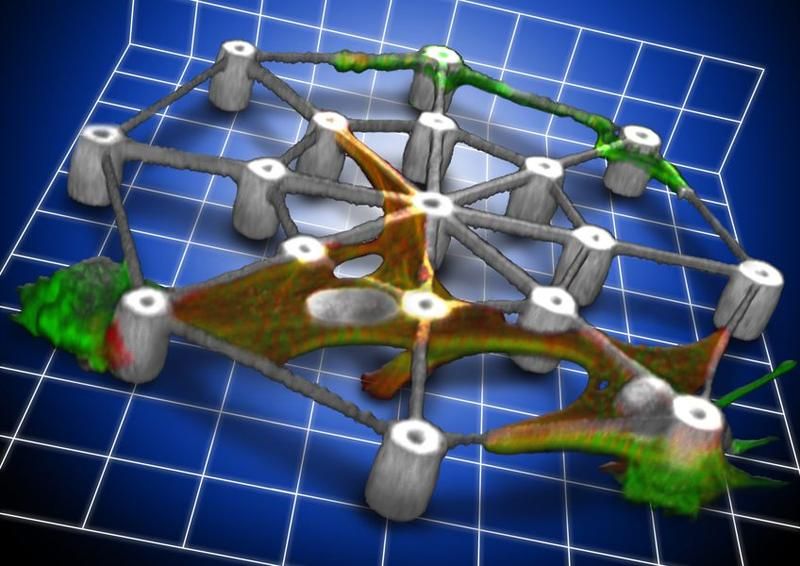
Zellen (rot und grün gefärbt) haften an den nur etwa ein Tausendstel Millimeter dicken Balken der elastischen Mikrostruktur.
M. Rill
Die Welt ist eine Scheibe - zumindest für Zellen auf dem Boden einer Petrischale. Außer in der obersten Zellschicht etwa auf der Haut oder im Darm leben Zellen im Organismus aber in einer dreidimensionalen und flexiblen Umgebung. „Sie treten auf ihrer gesamten Oberfläche in Kontakt mit Nachbarzellen und der extrazellulären Matrix, die dem Körpergewebe Festigkeit und Elastizität verleiht“, erläutert Professor Martin Bastmeyer vom DFG-Centrum für Funktionelle Nanostrukturen (CFN) des KIT. An deren Fasern, die aus unterschiedlichen Molekülen bestehen, können Zellen fest anhaften oder sich wie in einem dreidimensionalen Klettergerüst fortbewegen. Zusammensetzung und Struktur der Matrix beeinflussen Verhalten und Entwicklung der Zellen, die wiederum die Matrix auf- oder umbauen und verformen.
Dieses Wechselspiel untersucht Bastmeyer mit seinen neuen künstlichen Strukturen aus elastischen, langen Elementen mit einem Durchmesser von weniger als einem Tausendstel Millimeter. Für ihre Herstellung nutzt die Arbeitsgruppe ein als Direktes Laserschreiben (DLS) bezeichnetes Verfahren, das die Physiker Professor Martin Wegener und Dr. Georg von Freymann am CFN entwickelt haben. Dabei schreibt ein computergesteuerter, fokussierter Laserstrahl in einem Fotolack wie ein Stift in drei Dimensionen. Bei der Entwicklung bleiben die belichteten Bereiche stehen, die dann mit einem Protein beschichtet werden, an dem die Zellen anhaften können.
Auf diesen Strukturen ausgesäte Herzzellen aus Hühnerembryonen beginnen nach wenigen Tagen, sich rhythmisch zusammenzuziehen und die elastischen, dünnen Balken zu verbiegen. „Vergleichende Messungen mit dem Rasterkraftmikroskop zeigen, dass sie dabei eine Zugkraft von 47 Nanonewton entwickeln. Das würde ausreichen, um eine Masse von etwa fünf Millionstel Gramm zu bewegen“, erklärt die Biologin Dr. Franziska Klein. „Grob gerechnet könnte ein Würfel aus dicht gepackten Zellen mit einer Kantenlänge von fünf Zentimetern fast fünf Kilogramm anheben.“
Weiterführende Experimente mit anderen Strukturen sollen klären, wie Zellen auf unterschiedliche mechanische Eigenschaften und räumliche Gegebenheiten ihrer Umgebung reagieren. Hierfür will das Team aus Biologen und Physikern größere und komplexere Strukturen realisieren, in die Zellen wie in einen porösen Schwamm einwandern können. Die Ergebnisse könnten dabei helfen, Kulturbedingungen für die Gewebezucht und die Regenerative Medizin mit Stammzellen zu optimieren.
Originalveröffentlichung: Franziska Klein et al.; "Elastic Fully Three-dimensional Microstructure Scaffolds for Cell Force Measurements"; Advanced Materials 22, 868 (2010)
Meistgelesene News
Organisationen
Weitere News aus dem Ressort Forschung & Entwicklung

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.