Wasserstoff aus dem Reagenzglas: Forscher nutzen Wasserstofffabrik der Grünalge
Natürliches System ist sechsmal effektiver als andere chemische oder halb-artifizielle Verfahren
Wasserstoff gilt als Energieträger der Zukunft: Ohne Ausstoß von CO2 und Schadstoffen lässt sich daraus Strom gewinnen. Die umweltfreundliche Herstellung ausreichender Mengen Wasserstoffs beschäftigt daher die Forschung seit langem. Als mikroskopisch kleine Fabrik steht dabei die Grünalge Chlamydomonas reinhardtii im Mittelpunkt, die unter Stress Wasserstoff bilden kann. Bochumer Biologen ist es jetzt gelungen, die dafür verantwortlichen Bestandteile der Alge zu isolieren und die Produktion ins Reagenzglas zu verlegen. „Dieses natürliche System erzeugt sechsmal so viel Wasserstoff wie ein halb-artifizielles, über das amerikanische Kollegen erst kürzlich berichtet haben“, sagt Arbeitsgruppenleiter Prof. Dr. Thomas Happe. Darüber hinaus klärten die Forscher die Reaktion im Detail auf und ebneten so den Weg zur Optimierung der Wasserstoffausbeute.
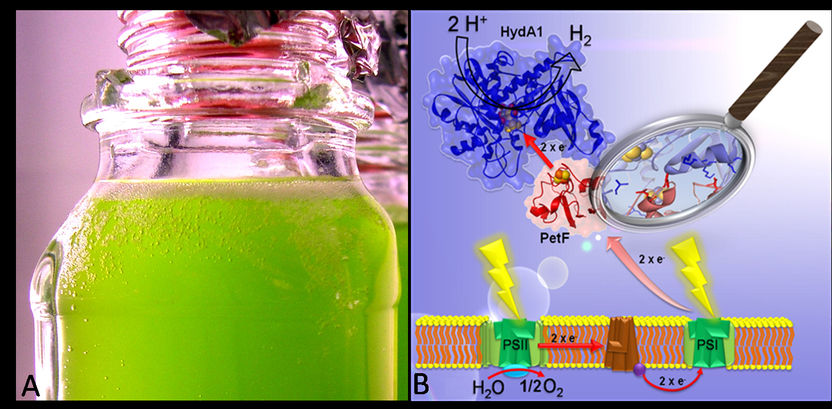
Links: Wasserstoffbildung in einer verschlossenen, unter Schwefel-Mangel kultivierten C. reinhardtii-Kultur. Rechts: Unter Nähstoffmangel fließen die in der Photosynthese angeregten Elektronen aus der Wasserspaltung in die H2-Bildung. Der entscheidende Schritt ist die Wechselwirkung zwischen Ferredoxin PetF und der [FeFe]-Hydrogenase HydA1. Sie setzt zwei nacheinander aufgenommene Elektronen mit H+-Ionen zu Wasserstoff um, der aus der Zelle entweicht.
Ruhr-Universität Bochum (RUB)
Notlösung für die Alge
Für die Grünalge ist die Wasserstoffproduktion eine Notlösung. Während sie die durch die Photosynthese gewonnene Energie unter normalen Bedingungen in Zellvermehrung und Wachstum investiert, fehlen ihr dafür bei Nährstoffmangel die Bausteine. Um die bei der Photosynthese aus Lichtenergie gewonnenen Elektronen trotzdem loszuwerden, setzt die Alge sie mit Hilfe eines speziellen Enzyms, der Hydrogenase, mit Protonen zu Wasserstoff um, den sie an ihre Umgebung abgibt. Schon lange experimentiert die Forschung mit Algenreaktoren, die auf diese Weise Wasserstoff herstellen. „Dieser langgehegte Traum der Forschung von der Erschließung der Solarenergie konnte bislang aber leider nur sehr ineffektiv umgesetzt werden“, erklärt Prof. Happe.
Drei Komponenten im Reagenzglas genügen
Der Bochumer Arbeitsgruppe um Prof. Happe ist es nun in Zusammenarbeit mit Kollegen der Universität Münster gelungen, den bislang nur unzureichend verstandenen grünalgenspezifischen Prozess der Wasserstoffbildung durch Kombination der Hydrogenase mit ausgewählten Proteinen der Photosynthesekette im Reagenzglas nachzubilden. Sie isolierten dafür getrennt voneinander die für die Lichtaufnahme erforderlichen Photosynthesekomplexe, das als Elektronenvermittler dienende Ferredoxin PetF und die wasserstoffproduzierende [FeFe]-Hydrogenase HydA1, die sie dann unter Belichtung vereinten. „Bereits nach wenigen Minuten ist eine deutlich lichtabhängige Wasserstoffbildung feststellbar, die nur einsetzt, wenn alle drei Komponenten enthalten sind“, so Prof. Happe.
Sechsmal mehr Wasserstoff als in halb-artifziellen Systemen
Die Wasserstoffbildung durch die natürlichen Komponenten im Reagenzglas zeigte sich dabei erstaunlich effektiv im Vergleich mit anderen Ansätzen. Erst kürzlich berichteten US-amerikanische Forscher aus Tennessee von der Etablierung eines semiartifiziellen Systems zur lichtgetriebenen Wasserstoffproduktion mit flächig aufgelagerten Photosynthesekomplexen und Platin-Nanopartikeln, welche die Katalysatorfunktion einer Hydrogenase ersetzen. Ihren Angaben zufolge liegt die Ausbeute, die mit einer großtechnischen Anlage unter optimalen Bedingungen gewonnen werden könnte, um eine Größenordnung über der Kraftstoffausbeute, die heute mit landwirtschaftlichen Mitteln in der Produktion von Biodiesel oder Bioethanol erzielt werden kann [Iwuchukwu et al.; 2009; Nature Nanotechnology]. „Die in dieser Studie erreichte Wasserstoffbildungsrate von hochgerechnet drei Litern pro Gramm Chlorophyll und Tag wird vom natürlichen System der Grünalgen bereits im Reagenzglas um das sechsfache übertroffen“, entgegnet Prof. Happe.
Wechselwirkung im Detail geklärt
Ferner gelang es der Bochumer Arbeitsgruppe, den genauen Kopplungsmechanismus von Photosynthese und Wasserstoff-bildendem Enzym experimentell auf molekularer Ebene aufzuklären. Von entscheidender Bedeutung scheinen dabei hochgradig spezifische Ladungswechselwirkungen zwischen den Proteinoberflächen von Ferredoxin und Hydrogenase zu sein. „Mit dem Verständnis dieser Protein-Protein-Wechselwirkung eröffnen sich nun verschiedene Möglichkeiten zur Optimierung der natürlichen Wechselwirkungseffizienz beider Proteine“, schätzt Prof. Happe. „Das könnte in Zukunft sowohl mit dem lebenden Organismus als auch mit enzymbasierten semiartifiziellen Systemen eine wirtschaftlich interessante und ökologisch vorbildliche Wasserstoff-Produktion ermöglichen.“
Originalveröffentlichung: Martin Winkler, Sebastian Kuhlgert, Michael Hippler and Thomas Happe; "Characterization of the Key Step for Light-driven Hydrogen Evolution in Green Algae"; JBC, Volume 284, Number 52, December 25, 2009