Spezialist aus den eigenen Reihen
Bauchspeicheldrüsenzellen lassen sich zur Insulin-Produktion anregen
Anzeigen
Gehen die Insulin produzierenden Zellen unseres Körpers zugrunde, kann sich daraus Diabetes entwickeln - eine der häufigsten Stoffwechselerkrankungen westlicher Industrienationen. Sie durch körpereigene, Insulin produzierende Zellen zu ersetzen, ist seit langem ein Traum der Diabetesforscher. Wissenschaftler am Max-Planck-Institut für Biophysikalische Chemie (Göttingen) sind diesem Ziel jetzt einen wichtigen Schritt näher gekommen. Schalteten die Forscher in zuckerkranken Mäusen ein einziges Gen in den Bauchspeicheldrüsenzellen an, verwandelten sich diese in Insulin produzierende Zellen. Ließe sich diese Umwandlung auch im Menschen gezielt regulieren, könnte dies zukünftig neue Therapiewege eröffnen, um Diabetes erfolgreich zu behandeln.
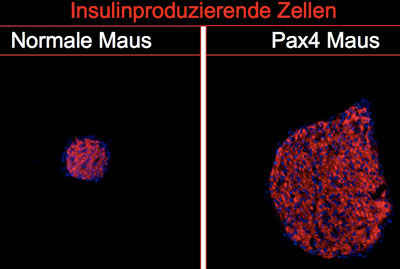
Die "Anschaltung" eines einzigen Faktors, Pax4, wandelt Vorläuferzellen der Bauchspeicheldrüse in funktionstüchtige, Insulin produzierende Zellen um. Dabei wächst die Anzahl dieser Insulin produzierenden Zellen mehrfach.
Collombat, Mansouri / MPIbpc
Damit sich der Zuckerstoffwechsel richtig einstellt, treten bereits während der Embryonalentwicklung wichtige Proteinfaktoren - die Transkriptionsfaktoren - in Aktion. Sie werfen gezielt genetische Programme an oder unterdrücken diese und verwandeln so Vorläuferzellen der Bauchspeicheldrüse in Zellen mit ganz bestimmten Eigenschaften. Ohne das Kontroll-Gen Pax4 entwickeln sich beispielsweise keine Insulin produzierenden Zellen. Andere Faktoren veranlassen Vorläuferzellen, Glukagon zu erzeugen. Damit die spezialisierten Zellen im richtigen Verhältnis entstehen, interagieren die Transkriptionsfaktoren miteinander in einem komplizierten "Räderwerk".
Göttinger Forscher um Ahmed Mansouri und Patrick Collombat konnten jetzt nachweisen, dass Pax4 in diesem komplexen Räderwerk der entscheidende "Schalter" ist, mit dem sich Vorläuferzellen der Bauchspeicheldrüse anregen lassen, Insulin zu produzieren. Schalteten die Göttinger Wissenschaftler in jungen zuckerkranken Mäusen gezielt das Pax4-Gen an, so hatten sich nach nur wenigen Tagen neue Insulin produzierende Zellen in der Bauchspeicheldrüse angesiedelt. "Wir waren völlig überrascht, dass es ausreichte, nur diesen einen Faktor in den Vorläuferzellen ‚anzuschalten’, nicht zwei oder gar mehr Faktoren", erklärt Ahmed Mansouri, Leiter der Forschungsgruppe "Molekulare Zelldifferenzierung".
Dass diese tatsächlich aus Vorläuferzellen in der Bauchspeicheldrüse abstammten konnten die Forscher mithilfe spezieller Untersuchungsmethoden nachweisen. Aber sind diese neuen Zellen ebenso funktionstüchtig wie normale Insulin produzierende Zellen? Wie die Wissenschaftler herausfanden, erzeugten die neuen Zellen in der Tat ausreichend Insulin, um in den kranken Mäusen den Blutzucker auf das Normalmaß zu senken. Auch die Lebensdauer der Mäuse ließ sich deutlich verlängern.
Aber aktives Pax4 stößt nicht nur in Vorläuferzellen die Produktion von Insulin an, wie die Ergebnisse der Göttinger Forscher zeigen. Auch ausgereifte Zellen, die bisher Glukagon herstellten, ließen sich durch aktives Pax4 reprogrammieren und in Insulin produzierende Zellen umwandeln. "Damit bestätigen wir erstmals experimentell, was viele Ergebnisse anderer Wissenschaftler bereits vermuten lassen: Die Bauchspeicheldrüse ist viel flexibler als bisher angenommen. Ihre Entwicklung ist auch im erwachsenen Körper noch nicht abgeschlossen", sagt Patrick Collombat. Folglich besteht Hoffnung, dass Diabetikern eines Tages durch eine Aktivierung des Pax4-Gens geholfen werden könnte. Aus den Vorläuferzellen, die jede Bauchspeicheldrüse bereithält, sollten sich auf diese Weise Zellen regenerieren lassen, die ausreichend Insulin erzeugen und abgestorbene Zellen ersetzen könnten.
Originalveröffentlichung: Patrick Collombat, Xiaobo Xu, Philippe Ravassard, Beatriz Sosa-Pineda, Sébastian Dussaud, Nils Billestrup, Ole D. Madsen, Palle Serup, Harry Heimberg, and Ahmed Mansouri; "The Ectopic Expression of Pax4 in the Mouse Pancreas Converts Progenitor Cells into alpha and subsequently ß Cells"; Cell (2009).