Grippeimpfstoffe ganz ohne Hühnereier
Zwei neue Designer-Zelllinien eignen sich dazu, Vakzine gegen Influenza herzustellen
Bislang werden Grippeimpfstoffe primär aus bebrüteten Hühnereiern gewonnen. Max-Planck-Wissenschaftler haben jetzt Wachstum, Stoffwechsel und Virusvermehrung zweier neuer Designer-Zelllinien untersucht und deren Eignung als Wirtszellen für die Herstellung von Impfstoffen in Bioreaktoren getestet. Die Vogelzelllinien AGE1.CR und AGE1.CR.pIX wurden von der Firma ProBioGen AG (Berlin) in Kooperation mit IDT Biologika GMBH (Dessau-Tornau) entwickelt. Offenbar eignen sich diese Zellen sehr gut, um Impfstoffe gegen ein breites Spektrum von Viren zu entwickeln. Das Ziel der Wissenschaftler ist es, den Weg für eine optimierte Produktion von Grippeimpfstoffen in Zellkulturen zu bahnen.
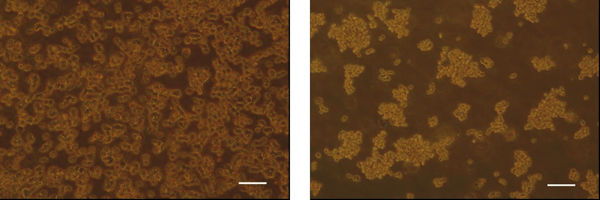
Lichtmikroskopische Aufnahmen von AGE1.CR (links) und AGE1.CRpIX Zellen (rechts). Die Aufnahmen stammen aus 24 Stunden alten T-Flaschen-Kulturen. Die CR Zellen zeigten nach der gleichen Kultivierungsdauer höhere Zellkonzentrationen und einen geringeren Aggregationsgrad in der unbewegten Kultur als CR.pIX Zellen. Der Balken gibt eine Länge von 100 µm an.
MPI für Dynamik komplexer technischer Systeme Magdeburg / Verena Lohr
Impfstoffe in ausreichender Menge zu produzieren, stellt eine der größten Herausforderungen der Biotechnologie dar - gerade auch angesichts drohender Pandemien der Schweine- und Vogelgrippe. Neben einer schnellen Diagnostik und der raschen Isolierung von Impfstämmen ist es vor allem entscheidend, tierische und humane Zelllinien zu kultivieren, die sich zur Herstellung von viralen Tot- und Lebendimpfstoffen eignen.
Die Mehrzahl aller zugelassenen Impfstoffe gegen Influenza wird gegenwärtig in Hühnereiern hergestellt. Im Fall einer Pandemie, so befürchten Experten, könnten allerdings die Impfstoffe weder in den benötigten Mengen noch schnell genug zur Verfügung stehen. Zudem besteht das Risiko allergischer Reaktionen auf Hühnereiweiß. Dies stellt die Forschung vor die Aufgabe, die Produktion von Impfstoffen auf Wirtszellen umzustellen, in denen sich das Virus ebenso gut vermehren lässt.
Die Fachgruppe Bioprozesstechnik am Max-Planck-Institut für Dynamik komplexer technischer Systeme in Magdeburg verfügt bereits seit vielen Jahren über das Know-how, Säugerzellen zur Impfstoffgewinnung zu kultivieren. Nun haben die Magdeburger Wissenschaftler anhand zweier Virentypen überprüft, ob sich neue Enten-Zelllinien als Wirtszellen für die Grippeimpfstoffherstellung eignen. Dabei arbeiteten sie eng mit der ProBioGen AG zusammen, ein auf Säugerzell-Engineering und Zellkulturen spezialisiertes Unternehmen.
Zwei Zelllinien im Vergleich
Gegenwärtig werden als Alternative zu bebrüteten Hühnereiern MDCK-Zellen aus Hunden (Madin Darby Canine Kidney Cells), Verozellen aus der Meerkatze und PER.C6-Zellen aus humanen Zellen genutzt, um neue Verfahren zur Produktion von Grippeimpfstoffen zu etablieren.
Die Zellen der neu entwickelten Linie (AGE1.CR) wurden aus Vorläuferzellen der Netzhaut (Retinoblasten) von Embryonen der Moschusente gewonnen. Diese bieten für die biopharmazeutische Anwendung den Vorteil, dass sie im Gegensatz zu Hühnerzellen nur wenige virale Elemente im Erbgut tragen. Damit wird das Risiko von unvorhergesehenen Veränderungen in der Zelle während der Produktion minimiert. Darüber hinaus wurde ihre Herkunft eindeutig dokumentiert, als sicher eingestuft und sämtliche bisherigen Arbeitsschritte und Passagen dokumentiert. Die Entenzellen sprechen außerdem auf mehrere Viren an, wie z. B. Influenza-Viren, stark abgeschwächte, modifizierte Pockenviren (MVA-Viren) sowie Tollwut- oder Herpesviren.
Die neuen Zellen wachsen in Suspension. Sie benötigen kein Serum, das teuer ist und zudem zu unerwünschten Kontaminationen mit Fremderregern führen kann. Darüber hinaus lässt die meist unterschiedliche Qualität einzelner Chargen die Prozessausbeuten oft erheblich schwanken. Im Gegensatz dazu sind Verfahren, die in definiertem serum-freiem Medium stattfinden, besser reproduzierbar. Da die genaue Zusammensetzung solcher Medien gezielt verändert werden kann, eignen sich diese besonders gut zu Studien, die Einflussgrößen auf Zellwachstum und Virusvermehrung untersuchen und die Prozesse durch mathematische Modelle beschreiben.
Der Zelllinie AGE1.CR wurde ein zusätzliches Gen mit auf den Weg gegeben, das die Virusausbeute steigern soll. "Wir konnten also zwei Zelllinien vergleichen - die ursprüngliche und die modifizierte (AGE1.CR.pIX). Wir haben untersucht, unter welchen Bedingungen sich Zellen und Viren optimal vermehren und welche Prozessparameter für die Impfstoffherstellung entscheidend sind", sagt Udo Reichl, Direktor am Max-Planck-Institut Magdeburg und Leiter der Fachgruppe Bioprozesstechnik.
Verhaltenstest für Zellen
Die neuen Zelllinien wurden von der Magdeburger Forschergruppe zunächst unter verschiedenen Bedingungen kultiviert, um das Wachstum und den Stoffwechsel der Zellen zu untersuchen. Primäres Ziel war dabei zunächst, möglichst hohe Zellkonzentrationen zu erreichen, da mehr Wirtszellen auch höhere Virusausbeuten erwarten lassen.
Mit beiden Zelllinien konnten hohe Zelldichten von bis zu fünf bis acht Millionen Zellen pro Milliliter erreicht werden, wobei sich der Einsatz von Schüttelkolben und Bioreaktoren als am vorteilhaftesten erwies. "Im Vergleich der eingesetzten Kultivierungssysteme konnten wir deutliche Unterschiede im Stoffwechsel feststellen", sagt Udo Reichl. Die Forscher haben im Vergleich beider Zelllinien zudem beobachtet, dass die AGE1.CR.pIX Zellen langsamer wachsen als ihre Doppelgänger ohne Gen. Anscheinend sind der Stoffwechsel und damit das Zellwachstum durch dieses Gen verändert.
Anwendung in der Produktion denkbar
Die Vogel-Designerzellen zeigten für Influenzaviren eine ebenso gute Produktivität wie MDCK- und Vero-Zellen, den bisher gängigen Produktionszelllinien für Humanimpfstoffe. Die Virusausbeuten machen zudem eine Großproduktion von Grippeimpfstoffen in serum-freien Medien möglich. "Die AGE1.CR Zellen können sich als industriefreundliche Zelllinie etablieren", ist Udo Reichl überzeugt.
Originalveröffentlichung: Verena Lohr et al.; "New avian suspension cell lines provide production of influenza virus and MVA in serum-free media: Studies on growth, metabolism and virus propagation"; Vaccine, Volume 27, Issue 36, 6. August 2009, Pages 4975-4982
Diese Produkte könnten Sie interessieren
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Diagnostik
Die Diagnostik ist das Herzstück der modernen Medizin und bildet in der Biotech- und Pharmabranche eine entscheidende Schnittstelle zwischen Forschung und Patientenversorgung. Sie ermöglicht nicht nur die frühzeitige Erkennung und Überwachung von Krankheiten, sondern spielt auch eine zentrale Rolle bei der individualisierten Medizin, indem sie gezielte Therapien basierend auf der genetischen und molekularen Signatur eines Individuums ermöglicht.

Themenwelt Diagnostik
Die Diagnostik ist das Herzstück der modernen Medizin und bildet in der Biotech- und Pharmabranche eine entscheidende Schnittstelle zwischen Forschung und Patientenversorgung. Sie ermöglicht nicht nur die frühzeitige Erkennung und Überwachung von Krankheiten, sondern spielt auch eine zentrale Rolle bei der individualisierten Medizin, indem sie gezielte Therapien basierend auf der genetischen und molekularen Signatur eines Individuums ermöglicht.