Messa a punto delle forbici genetiche
Scoperto un nuovo meccanismo della proteina anti-CRISPR per il controllo mirato delle tecnologie CRISPR
Le forbici geniche CRISPR-Cas offrono un'ampia gamma di potenziali applicazioni, dal trattamento delle malattie genetiche alle terapie antivirali e alla diagnostica. Per garantire la sicurezza di queste applicazioni, gli scienziati stanno studiando dei bloccanti in grado di controllare o impedire l'attività delle forbici geniche. Un inibitore promettente è la proteina anti-CRISPR AcrVIB1, ma il suo meccanismo d'azione era finora sconosciuto. Un gruppo di ricercatori dell'Istituto Helmholtz per la ricerca sulle infezioni basate sull'RNA (HIRI) di Würzburg, in collaborazione con il Centro Helmholtz per la ricerca sulle infezioni (HZI) di Braunschweig, ha decifrato l'esatta modalità di azione di AcrVIB1. Questo amplia i modi noti in cui gli Acr possono disattivare CRISPR. I risultati sono stati pubblicati sulla rivista scientifica Molecular Cell.
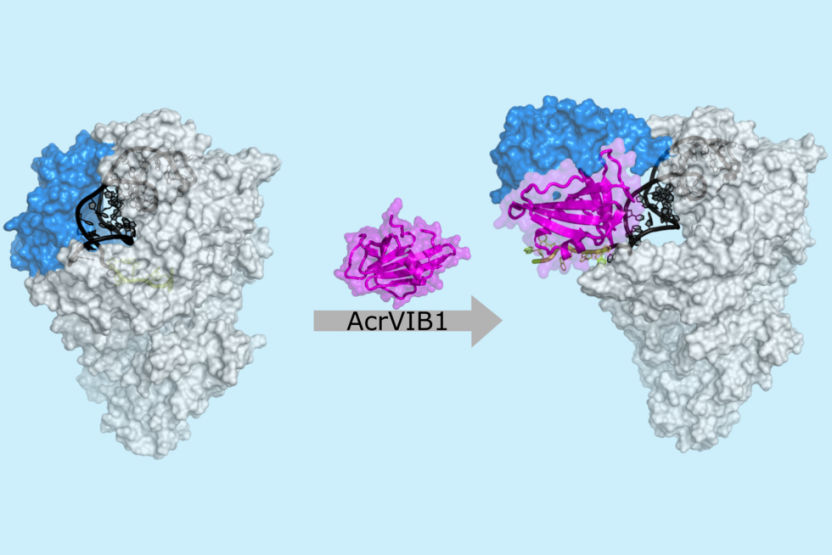
Micrografia crioelettronica: la proteina anti-CRISPR AcrVIB1 (magenta) si lega alla nucleasi Cas13b (grigio chiaro) e rafforza così il suo legame con l'RNA CRISPR (crRNA; grigio scuro e verde). AcrVIB1 causa un riarrangiamento strutturale della nucleasi (blu) e quindi rilascia l'RNA CRISPR, permettendone la scissione e la successiva degradazione.
© HZI / Stefan Schmelz
C'è sempre stata una corsa agli armamenti evolutiva tra i batteri e i loro virus, i cosiddetti fagi. Per proteggersi dagli attacchi dei fagi, i batteri hanno sviluppato sofisticati meccanismi di difesa con cui possono riconoscere i virus invasori e renderli innocui. Allo stesso tempo, i fagi hanno trovato strategie ingegnose per aggirare queste difese. Un esempio lampante di questa costante battaglia sono i sistemi di difesa CRISPR-Cas dei batteri e le proteine anti-CRISPR (Acrs) dei fagi, che possono bloccare specificamente queste "forbici genetiche" batteriche.
Oltre alla loro funzione di difesa, le proteine anti-CRISPR consentono un controllo più preciso delle tecnologie CRISPR. Tuttavia, per sfruttare appieno il loro potenziale, è importante comprenderne i meccanismi di base. I ricercatori dell'Istituto Helmholtz per la ricerca sulle infezioni basate sull'RNA (HIRI), un sito del Centro Helmholtz per la ricerca sulle infezioni (HZI) di Braunschweig, in collaborazione con la Julius-Maximilians-Universität di Würzburg (JMU), insieme agli scienziati dell'HZI, hanno ulteriormente chiarito la funzione di una proteina anti-CRISPR importante ma precedentemente non caratterizzata.
"In uno studio precedente, abbiamo utilizzato un algoritmo di apprendimento profondo per individuare nuovi Acr. Il risultato è stata la scoperta della prima proteina anti-CRISPR che ha come bersaglio la nucleasi Cas13b: AcrVIB1", afferma il capo del dipartimento di ricerca dell'HIRI, Prof. Chase Beisel, che ha condotto lo studio insieme al dipartimento del Prof. Wulf Blankenfeldt presso l'HZI. "La nucleasi Cas13b è in grado di riconoscere e tagliare l'RNA. Attualmente viene utilizzata per disattivare i geni, per studiarne la funzione, eliminare i virus o combattere le malattie genetiche". Il modo in cui la proteina AcrVIB1 inibisce la Cas13b è rimasto sconosciuto, fino ad ora. In uno studio pubblicato oggi sulla rivista Molecular Cell, il team di ricerca presenta questo meccanismo di blocco completamente nuovo.
Un vicolo cieco dell'RNA
La nucleasi Cas13b interagisce con un acido ribonucleico CRISPR (crRNA), che funge da molecola guida per riconoscere sequenze di RNA complementari, come quelle dei fagi. Non appena l'RNA bersaglio viene legato, Cas13b è in grado di tagliare non solo queste molecole di RNA complementari, ma anche tutti gli altri RNA nelle vicinanze, portandoli alla degradazione. Mentre la maggior parte delle proteine anti-CRISPR conosciute bloccano singole fasi di questo processo, come il legame del crRNA o il riconoscimento del bersaglio, AcrVIB1 utilizza un approccio diverso: la proteina non impedisce la connessione tra crRNA e nucleasi, ma la rafforza. Tuttavia, la coppia risultante è disfunzionale, quindi l'enzima non può iniziare a degradare gli RNA bersaglio anche se sono presenti. Inoltre, il crRNA legato diventa suscettibile all'attacco delle ribonucleasi cellulari, enzimi che degradano le molecole di RNA.
"Il legame più stretto tra la nucleasi e l'RNA guida era del tutto inaspettato. Un meccanismo più semplice e quindi inizialmente atteso sarebbe stato quello di impedire l'accoppiamento dell'RNA guida fin dall'inizio", spiega i risultati la prima autrice, la dottoressa Katharina Wandera, che ha conseguito il dottorato nel laboratorio di Chase Beisel. "Tuttavia, il percorso intrapreso da AcrVIB1 sembra essere più efficace: AcrVIB1 si lega strettamente a Cas13b e quindi inattiva la nucleasi. Allo stesso tempo, accelera la degradazione degli RNA guida, in modo che Cas13b diventi una sorta di 'vicolo cieco' per i crRNA".
Il team di Chase Beisel dell'HIRI e il laboratorio di Wulf Blankenfeldt dell'HZI hanno unito le forze per decifrare con maggiore precisione la struttura del meccanismo inibitorio. Utilizzando immagini ad alta risoluzione al microscopio crioelettronico, il gruppo di Blankenfeldt ha dimostrato che AcrVIB1 si lega a Cas13b mentre la regione di legame del crRNA rimane libera. "La nostra scoperta fornisce un modello per lo sviluppo di molecole che potrebbero imitare o modificare la funzione della proteina anti-CRISPR", afferma Blankenfeldt. Questi sono i primi dati pubblicati dal nuovo impianto di microscopia crioelettronica dell'HZI.
Un campo ampio
"In futuro, potremmo utilizzare molecole come AcrVIB1 per regolare o disattivare temporaneamente i sistemi CRISPR in varie applicazioni", afferma Blankenfeldt. Questa scoperta offre quindi un potenziale per migliorare ulteriormente la sicurezza e la precisione delle tecnologie basate su CRISPR.
"La decifrazione di questo meccanismo fornisce anche preziose indicazioni sulla coevoluzione di batteri e virus, che sono in costante corsa per superarsi a vicenda", spiega Wandera. Queste conoscenze potrebbero aiutare a comprendere meglio i meccanismi di resistenza batterica e quindi a guidare lo sviluppo di nuovi antibiotici e applicazioni nella biologia sintetica".
In sintesi, questo studio non solo contribuisce a una migliore comprensione delle strategie anti-CRISPR, ma apre anche la strada a terapie e procedure diagnostiche innovative in medicina. "Ma questo è solo l'inizio: ci sono sicuramente molti altri Acrs e nuovi meccanismi inibitori che aspettano di essere scoperti", dice Beisel, dando una prospettiva sui progetti di ricerca futuri.
Nota: questo articolo è stato tradotto utilizzando un sistema informatico senza intervento umano. LUMITOS offre queste traduzioni automatiche per presentare una gamma più ampia di notizie attuali. Poiché questo articolo è stato tradotto con traduzione automatica, è possibile che contenga errori di vocabolario, sintassi o grammatica. L'articolo originale in Tedesco può essere trovato qui.