Las células leucémicas activan el programa de reciclaje celular
Los hallazgos abren nuevas opciones terapéuticas para el futuro
Anuncios
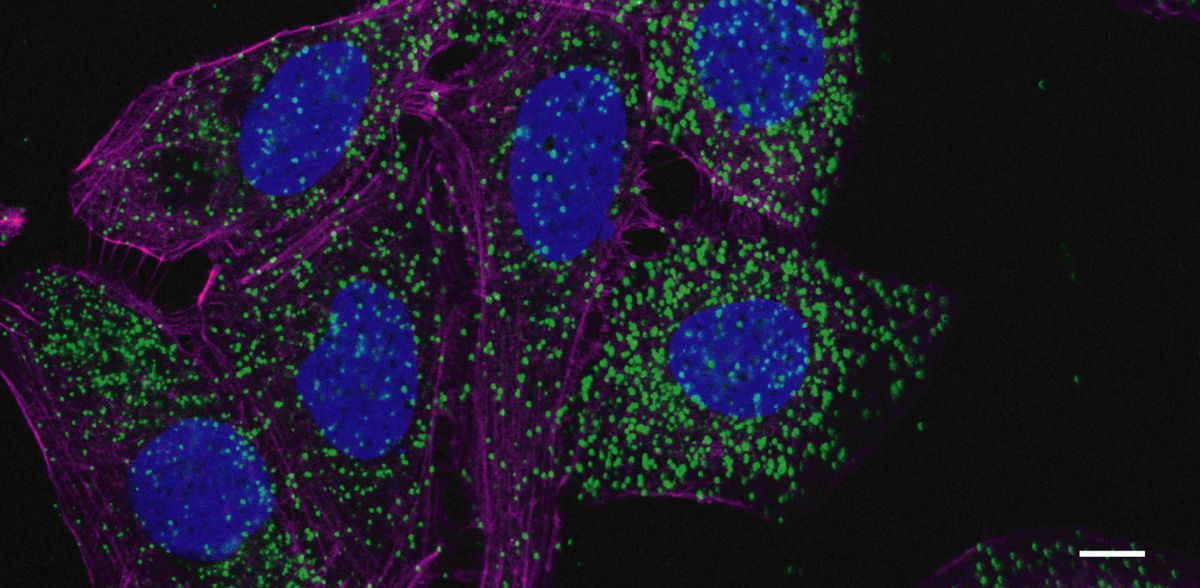
Para acelerar su crecimiento, las células leucémicas suelen activar el reciclaje de estructuras celulares, lo que les permite deshacerse de componentes defectuosos y abastecerse mejor de materiales de construcción. Investigadores de la Universidad Goethe de Fráncfort han demostrado ahora que las células leucémicas con una mutación muy común activan genes específicos que son importantes para este proceso de reciclaje. Sus hallazgos, publicados en la revista Cell Reports, abren nuevas opciones terapéuticas para el futuro.
En un estudio reciente, científicos dirigidos por el profesor Stefan Müller, del Instituto de Bioquímica II de la Universidad Goethe, investigaron una forma específica de cáncer de la sangre conocida como leucemia mieloide aguda o LMA. Esta enfermedad se presenta principalmente en la edad adulta y suele acabar siendo mortal para los pacientes mayores. En aproximadamente un tercio de los pacientes con LMA, el material genético de las células cancerosas presenta una mutación característica que afecta al llamado gen NPM1, que contiene las instrucciones de construcción de una proteína del mismo nombre.
Aunque ya se sabía que la variante mutada de NPM1 (abreviada como NPM1c) es un factor importante en el desarrollo de la leucemia, "junto con un equipo interdisciplinar formado por varios grupos de investigación de la Universidad Goethe, hemos descubierto ahora una nueva forma en que la variante del gen NPM1c lo consigue", explica Müller. Según esto, la proteína alterada interviene en la autofagia, un importante proceso celular que consiste en una vía metabólica a través de la cual la célula recicla sus propias estructuras. Por un lado, esta "autodigestión" sirve para eliminar moléculas defectuosas. "Por otro, también permite a la célula satisfacer su necesidad de componentes básicos importantes, incluso en caso de deficiencia de nutrientes o de aumento de la proliferación celular, característico de las células cancerosas", explica la estudiante de doctorado Hannah Mende, primera autora del estudio.
Durante la autofagia, la célula produce inicialmente una especie de bolsa de residuos, el autofagosoma, en la que empaqueta los componentes celulares que van a ser descompuestos y reciclados en caso necesario. A continuación, esta bolsa de residuos se transporta al centro de reciclaje de la célula, el llamado lisosoma, donde su contenido se descompone con la ayuda de ácidos y enzimas. Desde aquí, los componentes básicos se liberan en la célula, donde pueden reutilizarse. "Ahora hemos podido demostrar que NPM1c promueve la producción tanto de autofagosomas como de lisosomas", afirma Müller.
Los investigadores también han dado respuesta a la pregunta de cómo NPM1c produce estos efectos: Se une a un regulador central del sistema autofagosoma-lisosoma llamado GABARAP, y por tanto lo activa. "Mediante simulaciones por ordenador, hemos demostrado que esta unión de NPM1c y GABARAP tiene una estructura atípica", explica el Dr. Ramachandra M. Bhaskara, coautor del estudio y jefe del grupo de trabajo de biología celular computacional del Instituto de Bioquímica II. Los datos experimentales de biología estructural confirman los resultados de la simulación, en base a los cuales ahora puede ser posible desarrollar sustancias activas que influyan específicamente en la unión de NPM1c a GABARAP y combatan así el crecimiento de las células leucémicas.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Hannah Mende, Anshu Khatri, Carolin Lange, Sergio Alejandro Poveda-Cuevas, Georg Tascher, Adriana Covarrubias-Pinto, Frank Löhr, Sebastian E. Koschade, Ivan Dikic, Christian Münch, Anja Bremm, Lorenzo Brunetti, Christian H. Brandts, Hannah Uckelmann, Volker Dötsch, Vladimir V. Rogov, Ramachandra M. Bhaskara, Stefan Müller; "An atypical GABARAP binding module drives the pro-autophagic potential of the AML-associated NPM1c variant"; Cell Reports, Volume 42