¿Cómo combatir mejor el cáncer de sangre?
Varios centenares de combinaciones de tratamientos diferentes para probar simultáneamente fuera del organismo
Anuncios
A pesar de disponer de tratamientos aprobados, el mieloma múltiple sigue siendo incurable. Pero investigadores de la ETH de Zúrich y del Hospital Universitario de Zúrich se propusieron mejorar los resultados del tratamiento probando cientos de terapias existentes fuera del organismo para predecir su eficacia.
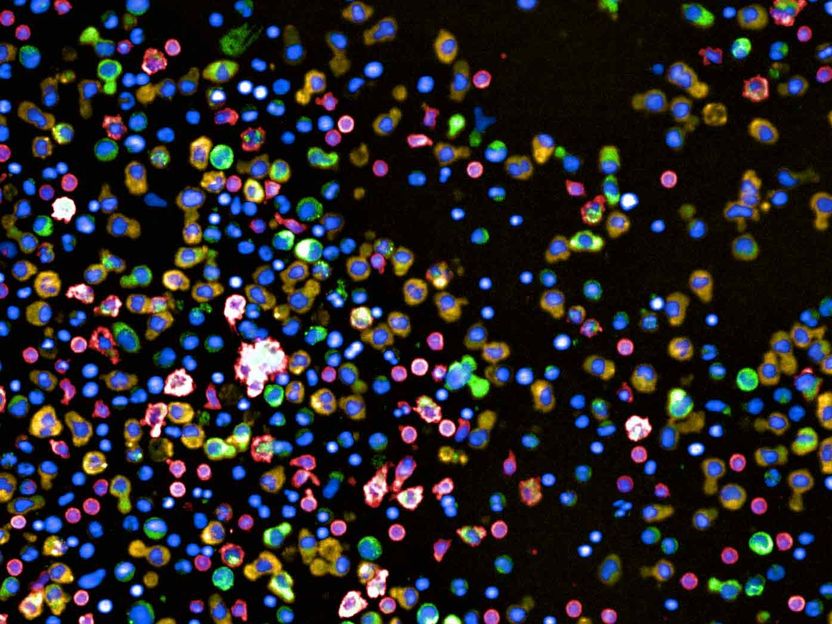
Células de la médula ósea de un paciente con mieloma múltiple. Las células rojas son monocitos sanos, las verdes y amarillas son células plasmáticas.
Berend Snijder Lab / ETH Zürich
El mieloma múltiple es un raro cáncer de la sangre causado por la multiplicación incontrolada de células plasmáticas anormales. Estas células plasmáticas son un tipo especial de glóbulos blancos que desempeñan un papel importante en el sistema inmunitario al producir anticuerpos esenciales en la médula ósea y los ganglios linfáticos.
A pesar de que cada vez se dispone de más fármacos aprobados y enfoques terapéuticos como la inmunoterapia, la enfermedad aún no tiene cura. La esperanza de vida media de los pacientes tras el diagnóstico es de sólo cinco años.
Uno de los principales problemas es la tendencia del cáncer a reaparecer incluso después del tratamiento. Esto se debe a que el tratamiento hace que las células cancerosas sean más resistentes a los fármacos utilizados, hasta que finalmente, tras varias rondas de tratamiento, no queda ninguna opción eficaz.
Para hacer frente a este problema, los investigadores de la ETH han adaptado su plataforma de cribado para buscar salidas a este problema y ofrecer así nuevas esperanzas de obtener resultados más satisfactorios en el tratamiento.
Biopsias al microscopio
Los investigadores utilizan un método de cribado de alto rendimiento denominado farmacoscopia, desarrollado por el profesor Berend Snijder, para comprobar la eficacia de diversos tratamientos en las células cancerosas del paciente.
Este método de vanguardia permite probar simultáneamente varios centenares de combinaciones de tratamientos diferentes fuera del organismo. Analizando las reacciones de las células a cada tratamiento, pueden determinar qué método es el más prometedor para cada paciente.
Para ello, las células de las biopsias se colocan en placas especiales con 384 pequeños pocillos, cada uno de los cuales contiene una combinación distinta de posibles sustancias de tratamiento. Al cabo de 24 horas, las células se tiñen con diferentes anticuerpos y sus reacciones se evalúan mediante imágenes generadas por microscopía automatizada. A continuación, se utiliza un algoritmo de aprendizaje profundo para identificar y clasificar los tipos de células. El proceso está automatizado en gran medida, lo que permite un análisis eficiente y preciso de los resultados.
138 biopsias analizadas individualmente
Los investigadores utilizaron la farmacoscopia para examinar de cerca 138 biopsias de médula ósea de 89 pacientes con mieloma múltiple en diferentes estadios, incluidos pacientes recién diagnosticados y no tratados, así como pacientes que se sometieron a múltiples rondas de tratamiento.
El objetivo era observar en cada biopsia el comportamiento de las células cancerosas en respuesta a diversos fármacos y combinaciones de fármacos aprobados. En función del aspecto de las células, los investigadores podían determinar la mejor opción de tratamiento para cada paciente.
Aunque el laboratorio Snijder ya había utilizado la farmacoscopia en estudios similares sobre otros tipos de cáncer de la sangre, como linfomas y leucemias, hubo que adaptar la plataforma para este estudio del mieloma.
Esperanza de tratamientos más eficaces
El trabajo pionero realizado por los investigadores de la ETH y del Hospital Universitario de Zúrich ofrece esperanzas de tratamientos más eficaces para el mieloma múltiple. Mediante el uso de la Farmacoscopia para probar cientos de tratamientos, los investigadores pudieron identificar nuevas opciones terapéuticas más eficaces para cada paciente.
Este nuevo enfoque de medicina personalizada es transferible a la clínica y puede así ayudar a los médicos a encontrar la mejor opción para sus pacientes en una fase temprana. "Sin embargo, primero tendremos que validar el método en ensayos clínicos", afirma Snijder.
Ahora, el laboratorio Snijder quiere seguir desarrollando la plataforma para ampliar su uso a los tumores sólidos. A diferencia de los cánceres sanguíneos, los tumores sólidos deben disociarse hasta cierto punto antes de poder analizarse en el formato de placa de 384 pocillos. Actualmente están adaptando la plataforma de cribado para tumores cerebrales, entre otros.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.