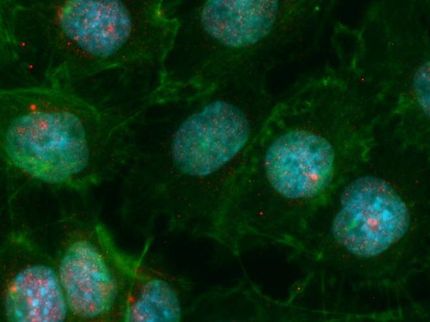
Guardianes del ADN fuera de control
Nuestro propio sistema inmunitario puede convertirse en el enemigo cuando los mecanismos que son realmente protectores se descontrolan
En la vasculitis asociada a ANCA, las reacciones inflamatorias excesivas provocan hemorragias pulmonares que pueden ser mortales si no se tratan. Investigadores de la Universidad de Bonn, junto con colegas de Alemania, Países Bajos, Suiza e Inglaterra, han descifrado un mecanismo en ratones y pacientes que conduce a esta grave enfermedad. Los resultados se publican ahora en la revista Journal of Experimental Medicine.
Imagen simbólica
pixabay.com
En la vasculitis asociada a ANCA se produce una grave inflamación de los vasos sanguíneos pequeños y medianos de los pulmones. Además, también pueden verse afectados la piel y los riñones. ANCA son las siglas de "anticuerpos citoplasmáticos antineutrófilos", que son anticuerpos producidos por el organismo que se dirigen a sus propios glóbulos blancos. Se trata de una enfermedad autoinmune grave y poco frecuente que suele ser mortal si no se trata debido a la hemorragia pulmonar.
La terapia consiste en la administración de fármacos que suprimen el sistema inmunitario. Recientemente, también se ha intentado bloquear la cascada inflamatoria con inhibidores. "El reto de encontrar nuevas terapias es que se sabe muy poco sobre los mecanismos que desencadenan la enfermedad", afirma el profesor Natalio Garbi, del Instituto de Medicina Molecular e Inmunología Experimental (IMMEI) del Hospital Universitario de Bonn.
Junto con colegas de Alemania, Países Bajos, Suiza y Reino Unido, los científicos han descubierto ahora un mecanismo responsable del desarrollo de la enfermedad en forma de la vía de señalización cGAS/STING/IFN-I. "Hemos podido demostrar en experimentos con ratones que los síntomas de esta enfermedad autoinmune -como la hemorragia pulmonar- mejoran cuando se bloquea esta vía de señalización con fármacos", afirma la primera autora y estudiante de doctorado Nina Kessler, del equipo de Natalio Garbi. En el estudio participaron 31 pacientes con vasculitis ANCA y, como controles, 57 individuos sanos, así como un nuevo modelo de ratón.
ADN extraviado
Normalmente, el material genético ADN se encuentra en el núcleo o las mitocondrias de las células. Pero si patógenos como bacterias o virus se han instalado en la célula, pueden dejar un rastro de ADN en el citosol que es detectado por un sensor especial llamado cGAS. Este centinela produce una molécula llamada cGAMP, que a su vez activa la molécula STING. Como resultado, se produce la producción de interferón de tipo 1 (IFN-I), lo que provoca una fuerte inflamación. Esto debería impedir la multiplicación de los patógenos e incluso llevar a las células muy infectadas al suicidio celular.
"Se vuelve problemático cuando estos mecanismos no son desencadenados por los patógenos, sino por nuestro propio ADN celular", explica Garbi. Entonces la vía de señalización cGAS/STING/IFN-I conduce a la muerte celular. "En nuestro estudio, demostramos que, por razones aún desconocidas, el ADN se libera del núcleo celular y activa la vía de señalización. Esto conduce a la destrucción de los vasos sanguíneos y a una hemorragia franca", afirma Garbi, miembro del grupo de excelencia ImmunoSensation2 de la Universidad de Bonn.
Los investigadores recrean el desarrollo de la enfermedad en ratones
Los investigadores recrearon los pasos más importantes del desarrollo de la enfermedad en ratones. Para ello, administraron autoanticuerpos patógenos a los animales e introdujeron productos bacterianos en sus pulmones para imitar una infección como la que se produce durante un brote de vasculitis ANCA. Los ratones desarrollaron entonces una enfermedad pulmonar y una hemorragia. En varios puntos, los investigadores interrumpieron la cadena de señalización cGAS/STING/IFN-I "silenciando" determinados genes, por ejemplo, para el IFN-I o para determinados macrófagos del sistema inmunitario.
A partir de los resultados obtenidos en los ratones, los investigadores concluyen que es efectivamente una sobreactivación de cGAS/STING por el ADN mal colocado en la célula lo que conduce a la enfermedad grave. Los elevados niveles sanguíneos de IFN-I y cGAMP en los pacientes estudiados sugieren que el guardián del ADN fuera de control en las células es el responsable de la progresión de la enfermedad. "Las células inmunitarias son a la vez amigas y enemigas de la enfermedad", afirma la doctora Susanne Viehmann, del laboratorio IMMEI del profesor Christian Kurts. Los macrófagos originados en la sangre producen la molécula inflamatoria IFN-I, que impulsa la enfermedad. Al mismo tiempo, otro tipo de macrófagos de los alvéolos se comen los glóbulos rojos que se escapan de los vasos, reduciendo así los factores proinflamatorios.
"Al comprender mejor los procesos moleculares de la vasculitis ANCA grave, hemos podido identificar posibles dianas farmacológicas en el modelo preclínico que ya están aprobadas para otras enfermedades", afirma Garbi. Sin embargo, todavía se necesita una investigación más intensa, añade.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.