Inteligente combinación de física cuántica y biología molecular
La inteligencia artificial ofrece una visión sin precedentes del funcionamiento de las biomoléculas
Anuncios
Una nueva técnica analítica es capaz de proporcionar una visión hasta ahora inalcanzable de la rapidísima dinámica de las biomoléculas. El equipo de desarrolladores, dirigido por Abbas Ourmazd, de la Universidad de Wisconsin-Milwaukee, y Robin Santra, del DESY, presenta su inteligente combinación de física cuántica y biología molecular en la revista científica Nature. Los científicos utilizaron la técnica para rastrear el modo en que la proteína amarilla fotoactiva (PYP) experimenta cambios en su estructura en menos de una trillonésima de segundo tras ser excitada por la luz.
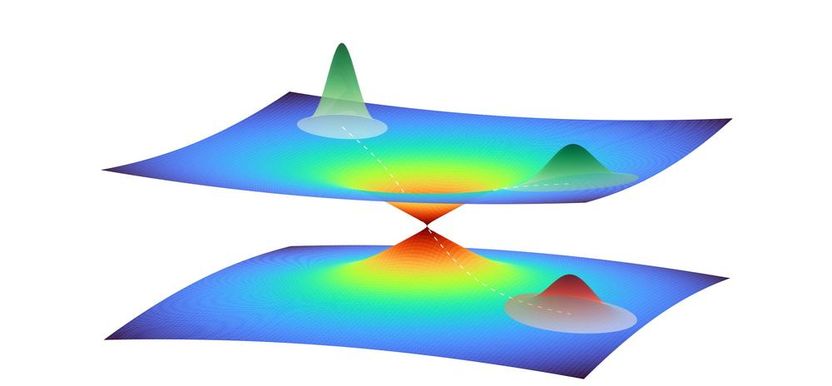
Ilustración de un paquete de ondas cuánticas en las proximidades de una intersección cónica entre dos superficies de energía potencial. El paquete de ondas representa el movimiento colectivo de múltiples átomos en la proteína amarilla fotoactiva. Una parte del paquete de ondas se mueve a través de la intersección de una superficie de energía potencial a la otra, mientras que la otra parte permanece en la superficie superior, dando lugar a una superposición de estados cuánticos.
DESY, Niels Breckwoldt
"Para entender con precisión los procesos bioquímicos en la naturaleza, como la fotosíntesis en ciertas bacterias, es importante conocer la secuencia detallada de los acontecimientos", explica Santra su motivación subyacente. "Cuando la luz incide sobre las proteínas fotoactivas, su estructura espacial se altera, y este cambio estructural determina el papel que asume una proteína en la naturaleza". Hasta ahora, sin embargo, ha sido casi imposible seguir la secuencia exacta en la que se producen los cambios estructurales. Sólo se pueden determinar los estados inicial y final de una molécula antes y después de una reacción e interpretarlos en términos teóricos. "Pero no sabemos exactamente cómo cambia la energía y la forma entre ambos", dice Santra. "Es como ver que alguien ha doblado las manos, pero no puedes ver cómo entrelaza los dedos para hacerlo".
Mientras que una mano es lo suficientemente grande y el movimiento es lo suficientemente lento como para que podamos seguirlo con los ojos, las cosas no son tan fáciles cuando se observan las moléculas. El estado energético de una molécula puede determinarse con gran precisión mediante la espectroscopia; y los rayos X brillantes, por ejemplo, de un láser de rayos X, pueden utilizarse para analizar la forma de una molécula. La longitud de onda extremadamente corta de los rayos X permite resolver estructuras espaciales muy pequeñas, como las posiciones de los átomos dentro de una molécula. Sin embargo, el resultado no es una imagen como una fotografía, sino un patrón de interferencia característico, que puede utilizarse para deducir la estructura espacial que lo ha creado.
Destellos brillantes y cortos de rayos X
Dado que los movimientos son extremadamente rápidos a nivel molecular, los científicos tienen que utilizar pulsos de rayos X extremadamente cortos para evitar que la imagen se vea borrosa. Sólo con la llegada de los láseres de rayos X fue posible producir pulsos de rayos X suficientemente brillantes y cortos para captar esta dinámica. Sin embargo, como la dinámica molecular tiene lugar en el ámbito de la física cuántica, donde las leyes de la física se desvían de nuestra experiencia cotidiana, las mediciones sólo pueden interpretarse con la ayuda de un análisis físico-cuántico.
Hay que tener en cuenta una característica peculiar de las proteínas fotoactivas: la luz incidente excita su capa de electrones para que entren en un estado cuántico superior, lo que provoca un cambio inicial en la forma de la molécula. Este cambio de forma puede provocar a su vez que los estados cuánticos excitado y básico se superpongan. En el salto cuántico resultante, el estado excitado vuelve al estado de tierra, con lo que la forma de la molécula permanece inicialmente inalterada. La intersección cónica entre los estados cuánticos abre, por tanto, una vía hacia una nueva estructura espacial de la proteína en el estado mecánico cuántico de tierra.
El equipo dirigido por Santra y Ourmazd ha logrado por primera vez desentrañar la dinámica estructural de una proteína fotoactiva en dicha intersección cónica. Para ello, han recurrido al aprendizaje automático, ya que una descripción completa de la dinámica exigiría tener en cuenta todos los movimientos posibles de todas las partículas implicadas. Esto conduce rápidamente a ecuaciones inmanejables que no pueden resolverse.
6000 dimensiones
"La proteína amarilla fotoactiva que estudiamos está formada por unos 2.000 átomos", explica Santra, científico principal del DESY y profesor de física en la Universidad de Hamburgo. "Como cada átomo es básicamente libre de moverse en las tres dimensiones espaciales, hay un total de 6000 opciones de movimiento. Eso lleva a una ecuación mecánica cuántica con 6000 dimensiones - que incluso los ordenadores más potentes de hoy en día son incapaces de resolver."
Sin embargo, los análisis informáticos basados en el aprendizaje automático fueron capaces de identificar patrones en el movimiento colectivo de los átomos de la compleja molécula. "Es como cuando se mueve una mano: ahí tampoco miramos cada átomo individualmente, sino su movimiento colectivo", explica Santra. A diferencia de una mano, donde las posibilidades de movimiento colectivo son obvias, estas opciones no son tan fáciles de identificar en los átomos de una molécula. Sin embargo, utilizando esta técnica, el ordenador pudo reducir las aproximadamente 6.000 dimensiones a cuatro. Al demostrar este nuevo método, el equipo de Santra también pudo caracterizar por primera vez una intersección cónica de estados cuánticos en una molécula compleja formada por miles de átomos.
El cálculo detallado muestra cómo se forma esta intersección cónica en el espacio cuatridimensional y cómo la proteína amarilla fotoactiva cae a través de ella de vuelta a su estado inicial tras ser excitada por la luz. Los científicos pueden ahora describir este proceso en pasos de unas decenas de femtosegundos (cuatrillonésimas de segundo) y avanzar así en la comprensión de los procesos fotoactivos. "Como resultado, la física cuántica está proporcionando nuevos conocimientos sobre un sistema biológico, y la biología está proporcionando nuevas ideas para la metodología de la mecánica cuántica", dice Santra, que también es miembro del Grupo de Excelencia de Hamburgo "CUI: Advanced Imaging of Matter". "Los dos campos se están fecundando mutuamente en el proceso".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.