Nuevas perspectivas sobre la evolución de las proteínas
Anuncios
¿Cómo se las arreglan para adaptarse a las toxinas ambientales sintéticas y, por ejemplo, para desarrollar estrategias para usar un pesticida y un agente de guerra química como alimento en menos de 70 años? Las adaptaciones evolutivas que subyacen a estos procesos han sido estudiadas en detalle por un equipo internacional de investigadores. Los científicos observaron una enzima que habían aislado de bacterias que habían estado expuestas a pesticidas en las cercanías de las fábricas que producían estos pesticidas. Usando una nueva combinación de métodos, los investigadores descubrieron qué mutaciones habían ocurrido en el gen a lo largo de los años - y cómo estas mutaciones llevaron a cambios bioquímicos que ahora permiten que la enzima rompa el pesticida.
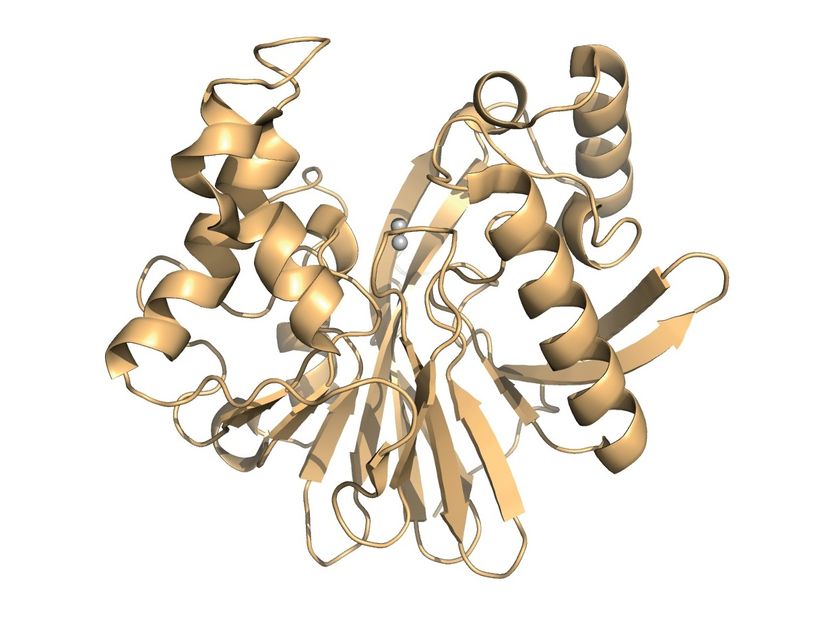
Modelo de la enzima que los investigadores investigaron en su estudio. Las dos esferas grises representan el centro activo que se une al plaguicida para partirlo.
G. Yang et al/Nat Chem Biol
"Con nuestro estudio demostramos que la técnica de la llamada reconstrucción ancestral no sólo puede utilizarse para descifrar procesos evolutivos que datan de muchos siglos atrás, sino también para investigar adaptaciones recientes con una evolución muy rápida, como las que se producen en las bacterias", subraya el coautor, el profesor Erich Bornberg-Bauer, de la Universidad de Münster, cuyo grupo participó de forma significativa en el estudio. El estudio se llevó a cabo en cooperación con el grupo de investigación dirigido por la profesora Nobuhiko Tokuriki de la Universidad de Columbia Británica en Vancouver, Canadá. Entre otras cosas, los resultados podrían ayudar a encontrar nuevas formas de descomponer y eliminar las toxinas ambientales y las sustancias químicas.
Antecedentes y método
Los investigadores utilizaron el método de reconstrucción ancestral, que utiliza algoritmos para recuperar el estado de las proteínas en los antepasados. Para ello, los científicos "resucitan" un tipo de gen primordial que se considera el punto de partida de la familia de genes actual. Clásicamente, este método se utiliza para reproducir proteínas que cambian lentamente a lo largo de millones a miles de millones de años. En este caso, los investigadores usaron este método para rastrear una enzima de muy rápida evolución durante unas cuantas décadas y descubrir mecanismos moleculares que han llevado a una función completamente nueva: la capacidad de separar el pesticida metilparatión. Sólo se ha producido industrialmente durante unos 70 años y está estrechamente relacionado con las toxinas nerviosas, que también son adecuadas para la guerra química. Los investigadores combinaron el método de reconstrucción ancestral con pruebas bioquímicas y estructurales de la proteína "resucitada" en el laboratorio e identificaron cinco mutaciones que son las principales responsables de la transición funcional de la proteína en el tiempo.
En un paso más, los científicos investigaron hasta qué punto estas mutaciones cambiaron la llamada aptitud, es decir, el grado en que los genes se adaptaron en ciertos momentos del tiempo. Además, caracterizaron muchas combinaciones diferentes de las mutaciones. Utilizaron análisis estadísticos novedosos para determinar la interacción de los genes y su diferente dominancia. Estos análisis proporcionaron información sobre las interacciones moleculares subyacentes, tanto dentro de la enzima como entre la enzima y el plaguicida.
Los investigadores encontraron que las cinco más importantes de las mutaciones identificadas juegan juntas en una red compleja y, en última instancia, permiten que el centro activo de la enzima se conecte mejor con el plaguicida y, por lo tanto, desarrolle nuevas funciones. "Nuestro método combinado también se puede utilizar en muchos otros casos para conocer mejor los mecanismos moleculares que subyacen a la evolución de las proteínas", dijo el coautor Elias Dohmen de la Universidad de Münster, quien reconstruyó las secuencias de proteínas ancestrales para el estudio como parte de su tesis doctoral en el grupo de Evolución Molecular y Bioinformática.
En investigaciones futuras, los científicos planean probar más proteínas con diferentes funciones con el fin de derivar reglas generalmente utilizables de la metodología. Además, quieren recoger aún más datos de secuencia para poder crear mejores reconstrucciones ancestrales.
Los nuevos conocimientos adquiridos son relevantes para la llamada evolución dirigida, un proceso que tiene como objetivo la optimización de enzimas y proteínas y que se utiliza principalmente en la biotecnología industrial. En 2018, Frances Arnold, del California Institute of Technology, recibió el Premio Nobel de Química por este método.
Además de la Universidad de Columbia Británica en Vancouver y la Universidad de Münster, las Universidades de Canberra en Australia y Uppsala en Suecia participaron en el estudio.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.