Neue Erkenntnisse zur Entstehung von Krebs
Anzeigen
Forscher der Universität Würzburg haben neue Signalwege identifiziert, die bei der Zellteilung von Bedeutung sind. Ihre Entdeckung kann als Angriffspunkt für neue Medikamente dienen.
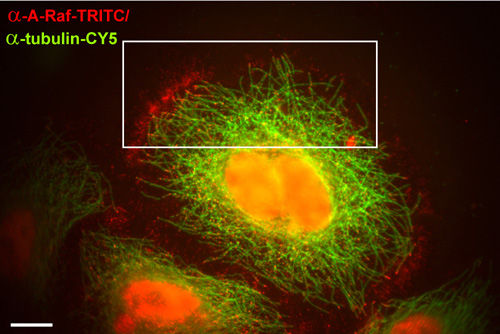
A-RAF-Kinase (rot) findet sich in der Zelle unter anderem in Endosomen im peri-plasmatischen Bereich und entlang der Mikrotubuli, hier grün gefärbt.
MSZ
Jede Zelle eines jeden Organismus steht normalerweise in ständigem Kontakt zu ihrer Umgebung. Rezeptoren an ihrer Oberfläche nehmen Signale von außen auf und transportieren sie ins Zellinnere, wo dann die weitere Verarbeitung geschieht.
Diesen Transport darf man sich nicht so vorstellen wie ein Förderband am Flughafen, das Handgepäck auf der einen Seite aufnimmt, durch den Röntgenapparat hindurchbefördert und jenseits davon wieder ausspuckt. In der Regel funktioniert die Signalübertragung im Organismus sehr viel aufwendiger, meist über mehrere Stufen hinweg in Form einer Kaskade, bei der mehrere Eiweiße nacheinander miteinander agieren.
Eine der wichtigsten dieser Kaskaden im menschlichen Organismus ist die so genannte MAP-Kaskade. Sie spielt bei der Zellteilung eine wichtige Rolle und wenn es darum geht, dass sich Zellen zu einer bestimmten Gewebsform entwickeln. Dass sich daraus ein enger Zusammenhang zur Entstehung von Krebszellen ergibt, liegt auf der Hand. Wichtig ist diese Kaskade aber auch bei der Reizweiterleitung im Nervensystem, wo permanent Signale zwischen den einzelnen Nervenzellen übertragen werden müssen.
Mit einem Enzym, das am Anfang der MAP-Kaskade steht, hat sich Elena Nekhoroshkova beschäftigt. Die 34-Jährige forscht am Institut für Medizinische Strahlenkunde und Zellforschung der Universität Würzburg am Lehrstuhl von Professor Ulf Rapp. Im Rahmen ihrer Doktorarbeit galt ihr besonderes Interesse einer Unterform der so genannten RAF-Kinasen. "Von ihnen gibt es drei bekannte Arten: Die RAF-Familienmitglieder B und C, von denen bekannt ist, dass eine erhöhte Aktivität ihrerseits zur Tumorbildung führen kann", erklärt Nekhoroshkova. Die dritte Variante hingegen, A-RAF, ist vergleichsweise wenig aktiv und darum bislang nicht intensiv erforscht worden. Sie sei "im Schatten der größeren Brüder gestanden", sagt die Wissenschaftlerin, die sich deshalb intensiv um A-RAF gekümmert hat.
Elena Nekhoroshkova ist es gelungen, eine bislang unbekannte Funktion dieses Enzyms nachzuweisen. "Dank seiner besonderen Fähigkeiten sitzt A-RAF an ganz bestimmten Stellen der Zellmembran und reguliert von dort aus die Aktivität der Rezeptoren", sagt Nekhoroshkova. Somit komme dem Enzym sowohl bei der Entstehung von Krebs als bei der Arbeit des Nervensystems eine wichtige Rolle zu. Gleichzeitig hat die junge Wissenschaftlerin weitere Proteine identifiziert, die im Zusammenspiel mit einer Variante von A-RAF mal bremsend, mal beschleunigend auf die Rezeptoren einwirkt.
"Dieser neue Signalweg ist vielversprechend als Ansatzpunkt für die Entwicklung neuer Krebstherapeutika", sagt Elena Nekhoroshkova. Ihrer Meinung nach könne damit sofort begonnen werden.
Originalveröffentlichung: Nekhoroshkova E, Albert S, Becker M, Rapp UR; "A-RAF Kinase Functions in ARF6 Regulated Endocytic Membrane Traffic"; PLoS ONE 2009, 4(2): e4647























































