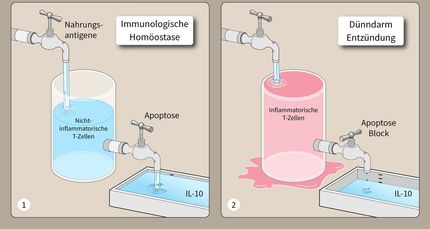
cFLIP: ein Schalter bei der Entscheidung über Leben und Tod von Hauttumorzellen
Anzeigen
Angesichts der weiter zunehmenden UV-Bestrahlung der Bevölkerung und dem immer höheren Lebensalter der Bevölkerung wird der weisse Hautkrebs in den kommenden Jahrzehnten deutlich weiter ansteigen. Eine defekte Regulierung des sogenannten programmierten Zelltodes (Apoptose) kommt bei der Entwicklung von Hautkrebs eine wichtige Bedeutung zu. Welche Mechanismen Hauttumorzellen zum Wachstum anregen, untersucht eine Arbeitsgruppe um den Magdeburger Mediziner Martin Leverkus. Das Ziel ist es, neue Ansätze zur Behandlung von Hautkrebs zu entdecken und zu verstehen, wie die Resistenz gegenüber dem programmierten Zelltod durchbrechen können.
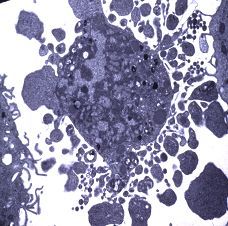
Auslösung von programmiertem Zelltod bei Zellen des Plattenepithelkarzinoms der Haut; elektronenmikroskopische Darstellung.
Arbeitsgruppe Professor Dr. Leverkus
Weißer Hautkrebs oder Plattenepithelkarzinom: Dies sind die Fachausdrücke für die häufigste Krebserkrankung des Menschen. Betroffen werden insbesondere Menschen im fortgeschrittenen Lebensalter, die stark der UV-Strahlung ausgesetzt waren. Die ersten Tumorzellen entstehen z.T. Jahrzehnte zuvor und werden erst durch weitere UV-Bestrahlung zu invasiven und damit gefährlichen Karzinomen", erklärt Martin Leverkus. Beim weißen Hautkrebs spielt offenbar ein in der Zelle vorhandenes Eiweiß, cFLIP, eine wichtige Rolle. So kann durch dieses Molekül die Auslösung des programmierten Zelltodes durch Botenstoffe blockiert werden. Interessanterweise binden diese Botenstoffe an Oberflächenmoleküle der Tumorzellen und können dadurch Apoptose auslösen. Ist der Inhibitor cFLIP stark exprimiert, können diese Botenstoffe nicht mehr programmierten Zelltod auslösen, sondern vielmehr andere tumorfördernde Signalwege der Zelle anschalten. Um die Bedeutung des Moleküls cFLIP, das in der Zelle in verschiedenen Formen vorkommen kann, genauer studieren zu können, arbeitet die Arbeitsgruppe mit Hilfe von Viren, die in der Lage sind, verschiedene Formen dieses Inhibitors in Tumorzellen einzuschleusen.
"Durch Einschleusung dieser Eiweiße in die Zelle erhoffen wir uns Aussagen über ihre Bedeutung bei der Entwicklung von Hautkrebs" sagt Leverkus weiter. Für zukünftige Therapien könnten aus den Erkenntnissen der Arbeitsgruppe von Leverkus wichtige Schlussfolgerungen für die Behandlung von Hautkrebs abgeleitet werden: "Wenn wir verstanden haben, wodurch cFLIP in der Zelle reguliert wird, werden daraus möglicherweise Wege identifiziert werden können, auch in Hautkrebszellen diese Eiweiße abzuschalten." Nunmehr wird in einem neuen von der Wilhelm-Sander-Stiftung geförderten Projekt studiert, ob cFLIP im Reagenzglas als auch im Mausmodell ähnliche Wirkungen erzielt. Die Gruppe um Martin Leverkus erhofft sich, aus den Erkenntnissen des Projektes zukünftig auch Therapieverfahren zur gezielten Veränderung der Expression des Inhibitors cFLIP in Hautkrebszellen entwickeln zu können. Die Arbeitsgruppe für Experimentelle Dermatologie wird deshalb die verschiedenen Facetten des Moleküls cFLIP in den nächsten Jahren weiter beim weißen Hautkrebs aufklären, die hoffentlich die Grundlage für einen möglichen Einsatz von gezielten blockierenden Substanzen in der Therapie des weißen Hautkrebses schaffen.
Die Wilhelm Sander-Stiftung fördert dieses Forschungsprojekt mit über 150.000 €.