Genetischen Ursachen von Übergewicht auf der Spur
Wissenschaftler haben einen neuen Regulator bei der zellulären Fettspeicherung entdeckt
Zuviel Fett im Körpergewebe kann zu schwerwiegenden gesundheitlichen Folgen wie Diabetes oder Bluthochdruck führen. Forscher vom Max-Planck-Institut für Biophysikalische Chemie und den National Institutes of Health haben jetzt einen Proteinkomplex entdeckt, der beim Abbau des Körperfetts eine entscheidende Rolle zu spielen scheint.
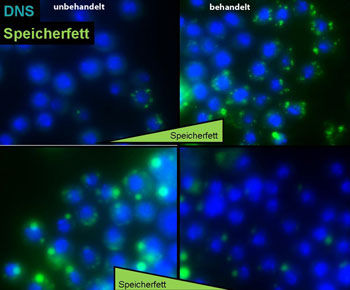
Drosophila-Zellen, in denen die DNA blau und Speicherfette grün gefärbt sind. Durch die Behandlung mit RNA Interferenz (RNAi) gegen Regulatorgene des Fettaufbaus und -abbaus (obere Reihe: COPI, untere Reihe: Lipidtröpfchen-Protein) kann der Fettgehalt erhöht (obere Reihe) bzw. verringert (untere Reihe) werden. Rund 500 Gene konnten identifiziert werden, die den Fettgehalt der Zellen veränderten.
Max-Planck-Institut für biophysikalische Chemie/Beller
Lebewesen sichern ihr Überleben unter anderem dadurch, dass sie in Zeiten des Nahrungsüberschusses kontrolliert Fett speichern. In kleinen Lipidtröpfchen wird dieses in der Zelle zwischengespeichert und kann in Hungerzeiten wieder mobilisiert werden. Ist die Regulation von Fettaufbau und Fettabbau gestört, sind krankhaftes Übergewicht und Fettleibigkeit (Adipositas) die Folge.
Längst ist Adipositas nicht mehr nur ein Problem westlicher Überflussgesellschaften, sondern betrifft eine wachsende Anzahl von Menschen weltweit. Ein Überangebot energiereicher Nahrungsmittel, kombiniert mit geringer Bewegung, ist ohne Zweifel einer der entscheidenden Faktoren, die zu Fettleibigkeit führen. Doch trotz eines ähnlichen Lebensstils kann die Gewichtszunahme von Mensch zu Mensch enorm variieren. Immer mehr wissenschaftliche Studien weisen inzwischen auch auf eine starke genetische Prädisposition hin. Diese beruht auf dem komplexen Zusammenspiel vieler Gene, von denen längst nicht alle bekannt sind.
Systematisches Screening im Erbgut der Fliege
Einem internationalen Wissenschaftlerteam um Mathias Beller vom Göttinger Max-Planck-Institut für biophysikalische Chemie sowie Carole Sztalryd und Brian Oliver von den National Institutes of Health (Bethesda, USA), gelang es nun, in der Taufliege eine Vielzahl neuer Gene zu identifizieren, die in Abhängigkeit vom Ernährungszustand des Insekts den Fettauf- und -abbau regulieren. Dazu führten die Wissenschaftler ein systematisches Screening im Erbgut der Taufliege Drosophila melanogaster mittels RNA Interferenz (RNAi)-Technik durch. Dabei binden kurze RNAs an komplementäre Abschnitte der Gen-Transkripte und verhindern so, dass diese abgelesen und zur Proteinherstellung genutzt werden. Einzelne Gene können so gewissermaßen stumm geschaltet werden.
Es gibt zwar keine offensichtlich dicken oder dünnen Taufliegen, doch kann der Körperfettgehalt fetter Artgenossen 15-mal höher sein als bei mageren Exemplaren. Rund 500 neue Kandidaten fanden die Forscher über ihre systematische Suche, die Funktion knapp eines Drittels davon ist noch unbekannt.
Fehlendes Protein bewirkt Stopp bei Fettabbau und Verbrennung
"Völlig überraschend haben wir dabei auch den COPI-Proteinkomplex identifiziert, der eine Schlüsselrolle in einem ganz anderen, lebenswichtigen Prozess der Zelle übernimmt, dem intrazellulären Transport von Proteinen und Lipiden", erklärt der Göttinger Entwicklungsbiologe Mathias Beller. Ob das COPI (Coat Protein Complex) direkt mit den Lipidtröpfchen interagiert, ist noch nicht genau geklärt. "Unsere Ergebnisse deuten aber stark darauf hin, dass COPI auf der Lipidtröpfchen-Oberfläche agieren und deren Protein-Zusammensetzung regulieren könnte."
Schalteten die Wissenschaftler den COPI-Komplex aus, der aus mindestens sieben Proteinen besteht, so fehlte vor allem ein Mitspieler im Proteinverband auf den Lipidtröpfchen, das ATGL (Adipose Tryglyceride Lipase). Mit fatalen Folgen für den Organismus: Wenn ATGL fehlt, können überschüssige Fettreserven nicht abgebaut und als Energiequelle genutzt werden. Dem Modell der Forscher zufolge könnte COPI das ATGL über einen noch unbekannten Mechanismus rekrutieren und aktivieren und so dessen Bindung an die Lipidtröpfchen-Oberfläche fördern.
Lernen lässt sich aus den neuen Ergebnissen aber nicht nur etwas über Fettleibigkeit bei Fliegen. Wie die Forscher herausfanden, hat COPI in Mauszellen - und damit möglicherweise auch in menschlichen Zellen - offenbar eine ganz ähnliche Funktion. Dies scheint nicht nur für das COPI, sondern auch andere neu identifizierte Kandidaten zu gelten. "Unser Ziel ist nun, Moleküle zu finden, mit denen wir gezielt in das Zusammenspiel von COPI und ATGL eingreifen können. Diese könnten zukünftig neue therapeutische Möglichkeiten eröffnen, Fettleibigkeit und Übergewicht zu behandeln", sagt Beller.
Originalveröffentlichung: Mathias Beller et al.; "COPI Complex is a Regulator of Lipid Homeostasis" PLOS Biology, 25. November 2008


























































