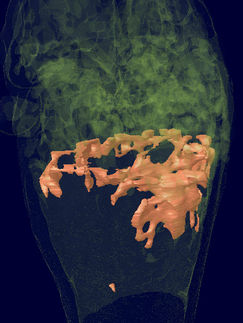
Blick ins "Herz" einer zellulären molekularen Maschine
Wie aus der Erbsubstanz einer Zelle Proteine erzeugt werden, ist ein zentrales Thema biologischer Forschung. Eine besondere Rolle spielen dabei kleine molekulare Maschinen in der Zelle - die Spleißosomen. Sie bringen die Bauanleitungen für die Proteine in eine "lesbare" Form, in der die Information direkt für die Proteinherstellung genutzt werden kann. Die Komplexität und hohe Dynamik der Spleißosomen machten es bisher jedoch unmöglich, ihre Funktionsweise im Detail zu untersuchen. Wissenschaftlern am MPI für Biophysikalische Chemie ist es nun erstmals gelungen, faszinierende Einblicke in das aktive "Herzstück" der Spleißosomen zu erhalten.
In den Zellen unseres Körpers werden alle wichtigen Funktionen - Katalyse, Bewegungs- und Transportprozesse, Signalübertragung und Informationsverarbeitung - von Proteinen ausgeführt. Die Bauanleitungen dieser Proteine sind in der Erbsubstanz einer jeden Zelle archiviert. Allerdings ist diese Information für die Herstellung von Proteinen nicht direkt nutzbar. Dazu müssen die Baupläne zunächst in eine Boten-RNA umkopiert werden. In dieser Rohfassung der Boten-RNA enthalten die Bauanleitungen aber noch einigen Ballast; sie sind nicht durchgängig "lesbar". Erst wenn die dazwischen liegenden überflüssigen Abschnitte entfernt werden, können die Bauanleitungen richtig interpretiert werden. Das präzise Herausschneiden nicht benötigter Abschnitte und das Verbinden erforderlicher Teilstücke erfolgen dabei ganz ähnlich dem Trennen und Verknüpfen von Seilenden in der Seefahrt. In Analogie dazu bezeichnen Wissenschaftler den zellulären Vorgang als "Spleißen".
Das Spleißen erfolgt mit Hilfe einer komplexen makromolekularen Maschine aus über 150 Proteinen und bis zu fünf RNA-Molekülen - dem Spleißosom. Dieses muss sich für jede Runde von Schneiden und Verknüpfen auf der RNA neu zusammenbauen. Dazu werden im Zellkern aus einer Vielzahl von Einzelkomponenten zunächst eine Reihe vorgefertigter Komplexe bereitgestellt. Diese werden dann in einem hochdynamischen Prozess in wenigen Schritten zum funktionsfähigen Spleißosom zusammengesetzt. Doch sind Spleißosomen nicht nur hochdynamisch, sondern auch äußerst empfindlich. Versuche, sie ohne Verlust ihrer Aktivität aufzureinigen, blieben daher bisher erfolglos.
Wissenschaftlern vom Göttinger Max-Planck-Institut für biophysikalische Chemie unter Leitung von Prof. Reinhard Lührmann ist es nun erstmals gelungen, aktive Spleißosomen-Komplexe zu isolieren. "Spleißsomen-Komplexe direkt bei ihrer Arbeit untersuchen zu können, ermöglicht uns neue detaillierte Einblicke in den Mechanismus des Spleißens. Dabei können wir auch genau bestimmen, welche Proteine der Zelle für diesen Prozess unentbehrlich sind", erklärt Henning Urlaub, einer der am Projekt beteiligten Forschungsgruppenleiter. Mit Hilfe der stabilen Spleißosomen-Komplexe können Wissenschaftler das Spleißosom zudem auch strukturell im aktiven Zustand untersuchen. Die räumliche Struktur des Spleißosoms "in Aktion" zu kennen, sei eine wesentliche Voraussetzung, im Detail zu verstehen, wie es funktioniert, so die Wissenschaftler.
Durch unterschiedliche Verknüpfung und geschicktes Überspringen bestimmter Teilabschnitte der Bauanleitung ermöglicht das Spleißen, eine schier unendliche Vielfalt von Proteinen aus einem begrenzten Vorrat an DNA herzustellen. Für die komplexen Aufgaben, die die Zellen höher entwickelter Organismen ausführen, ist diese Proteinvielfalt unentbehrlich. Somit ist nicht verwunderlich, dass eine Vielzahl von Krankheiten - darunter viele bösartige Tumorkrankheiten und neurodegenerative Erkrankungen - auf Fehler im Spleißen der Boten-RNA zurückzuführen sind. Die Funktion und Dynamik des Spleißprozesses im molekularen Detail zu kennen, könnte daher zukünftig auch dazu beitragen, Therapien weiterzuentwickeln und neue Therapieansätze zu ermöglichen.
Originalveröffentlichung: Nature 2008, 452.
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren

Antibody Stabilizer von CANDOR Bioscience
Protein- und Antikörperstabilisierung leicht gemacht
Langzeitlagerung ohne Einfrieren – Einfache Anwendung, zuverlässiger Schutz

DynaPro NanoStar II von Wyatt Technology
NanoStar II: DLS und SLS mit Touch-Bedienung
Größe, Partikelkonzentration und mehr für Proteine, Viren und andere Biomoleküle

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.