Wie «Schläferzellen» in Krebstumoren zerstört werden können
Trotz erfolgreicher Chemotherapie wachsen in vielen metastasierten Krebsarten verstreute Tumore wieder zurück. Wie ein Forschungsteam unter der Leitung der Universität Bern nun herausgefunden hat, liegt das an vereinzelten Krebszellen, welche wegen einer Ruhephase die Chemotherapie überleben. Wenn diese «Schläferzellen» jedoch spezifische Defekte aufweisen, können sie vernichtet werden. Das könnte die Wirksamkeit der Chemotherapie bei bestimmten Patienten erhöhen.
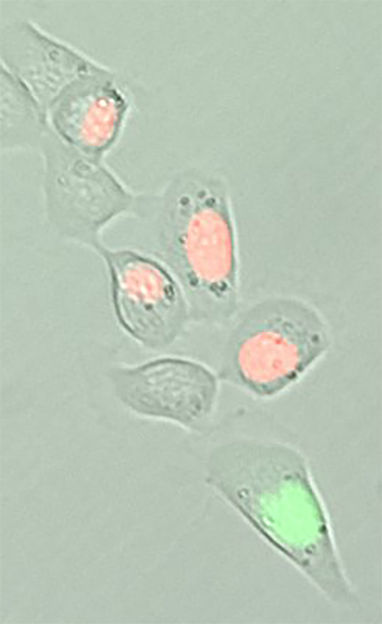
«Schläferzellen» aufspüren: mit neuen Markern lassen sich die medikamenten-toleranten Zellen (ohne farbigen Zellkern) von aktiven, sich teilenden Tumorzellen (rote oder grüne Zellkerne) herausfiltern.
Bild: zvg
Viele haben es im Familien-, Freundes- oder Bekanntenkreis erlebt: Die Chemotherapie schlägt bei Krebspatienten zunächst hervorragend an, obwohl der Tumor metastasiert, also in entferntes Gewebe abgesiedelt hat. In einigen Fällen scheint der Krebs sogar besiegt zu sein. Doch dann folgt die Ernüchterung: Einige wenige Krebszellen haben überlebt und vermehren sich wieder. Teilweise sprechen sie auch wieder auf eine erneute Therapie an, entwickeln dann aber doch eine Resistenz gegen alle Therapiemethoden. «Uns interessiert, wieso einzelne Tumorzellen die Therapie überleben können», sagt Sven Rottenberg von der Vetsuisse Fakultät der Universität Bern. Ein internationales Forschungsteam unter seiner Leitung hat nun sogenannte Schläferzellen identifiziert, welche der Therapie entkommen. Da Chemotherapien sich insbesondere gegen aktive, sich teilende Tumorzellen richten, können einige dieser Schläferzellen mit Hilfe einer kurzfristigen Wachstumspause überleben. Nach Beendigung der Therapie fangen sie dann wieder an, sich zu vermehren. Wenn diese Schläferzellen jedoch eine spezifische Mutation aufweisen, die sie an der Reparatur von eigenen DNA-Schäden hindert, können sie gezielt mit Medikamenten zerstört werden.
Mögliche Alternative zur Immuntherapie
Wenn Tumore nach einer Behandlung wieder zurückwachsen, sprechen sie manchmal wieder auf die gleiche Chemotherapie an. Sie haben also keine sogenannte «sekundäre Resistenz» erworben, denn dann würden sie bei erneuter Therapie einfach weiter wachsen. «Bei den wenigen verbliebenen Tumorzellen, welche die Chemotherapie überleben, sprechen wir in diesem Fall von sogenannten ‹Medikamenten-toleranten Zellen›», sagt Rottenberg. Wie kann man diese verbliebenen Zellen nun vernichten? «Für bestimmte Krebsarten wie Leukämien oder Melanome gibt es bereits enorme Fortschritte im Bereich der Immuntherapie. Diese zeichnet sich durch die gezielte Stärkung von körpereigenen Immunzellen aus im Gegensatz zur Chemotherapie, mit der eine direkte Zerstörung der Krebszellen angestrebt wird. Mit dieser gegen die Krebszellen gerichteten Stärkung des Immunsystems können bei einigen Patientinnen und Patienten auch die medikamenten-toleranten Zellen vernichtet werden.» Die Erfolge dieser neuen Immuntherapie bei anderen häufigen Tumoren sind aber laut Rottenberg noch bescheiden – zudem verursachen sie Nebenwirkungen und enorme Kosten.
Nun konnten die Forschenden im Mausmodell eine Alternative aufzeigen: Bei Brusttumoren mit einem spezifischen Defekt in der DNA-Reparatur können die Tiere mit bereits etablierten und günstigen Chemotherapie-Medikamenten geheilt werden, wenn genügend DNA-Schäden in den ruhenden Tumorzellen erreicht werden. Rottenberg hofft, dass aufgrund dieser Befunde die Therapie von Brust-, Eierstock- und Prostatakrebs in der Zukunft verbessert werden kann.
Defekt bei DNA-Reparatur als Achillesferse der Krebszellen
Hintergrund sind die Fortschritte im Bereich der personalisierten Medizin. Krebsarten werden nicht mehr nur nach Ursprung des Gewebes eingeteilt und behandelt, sondern es wird mit gezielten Analysen (etwa der Sequenzierung von Genen oder der Untersuchung nach dem Vorhandensein von bestimmten Proteinen) nach individuellen Mutationen gesucht, die therapeutisch ausgenutzt werden können. Ein Beispiel sind Defekte in der DNA-Reparatur. Diese entstehen durch eine Fehlfunktion von Proteinen, die in normalen Körperzellen DNA-Schäden reparieren. Sind diese Proteine inaktiv – was bei vielen Patientinnen und Patienten mit Brust-, Eierstock- oder Prostatakrebs der Fall ist – kommt es zu einer fehlerhaften Reparatur. Das kann therapeutisch ausgenutzt werden, wie Rottenberg erläutert: «DNA-reparatur-defekte Schläferzellen sprechen auf bestimmte Stoffe an, welche die DNA schädigen.» Diese Stoffe treffen sowohl gesunde Zellen wie auch den Krebs. Im Gegensatz zu normalen Zellen sind die Tumorzellen aber deutlich empfindlicher, da sie den Schaden nicht gut reparieren können. Im Tiermodell zeigten sich dabei sogenannte DNA-Crosslinker als sehr effizient. Diese sind bereits lange auf dem Markt, werden aber bisher nicht speziell für Krebsarten mit solchen Defekten eingesetzt.
Wie die meisten Krebsmedikamente haben auch diese Stoffe starke Nebenwirkungen wie etwa Knochenmarksschädigungen. Bei bestimmten Patientinnen und Patienten könnten diese Nebenwirkungen allerdings durch eine Stammzelltransplantation ausgeglichen werden, ähnlich wie bei Leukämie-Behandlungen. «Erste klinische Versuche in den Niederlanden haben gezeigt, dass einige Brustkrebspatientinnen mit metastasierten Brustkrebs tatsächlich durch eine solche intensivierte Chemotherapie geheilt werden konnten», sagt Rottenberg.
Originalveröffentlichung
Pajic M, Blatter S, Guyader C, Gonggrijp M, Kersbergen A, Küçükosmanoglu A, Sol W, Drost R, Jonkers J, Borst P, Rottenberg S; "Selected alkylating agents can overcome drug tolerance of G0-like tumor cells and eradicate BRCA1-deficient mammary tumors in mice"; Clinical Cancer Research, in press (2017).