Brüchiges Erbgut: Neuer Therapie-Ansatz gegen Speiseröhrenkrebs
Anzeigen
Bei Speiseröhrenkrebs könnte eine medikamentöse Strategie erfolgreich sein, die bereits bei Leukämien im klinischen Einsatz ist. Das zeigen Forscher des Universitätsklinikums Freiburg. Sie behandelten gesunde und entartete Speiseröhrenepithelzellen mit „epigenetisch“ wirksamen Substanzen, die das Erbgut der Krebszellen brüchig machen. Während die gesunden Zellen überlebten, starben die Krebszellen ab. Ein solcher epigenetischer Therapie-Ansatz könnte bei inoperablem Speiseröhrenkrebs zielgerichteter wirken als bisherige Strahlen-und Chemotherapien. Die in der Zeitschrift Epigenetics veröffentlichte Studie könnte langfristig zu effektiveren und verträglicheren Krebs-Therapien beitragen.
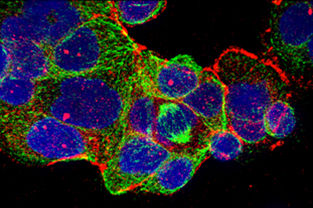
Speiseröhrenkrebszellen in der Petrischale angefärbt: Blau: DNA im Zellkern, Rot und Grün: Eiweißstoffe in der Zelle
Universitätsklinikum Freiburg
Speiseröhrenkrebs in der westlichen Welt stark auf dem Vormarsch
6.500 Menschen erkrankten im Jahr 2012 in Deutschland an Speiseröhrenkrebs, der damit zwar zu den selteneren Tumorerkrankungen gehört; gleichzeitig zeigt er aber eine der höchsten Zuwachsraten an Neuerkrankungen. Die Zahlen haben sich seit 1990 mehr als versiebenfacht. Grund sind vermutlich verändertere Lebens- und Ernährungsgewohnheiten. Wichtigste Risikofaktoren sind langjähriges Sodbrennen, Alkoholkonsum und Rauchen. Es gibt zwei häufige histologische und klinische Typen von Speiseröhrenkrebs, das Adenokarzinom und das Plattenepithelkarzinom. Bislang werden Erkrankte chirurgisch, mit Strahlen- oder Chemotherapie oder einer Kombination aus beidem behandelt. Wegen der meist späten Diagnose überlebt aber gerade einmal jeder fünfte Patient mehr als fünf Jahre – trotz Therapie.
Epigenetische Behandlung wirkt gezielt gegen Krebszellen
Einen gänzlich neuen Ansatz im Kampf gegen Speiseröhrenkrebs hat nun die Forschergruppe von Prof. Dr. Silke Lassmann und Prof. Dr. med. Martin Werner am Institut für Klinische Pathologie des Universitätsklinikums Freiburg erprobt. Die jetzt erschienene Studie ist in enger Zusammenarbeit mit dem Deutschen Konsortium für Translationale Krebsforschung entstanden, dem Prof. Lassmann und Prof. Werner angehören sowie dem Exzellenzcluster BIOSS Centre for Biological Signalling Studies der Universität Freiburg, an dem Prof. Lassmann Assoziiertes Mitglied ist.
Im Labor behandelten sie mit ihrem Team junger Wissenschaftlerinnen und Wissenschaftler Zellkulturen aus normalen und entarteten Zellen mit vier „epigenetisch“ wirksamen Substanzen, die das Erbmaterial auflockern und dadurch zerbrechlicher machen. Bricht das Erbmaterial, führt dies meist zum Absterben der Zelle. Die Wirkstoffe wurden jeweils allein und in Kombination auf die Zellen aufgebracht. Während sich die Zellen gegen einzelne Substanzen zur Wehr setzen konnten, starben die Krebszellen bei der Kombination der beiden Stoffe Entinostat und Azacitidin. Gesunde Zellen nahmen auch dann keinen Schaden.
„Gesunde Zellen haben offenbar noch einen Plan B, also Schutz- und Reparatur-Mechanismen, die bei Krebszellen nicht mehr funktionieren. Das macht die Krebszellen anfälliger“, sagt Prof. Lassmann. Welche Schutzmechanismen bei gesunden Zellen vorhanden sind und bei Krebszellen fehlen, möchten die Forscher als nächstes herausfinden. Azacitidin ist bereits für die Behandlung von Leukämien zugelassen. Für Entinostat läuft derzeit die Zulassung in der Krebstherapie.
Ergebnisse möglicherweise auch auf andere Tumoren übertragbar
In Gewebeschnitten von operativ entferntem Speiseröhrenkrebs wiesen die Forscher jene Zielstrukturen nach, gegen die die epigenetischen Wirkstoffe gerichtet sind. Auch in Darmkrebs-Gewebe und anderen Tumorarten des Magen-Darm-Trakts ließen sich dieselben molekularen Ziele identifizieren. Das spricht dafür, dass sich die Erkenntnisse zumindest teilweise auf andere Tumorarten übertragen lassen.
„Grundsätzlich besteht die Möglichkeit, dass sich daraus ein neuer Ansatz im Kampf gegen Speiseröhrenkrebs entwickeln lässt. Aber klar ist: das ist nur ein erster Schritt und viele weitere müssen folgen“, dämpft Prof. Lassmann zu große Hoffnungen.
Die Forschungsarbeit ist im Rahmen des Sonderforschungsbereichs SFB 992 „Medizinische Epigenetik – Von grundlegenden Mechanismen zu klinischen Anwendungen“ entstanden, dem die Arbeitsgruppe von Prof. Lassmann angehört. Gleichzeitig besteht ein intensiver Austausch mit dem Zentrum für Gastrointestinale Tumore des Universitätsklinikums Freiburg, das Diagnose und Therapie auf dem neuesten Stand der Forschung betreibt.