Genetische Krankheiten verschieben Grenzen im Genom
Forscher erklären Entstehung seltener Erkrankungen durch Zerstörung funktionaler Grenzen innerhalb der DNA
Anzeigen
Neuere Untersuchungen haben gezeigt, dass unser Genom und das von anderen Säugetieren in große funktionelle Einheiten unterteilt ist, die sogenannten TADs (topologically associated domains). Dabei handelt es sich um sehr lange DNA-Abschnitte, die ein oder mehrere Gene und deren regulatorische Elemente enthalten: Eine wichtige Funktion der TADs scheint zu sein, abgeschlossene Bereiche der Genregulation zu bilden und diese gleichzeitig gegen Nachbarbereiche abzuschirmen. Wissenschaftler des Max-Planck-Instituts für molekulare Genetik und der Charité – Universitätsmedizin Berlin haben jetzt an drei genetisch bedingten seltenen Erkrankungen des Menschen gezeigt, dass Veränderungen der äußeren Grenzen der TADs zu erheblichen Störungen bei der Regulation der zugehörigen Gene führen können. Die TADs haben also für die ordnungsgemäße Funktion der Gene die große Bedeutung. Die Ergebnisse der Forscher zeigen, dass für die Entstehung einer Erkrankung nicht nur Veränderungen an kodierenden Genen selbst, sondern überraschenderweise auch Veränderungen in weit von den jeweiligen Genen entfernt liegenden nicht-kodierenden Regionen verantwortlich sein können.
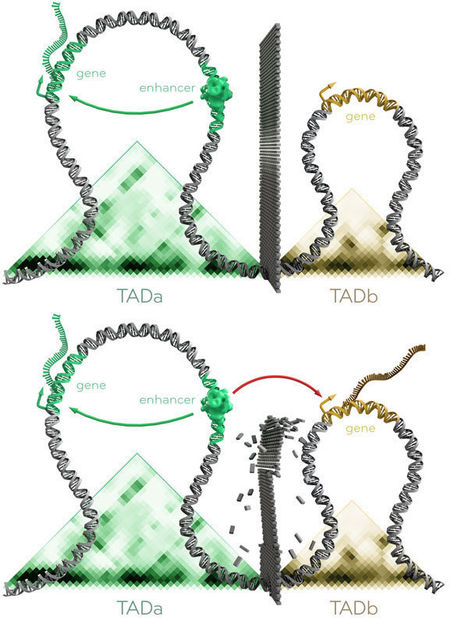
Schematische Darstellung zweier TADs in gesunden Genom. Oben: Die "Mauer" zwischen den beiden Bereichen bewirkt, dass der Regulator (=enhancer) in TADa nur das Gen in TADa beeinflussen kann, nicht aber das Gen in TADb. Unten: Wenn die Grenze zwischen zwei TADs aufgrund einer Mutation verändert oder verschoben wird, kann der Regulator/enhancer auch diejenigen Gene beeinflussen, die zuvor vor ihm abgeschirmt waren.
© MPI f. molekulare Genetik/ Thomas Splettstoesser
Das menschliche Genom hat etwa 20.000 Gene, fast genauso viele wie der nur einen Millimenter kleine Fadenwurm C. elegans. Mensch und Fadenwurm - zwei in ihrer biologischen Komplexität völlig unterschiedliche Organismen - beruhen auf fast der gleichen Anzahl an Genen. Dies liegt daran, dass der Mensch sein genetisches Potenzial besser ausschöpft, zum einen durch die Modifikation von Genprodukten, aber auch durch den vielfachen Einsatz der gleichen Gene für unterschiedliche Funktionen.
Dafür ist ein hoher Grad an Steuerung erforderlich, tragen doch alle Zellen des Körpers die gleiche genetische Information. Wissenschaftler schätzen, dass etwa 40 Prozent unseres Genoms nur für die Regulation der Gene erforderlich ist. Es ist aber noch weitgehend unklar, wie sichergestellt wird, welche Regulatoren welche Gene beeinflussen bzw. nicht beeinflussen.
Eine wesentliche Rolle spielen dabei sogenannte TADs (topologically associated domains): Bereiche, in denen das Genom große dreidimensionale Strukturen aus Histonen, regulatorischen Proteinen und Transkriptionsfaktoren bildet. Eine TAD umfassßt jeweils ein oder mehrere Gene, sowie alle regulatorischen Elemente, von denen diese beeinflußt werden. Ihre Struktur ist sowohl in unterschiedlichen Zelltypen als auch in verschiedenen Tierarten nachweisbar, sie gelten daher als hoch konserviert. Regulatorische Elemente innerhalb einer TAD beschränken ihre Aktivität auf „ihre“ TAD, umgekehrt werden Gene in benachbarten TADs von dieser Aktivität abgeschirmt.
Die Bedeutung der TADs im Zusammenhang mit der Entstehung von Krankheiten haben jetzt Wissenschaftler des Max-Planck-Instituts für molekulare Genetik und der Charité – Universitätsmedizin Berlin an drei unterschiedlichen, angeborenen menschlichen Erkrankungen untersucht. Sie haben herausgefunden, dass Veränderungen insbesondere der äußeren Grenzen der TADs zu erheblichen Störungen bei der Regulation der Gene und damit zu Krankheiten führen können. Die Ergebnisse zeigen, dass für die Entstehung einer Erkrankung nicht nur Veränderungen an kodierenden Genen selbst, sondern aufgrund dieser übergeordneten Struktur des Genoms auch Veränderungen in weit von den jeweiligen Genen entfernt liegenden nicht-kodierenden Regionen verantwortlich sein können.
Die Berliner Forscher konzentrierten sich bei ihren Untersuchungen auf drei unterschiedliche seltene menschliche Erkrankungen der Knochen in Händen und Füßen. Die Brachydaktylie ist eine erblich bedingte Verkürzung der Finger und Zehen. Bei der Polydaktylie kommt es zur Bildung zusätzlicher Finger und bei der Syndaktylie zum Zusammenwachsen mehrerer Finger oder Zehen. Alle drei Erkrankungen haben genetische Ursachen und entstehen bereits im Laufe der Embryonalentwicklung.
Die Forscher konnten zeigen, dass die drei Erkrankungen durch jeweils unterschiedliche, sogenannte strukturelle Veränderungen des Genoms (Deletion, Duplikation, Inversion) entstehen. Bei einer Deletion fehlt ein größerer Abschnitt des Genoms, bei einer Duplikation kommt es zu einer Verdopplung und bei der Inversion ist ein größerer Genomabschnitt innerhalb der DNA-Sequenz umgedreht. Die gefundenen Veränderungen zerstören die Struktur der TADs in dieser Region, indem sie deren Grenzen verschieben bzw. entfernen.
„Strukturveränderungen des Genoms sind eine häufige Ursache für genetische Erkrankungen. Die Suche nach diesen Veränderungen gehört daher zum diagnostischen Standard bei ihrer Abklärung. Oft sind die gefundenen Veränderungen aber schwierig zu interpretieren und es bleibt dann unklar, ob sie tatsächlich die Ursache der Erkrankung sind“, erklärt Stefan Mundlos, Leiter der Forschungsgruppe am MPIMG, die diese Untersuchungen durchgeführt hat. Deshalb haben die Forscher die genetischen Veränderungen, die bei den menschlichen Erkrankungen gefunden wurden, in das Erbgut von Mäusen übertragen. Sie verwendeten dafür eine von ihnen selbst entwickelte Variante des sogenannten CRISPR/Cas-Verfahrens, welches es erlaubt, in kurzer Zeit gezielt große strukturelle Umbauten im Genom von Mäusen vorzunehmen. „Unsere Ergebnisse belegen, dass die Veränderungen im Erbgut der Grund für die Erkrankungen beim Menschen sind: Die Mäuse mit dem veränderten Genom weisen die gleichen Krankheitssymptome auf wie die betroffenen Menschen.“
Bislang gingen Wissenschaftler davon aus, dass Fehlfunktionen eines Gens entweder in Veränderungen des Gens selbst oder in den Steuerungsfaktoren begründet sein müssen, die die Aktivität des Gens regulieren. Die Ergebnisse der Berliner Forscher zeigen jedoch, dass darüber hinaus auch die Umgebung eines Gen – und zwar über eine Entfernung von bis zu mehreren Millionen Basen hinweg –einen starken Einfluss auf die ordnungsgemäße Funktion des Gens besitzt.
„Man kann sich die DNA als langen Faden vorstellen, der durch Mauern in unterschiedliche Abschnitte bzw. TADs unterteilt ist“, erläutert Mundlos. „Innerhalb eines Abschnittes können alle Elemente – Gen, Regulator, Transkriptionsfaktoren, Polymerasen und viele andere – frei miteinander interagieren. Die Mauern begrenzen diese Bereiche und schirmen sie von benachbarten Aktivitäten ab. Durch strukturelle Veränderungen können einzelne Mauern jedoch entfallen oder an eine andere Stelle versetzt werden. Dadurch verändert sich die Zusammensetzung der TAD und auf einmal können Elemente miteinander agieren, die zuvor streng voneinander getrennt waren. Als Folge können Gene falsch reguliert werden und zum Beispiel die von uns untersuchten Fehlbildungen verursachen.“ Aus den Ergebnissen der Berliner Forscher lässt sich daher ein grundsätzlich neues Verständnis dafür ableiten, über welche Mechanismen Veränderungen im Genom Krankheiten verursachen können.
Die Forschungsgruppe von Stefan Mundlos wird von einer privaten Förderin der Max-Planck-Förderstiftung im Rahmen des Projektes „Moderne Verfahren der Genomanalyse bei seltenen Erkrankungen“ unterstützt.
Originalveröffentlichung
Darío G. Lupiáñez et al.; Disruptions of Topological Chromatin Domains Cause Pathogenic Rewiring of Gene-Enhancer Interactions; Cell, May 7, 2015