Supermikroskop ermöglicht Einblick in Energiehaushalt der Zelle
Technische Tricks lassen Details im Inneren von Zellen beobachten
Objekte, die kleiner sind als die Wellenlänge des Lichts kann man mit Lichtmikroskopen nicht sehen – zumindest dachte man das lange. Mittlerweile wurden aber besondere Tricks entwickelt, um diese Regel zu umgehen. An der TU Wien gelang es mit Hilfe eines Superauflösungs-Mikroskops, die Anordnung von Proteinen mit einer Genauigkeit im Bereich von etwa 30 Nanometern zu untersuchen. Gemeinsam mit der Universität für Veterinärmedizin in Wien konnten damit wichtige Details über das Arbeitsweise von Mitochondrien entschlüsselt werden, die in unseren Zellen für die nötige Energie sorgen.
Viele Lichtpunkte ergeben ein Bild
„Proteine lassen sich mit fluoreszierenden Molekülen spezifisch markieren. Mit Hilfe von Laserlicht kann man sie dann zum Leuchten bringen“, erklärt Prof. Gerhard Schütz vom Institut für angewandte Physik der TU Wien. Würden alle Proteine gleichzeitig fluoreszieren, würden sich die jeweiligen Flecken überlagern und ein verschwommenes, undeutliches Bild ergeben.
Der Trick besteht nun darin, dass die Farbstoffmoleküle zwischen zwei Zuständen hin und her wechseln: Meistens befinden sie sich im Dunkelzustand, doch manchmal wechseln sie ganz zufällig in einen aktiven Zustand und fluoreszieren. Nimmt man nun Bilder einer winzigen biologischen Struktur auf, so sieht man auf jedem Foto bloß einzelne helle Flecken – die meisten Moleküle senden gerade kein Licht aus. In einem Film hingegen sieht man die einzelnen Moleküle nacheinander aufleuchten und wieder verschwinden. Man kann also mit der Zeit alle markierten Proteine getrennt voneinander beobachten.
Jedes fluoreszierende Protein wird als heller Fleck sichtbar. Am Computer kann man das genaue Zentrum dieses Flecks ermitteln und daraus sehr exakt den Aufenthaltsort des jeweiligen Proteins bestimmen. Aus tausenden Bildern wird dann die Gesamtstruktur zusammengesetzt, und so entsteht ein Bild mit einer Auflösung von ungefähr 30 Nanometern – obwohl das verwendete Licht eine Wellenlänge von etwa 500-700 Nanometern aufweist.
Mit diesem Trick untersuchte das Team von Gerhard Schütz an der TU Wien gemeinsam mit der Forschungsgruppe von Prof. Elena Pohl (Veterinärmedizinische Universität Wien) die Proteinverteilung in Mitochondrien. Mitochondrien sind für jede Zelle lebenswichtig. Sie sorgen dafür, dass Adenosintriphosphat (ATP) hergestellt wird – der universelle Energieträger in unseren Zellen.
Konkurrenz um Energie
Das Mitochondrium hat eine glatte Außenmembran, unter der sich eine schlingenartig aufgefächerte Innenmembran verbirgt. „An den Einstülpungen der verschlungenen Membran findet ein ganz wichtiger Prozess der zellulären Energiegewinnung statt, die sogenannte Atmungskette“, erklärt Gerhard Schütz. „Dabei transportieren mehrere Proteinkomplexe Protonen über die Innenmembran und bauen damit eine elektrische Spannung auf. Diese elektrische Spannung nutzen bestimmte Proteine, um ATP zu erzeugen.“. Allerdings haben die ATP-erzeugenden Proteine dabei einige Gegenspieler: Uncoupling Proteine können durch durch eine Art Kurzschluss die elektrischen Ladungsunterschiede ausgleichen.
Nach so einem Kurzschluss kann die Energie, die in der elektrischen Ladungsverteilung gespeichert war, nicht mehr zur Produktion von ATP verwendet werden. Stattdessen entsteht Wärme. Auch dieser Effekt hat eine wichtige biologische Funktion: Zum Beispiel bei Tieren, die Winterschlaf halten, kann dadurch die zelluläre Wärmeproduktion reguliert werden.
„Wir haben uns die Frage gestellt, wie die Balance zwischen diesen beiden Effekten – der ATP-Produktion und der Wärmeerzeugung – überhaupt funktionieren kann“, sagt Gerhard Schütz. „Über die Details dieser Abläufe wusste man bisher recht wenig.“
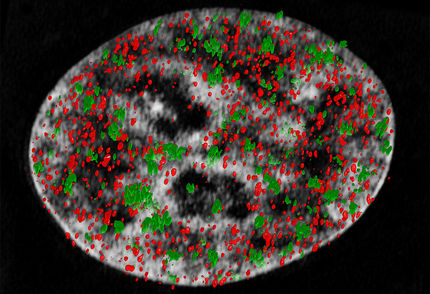
Die Supermikroskopie allerdings konnte nun endlich Licht in diese Angelegenheit bringen: Man fand heraus, dass beide Proteine (die ATP-erzeugende Synthase und das Kurzschluss-verursachende UCP4) an unterschiedlichen Stellen im Mitochondrium aktiv sind. Im Inneren der Schlingen der Mitochondrien-Wand entsteht ATP, weiter außen ist UCP4 aktiv. So lässt sich nun verstehen, warum die Konkurrenz der beiden Effekte für unsere Zellen kein Problem ist.
„Noch gibt es hier viel zu forschen. Wir können noch nicht genau sagen, wozu das Mitochondrium UPC4 an der Membran benötigt“, sagt Gerhard Schütz. „Eine mögliche Erklärung wäre, dass es Protonen davon abhält, aus dem Mitochondrium auszutreten und andere Teile der Zelle zu schädigen.“ Solchen Fragen will das Forschungsteam mit Hilfe der Supermikroskopie noch weiter nachgehen.