Auf dem Zuckerweg in die Zelle
Freiburger Forscher bauen Bakterienproteine nach, die Stoffe über die Zellmembran einschleusen können
Anzeigen
Auf welche Weise Bakterien den Schutz der Außenmembran überwinden, um in Zellen des Körpers zu gelangen, erforscht Juniorprofessor Dr. Winfried Römer mit seinem Mitarbeiter Kevin Tröndle und seiner Mitarbeiterin Dr. Julie Claudinon vom Institut für Biologie II, Mitglieder des Exzellenzclusters BIOSS Centre for Biological Signalling Studies der Universität Freiburg. Seine Erkenntnisse nutzt er, um Medikamente über den gleichen Weg in Zellen einzuschleusen, damit diese dort wirken können. Nun ist es ihm gelungen, eine modifizierbare Version eines Bakterienproteins zu erstellen, das in Zukunft als Transportmittel in die Zelle dienen könnte. Er erkannte außerdem, dass die genaue Geometrie des synthetischen Bakterienstoffs beim Erkennen des zellulären Rezeptors und beim Einschleusen in die Zelle eine Rolle spielt.
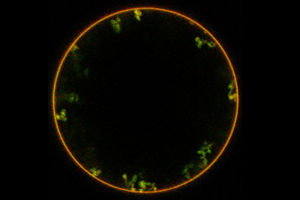
Die Forscher zeigten im Versuch mit synthetischen Vesikeln (rot), dass Neolektin (grün) die Membran dazu bringt, Einstülpungen zu bilden. Auf diesem Weg wäre es möglich, Stoffe mithilfe von Neolektin in Zellen zu transportieren.
Winfried Römer
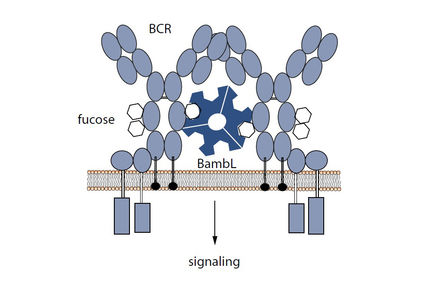
Lektine sind Proteine, die unter anderem von Bakterien gebildet werden. Sie binden an Zuckern, die auf Signalproteinen an der Oberfläche der Wirtszelle verteilt sind. Damit aktivieren sie eine Signalkaskade in der Zelle. Die Außenmembran stülpt sich daraufhin ein, um das Protein zu umhüllen und es ins Innere zu transportieren. Bakterien nutzen diesen Prozess, die Endozytose, und dringen so in Körperzellen ein, um sich zu vermehren. Römer entwickelte nun in Zusammenarbeit mit Dr. Anne Imberty von der Universität Grenoble/Frankreich solche Proteine. Diese „Neolektine“ binden, ähnlich wie Lektine, an die Zuckerreste der Zelle. Zum ersten Mal waren die Forscherinnen und Forscher mit den synthetischen Proteinen in der Lage, die Anzahl der Bindungen für Zucker gezielt zu variieren. „Die Neolektine können wir so designen und optimieren, dass sie als Werkzeuge in der Grundlagenforschung, der gezielten Medikamentenaufnahme und der Früherkennung von Tumorzellen zum Einsatz kommen“, erklärt Römer. D
Die Wissenschaftlerinnen und Wissenschaftler erstellten die Proteine, indem sie veränderte Lektin-Gene in Bakterien einfügten. Die Mikroorganismen produzierten anschließend die Neolektine. So bauten die Wissenschaftler 13 Proteine, die sich in ihrer Architektur vom Original auf den ersten Blick nicht unterscheiden. Die Forscher veränderten aber die Anzahl und die Distanz zwischen den Bindungsstellen für Zucker. Diese zwei Faktoren erwiesen sich im Experiment als kritisch für die Aufnahme und Wirkung der Neolektine. Die Wissenschaftler testeten die Proteine im Labor zuerst auf Oberflächen, an denen Zucker gebunden war. Zusätzlich erforschten sie die Neolektine an großen synthetischen Vesikeln, Blasen aus Fettsäuren, auch Liposome genannt, die Zellmembranen simulieren sollen. In allen Versuchen fanden sie Neolektine, die besonders gut binden konnten. Die Forscher erkannten: Damit sich die Zellmembran einstülpt, braucht es die richtige räumliche Nähe der Zuckerbindungstaschen. Doch auch die Anzahl der Bindungen spielt eine wichtige Rolle: Mindestens zwei sind notwendig, damit das Neolektin schnell in die Zelle aufgenommen wird.