Piraten gegen multiresistente Keime
Einsatz von Bakteriophagen als neue Strategie im Kampf gegen den multiresistenten Keim Achromobacter xylosoxidans
Infektionen durch den oft multiresistenten Keim Achromobacter xylosoxidans werden immer häufiger beschrieben. Der opportunistische Erreger spielt u.a. eine Rolle bei der bisher unheilbaren Stoffwechselkrankheit Mukoviszidose. Bakteriophagen (kurz: Phagen) wären als die natürlichen Feinde der Bakterien eine naheliegende Alternative, um Infektionen, besonders mit „Krankenhauskeimen“, wirksam zu bekämpfen. Dr. Johannes Wittmann, Forscher am Leibniz-Institut DSMZ-Deutsche Sammlung von Mikroorganismen in Braunschweig, isolierte verschiedene Phagen gegen das Bakterium und analysierte sie eingehend. Es ist die erste Studie, die eine große Anzahl und Diversität von Phagen zusammenstellt, die möglicherweise gegen den Keim Achromobacter xylosoxidans einsetzbar sind. Weitere Untersuchungen folgen, um ihr Potenzial als Therapiephagen zu prüfen. Die Ergebnisse wurden gerade in den wissenschaftlichen Journalen PLOS One und Virology Journal veröffentlicht.
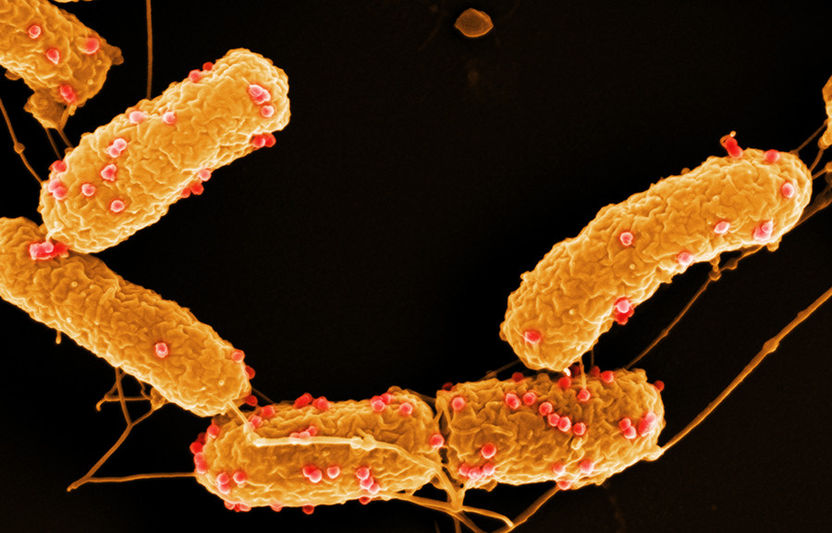
Anheftung von JWAlpha-Phagen an Achromobacter-Bakterien DSM 11852. (Elektronenmikroskopische Aufnahme. Die Probe wurde 5 Minuten nach der Phagenapplikation genommen. Die Phagen sind rot gefärbt.
HZI (M.Rohde), DSMZ (J.Wittmann)
Viren, die Bakterien befallen, werden als Bakteriophagen bezeichnet. Sie rücken zunehmend in den Fokus des wissenschaftlichen Interesses. Dies hat ganz praktische Gründe: In Zeiten, in denen Antibiotika zur Bekämpfung multiresistenter bakterieller Infektionserreger erschreckend wirkungslos werden, gewinnen die natürlichen Feinde der Bakterien neue Bedeutung. Hier setzt die aktuelle Grundlagenforschung an der DSMZ im Team um Dr. Johannes Wittmann und Dr. Christine Rohde an.
„Wie der Name Bakteriophagen, aus dem griechischen „phagos“ abgeleitet, verrät, „fressen“ diese Viren Bakterien und vernichten sie damit“, erklärt Dr. Johannes Wittmann, Postdoc an der DSMZ. „Die Phagen nutzen dazu ein ausgeklügeltes System. Sie injizieren ihre Erbsubstanz in die Bakterienzelle, die von der Proteinmaschinerie der Bakterien abgelesen wird.
Durch diese Umprogrammierung übernehmen die Phagen, wie „Mikropiraten“, das Kommando in der Bakterienzelle. Es entsteht eine Vielzahl neuer Phagen. Die Wirtszelle platzt und entlässt hunderte dieser Viren, die weitere Bakterien vernichten können.“
Neue Strategie im Kampf gegen multiresistente Keime
Das effektive Wirkprinzip der Phagen und ihre Unschädlichkeit gegenüber dem menschlichen Organismus könnten sie zu einem Mittel im Kampf gegen verschiedene multiresistente Infektionserreger machen. „Phagen sind zur Bekämpfung von Pathogenen besonders geeignet, da sie spezifisch für jeweils eine Wirtsbakterienart sind“, so Johannes Wittmann. „Sie sind quasi ein „intelligentes“, selbstlimitierendes Medikament und vermehren sich nur am Ort der bakteriellen Infektion und nur bis alle Wirtsbakterien verbraucht sind.“
Im Fokus der ersten breit angelegten wissenschaftlichen Phagen-Studie der DSMZ steht der bisher nur unzureichend erforschte opportunistische Infektionserreger Achromobacter xylosoxidans, ein bewegliches Gram-negatives Stäbchen. Der Keim ist weit verbreitet in der natürlichen Umwelt, im Boden oder verschiedenen Wasserquellen. Er kann aber auch schwere Infektionen bei immunsupprimierten Menschen, wie Endokarditis, Bakteriämie oder Meningitis verursachen.
„Im medizinischen Bereich spielt der häufig multiresistente Erreger Achromobacter eine nicht zu vernachlässigende Rolle bei der Mukoviszidose, einer tragischen, bisher unheilbaren Stoffwechselkrankheit“, informiert Johannes Wittmann. „Der Keim ist dort oft einer unter mehreren, die in der erkrankten Lunge meist Biofilme bilden. Biofilme sind durch Phagen besser erreichbar als durch Antibiotika. Gerade die opportunistisch pathogenen Keime bereiten im Krankenhaus große Sorgen. Für das Projekt standen wir deshalb auch in fachlichem Austausch mit der Charité in Berlin.“
„Wir verzeichnen besonders in den letzten Jahren eine Zunahme der Patienten mit opportunistischen Infekten“, berichtet dazu Univ.- Prof. Dr. Martin Witzenrath von der Medizinischen Klinik mit Schwerpunkt Infektiologie und Pneumologie der Charité - Universitätsmedizin Berlin. „In diesem Zusammenhang stellen uns Erreger mit Resistenzen gegen gängige Antibiotika, wie Penicillin, Makrolide oder Cephalosporine vor große Herausforderungen in der Therapie der Patienten. Klinisch macht uns auch Achromobacter Probleme, besonders bei Patienten mit Mukoviszidose. Es steht zu befürchten, dass wir zukünftig noch häufiger mit ihm konfrontiert werden. Dies zeigt den dringenden Bedarf an neuen Alternativen, um antibiotikaresistente Pathogene zu bekämpfen. Die vorliegende Studie von Dr. Wittmann ist ein wichtiges Exempel für eine neue Alternativstrategie.“
Neue Phagen gegen Achromobacter
„Phagen lassen sich am einfachsten dort aufspüren, wo auch die vermuteten Keime zu finden sind, z. B. in Abwässern. Wir konnten die Phagen, die wirksam gegen Achromobacter sind, gut aus Klärwässern der Stadtwerke isolieren. Für das Screening wurden die Klärwerks-Filtrate mit den Wirtsbakterien inkubiert“, erzählt Johannes Wittmann. „Anhand der Löcher im Bakterienrasen auf den Agarplatten sind passende Phagen bald erkennbar.“
Als Wirtsbakterien wurden über 60 verschiedene Stämme der Gattung Achromobacter mit einer hohen mikrobiologischen Vielfalt eingesetzt. Sie stammten aus der Sammlung der DSMZ und anderen Kulturensammlungen in Schweden, der Tschechischen Republik, Belgien und Kanada. Die Stämme wurden meist aus klinischen Proben wie Sputum, Blut, Urin sowie aus der Umwelt isoliert und wiesen durchweg eine Vielzahl von Resistenzen gegen die in Kliniken eingesetzten Antibiotika auf.
Insgesamt 34 Phagen konnten isoliert und charakterisiert werden. Zum Teil wurde ihre Erbsubstanz in der DSMZ bereits entschlüsselt. „Dabei war sehr überraschend, dass wir zwei Vertreter in die seltene Phagenfamilie „N4-like“ einordnen konnten“, so Wittmann.
„Um die gegen Achromobacter wirksamen Phagen jetzt auch auf ihren Einsatz als Therapiephagen zu überprüfen und in die Sammlung der Therapiephagen der DSMZ zu integrieren, müssen noch weitere Studien erfolgen“, informiert Dr. Christine Rohde, Leiterin der AG. „Dazu gehört die vollständige Sequenzierung des Phagengenoms, um Gene auszuschließen, die für unerwünschte Eigenschaften kodieren.“
Originalveröffentlichung
J. Wittmann et al.: Isolation and Characterization of Numerous Novel Phages Targeting Diverse Strains of the Ubiquitous and Opportunistic Pathogen Achromobacter xylosoxidans. PLOSone (2014)
J. Wittmann et.al : First genome sequences of Achromobacter phages reveal new members of the N4 family. Virology Journal 2014