Wächter schließen Grippe-Viren aus
Anzeigen
Die Grippe-Saison 2014 hat recht ruhig begonnen. Nachgewiesen wurde bislang laut Robert-Koch-Institut meist eine Influenza vom Typ A (H3N2). Der diesjährige Grippe-Impfstoff erfasst diesen Typ. Wer ungeimpft eine Grippe erwischt, dem kann die Medizin derzeit nur begrenzt helfen. Denn Grippeviren verändern ihr Erbgut und damit ihre Oberfläche rasend schnell, so dass Medikamente rasch unwirksam werden. Berliner Wissenschaftler gehen deshalb einen völlig neuen Weg. Sie greifen nicht mehr das Virus selbst an, sondern wollen ihm den Weg in die Wirtszelle versperren. Ohne Wirtszelle jedoch können sich Viren nicht vermehren.
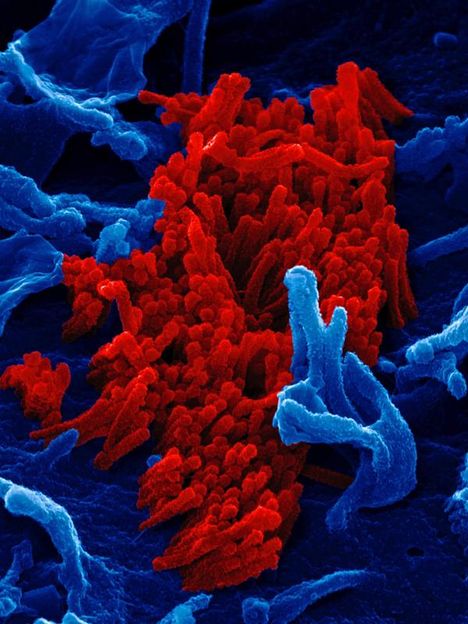
Wissenschaftler haben neue Wirtszellfaktoren identifiziert, die für Influenza-A-Infektionen unerlässlich sind. Das Bild zeigt Viren der Schweinegrippe (H1N1).
Max-Planck-Institut für Infektionsbiologie / Volker Brinkmann
„Ein Virus ist ja im Grunde kein lebender Organismus, sondern eine Software mit Verpackung“, erläutert Dr. Jens von Kries vom Leibniz-Institut für Molekulare Pharmakologie (FMP) in Berlin-Buch. „Dieses Programm zwingt, sobald es in der Zelle angelangt ist, die Zelle dazu, unzählige Kopien des Virus zu produzieren. Dabei stirbt die Zelle am Schluss und entlässt Tausende oder Millionen neuer Viren in die Blutbahn.“ Grippeviren seien zudem darauf programmiert, sich extrem fehlerhaft zu vermehren. Und nicht nur das, sie können ihr Erbgut mit anderen Influenza-Typen ständig neu vermischen. Das menschliche Immunsystem muss deshalb immer wieder neu passgenaue Antikörper produzieren.
Die echte Virus-Grippe Influenza ist bis heute eine der gefährlichsten Infektionen. Laut Weltgesundheitsorganisation WHO erkranken jährlich zwischen 10 und 20 Prozent der Weltbevölkerung an Grippe. In schweren Grippejahren gibt es allein in Deutschland mehrere Tausend Tote. Und seit langem befürchten Epidemiologen eine verheerende Pandemie wie vor 100 Jahren, als die Spanische Grippe um die Welt raste und knapp 50 Millionen Menschen das Leben kostete.
Die heutigen Impfstoffe bieten eine gewisse Sicherheit, allerdings auch nicht immer. Da sich ständig überraschend neue Varianten bilden, kann es passieren, dass der Impfstoff nicht gut oder im schlimmsten Fall gar nicht wirkt. Diese extrem hohe Mutationsgeschwindigkeit macht auch die Medikamentenentwicklung so schwierig. Die Arbeitsgruppe von Jens von Kries hat sich deshalb auf zwei andere Wege konzentriert. Sie will während der Infektion bestimmte Eiweiße (Proteine) auf oder in der menschlichen Wirtszelle durch Medikamente blockieren, die das Virus unbedingt zum Eindringen oder zur Vermehrung benötigt. „Unsere Zellen sind darauf programmiert, die Erbsubstanz DNA möglichst fehlerfrei zu kopieren, denn Mutationen können zu Krebs führen“, sagt Jens von Kries. „Wenn wir also die seit Urzeiten von Viren genutzten Eintrittspforten in die Zelle verschließen, dann kann das Virus darauf nicht reagieren.“
Das ist ein ambitionierter Plan, der nur mit Kollegen aus verschiedenen internationalen Forschergruppen zu realisieren ist. So hat die Arbeitsgruppe von Professor Thomas F. Meyer, Direktor am Berliner Max-Planck-Institut für Infektionsbiologie, aus 24.000 Genen mittlerweile rund 300 herausgefischt, die die Bauanleitung für Proteine enthalten, die die Viren zu ihrer Vermehrung benötigen. Getestet wurde das mit verschiedenen Influenza-Stämmen, darunter das hochgefährliche Vogelgrippevirus H5N1. „Zwar mag uns das Ausschalten menschlicher Genfunktionen auf den ersten Blick als problematisch erscheinen“, sagt Meyer. „Es handelt sich aber um genau dasselbe therapeutische Prinzip, das wir seit Jahrzehnten zur medikamentösen Behandlung sonstiger Erkrankungen von lästigen Kopfschmerzen bis hin zu Krebs erfolgreich heranziehen. Also warum nicht auch für die Therapie von Infektionskrankheiten?“ Denn nur wenn bestimmte Faktoren eines Erregers mit denen des Wirts genau passen, komme es tatsächlich zu einer Ansteckung. Viren benötigten Hunderte von Faktoren der menschlichen Zelle. Deshalb, so Meyer, sollte es möglich sein, durch die Blockade von Wirtsfaktoren eine Infektion erfolgreich zu unterbinden. Auch für andere Infektionskrankheiten könne sich dieser Weg als wichtig herausstellen, denn immer mehr Bakterienstämme erweisen sich als resistent gegen Antibiotika. Meyer koordiniert das von der EU geförderte Projekt „ANTIFLU“.
Mit der von Jens von Kries geleiteten Screening Unit am Leibniz-Institut für Molekulare Pharmakologie wurden bislang Tausende Substanzen auf ihre Eignung getestet, die von den Max-Planck-Forschern ausgewählten Proteine zu blockieren. Diese Wirkstoffe für mögliche Therapien werden anschließend an der israelischen Hebrew University in Jerusalem kristallisiert und so optimiert, dass sie die Eiweiße noch besser blockieren. An mit Grippe infizierten Zellen und später Mäusen testet die Max-Planck-Gruppe anschließend diese Substanzen auf Wirksamkeit.
Eine weitere Eintrittspforte von Viren in die Zelle erforscht derzeit Professor Volker Haucke, der Direktor des Leibniz-Instituts für Molekulare Pharmakologie. Er und seine Kollegen am amerikanischen National Institute of Health sowie am Deutschen Krebsforschungszentrum konnten zeigen, dass manche Viren so wie beispielsweise das Immunschwächevirus HIV, das von Zecken übertragene Krim-Kongo-Fiebervirus oder eben Grippeviren winzige zelluläre Transportvesikel benutzen, um in das Zellinnere zu gelangen. Haucke hat Hemmstoffe identifiziert, die das Einschleusen von Viren durch diesen Aufnahmeweg verhindern. Diese kleinen Moleküle nennt er Pitstops. „Künftige Generationen von Pitstops und ähnlichen Molekülen“, so erläutert Volker Haucke, „könnten ein weiterer neuer therapeutischer Ansatz nicht nur für virale und bakterielle Infektionen sein, sondern auch zur Behandlung von Krebs und neurologischen Erkrankungen dienen.“ Diese Vesikel sind nur einen Zehntelmikrometer kleine Bläschen, die sich von der jede Zelle umhüllenden Zellmembran abschnüren und so Nährstoffe und Signalmoleküle in die Zelle hineintransportieren. In Nervenzellen hängt die Ausschüttung von Botenstoffen, sogenannten Neurotransmittern, von solchen Transportprozessen ab.
„Wir wollen wissen, ob es möglicherweise bereits ausreicht, ein einzelnes Eiweiß in der Zelle zu blockieren, um das Virus zu stoppen“, sagt Jens von Kries. Dies müsse sehr sorgfältig getestet werden, denn es bestehe immer die Gefahr, dass durch die Gabe eines Hemmstoffes, der die Virusaufnahme blockiert, umgekehrt auch die Übertragung von Neurotransmittern in Nervenzellen blockiert wird. „Das Eindringen des Virus erfolgreich verhindert – Patient tot, das wäre keine gute Therapie“, meint Jens von Kries.
Erste Daten zeigen, dass der Ansatz verheißungsvoll ist. Mehrere der identifizierten Substanzen weisen laut FMP-Forscher Jens von Kries einen starken antiviralen Effekt auf. Da sie ausschließlich auf die menschlichen Zellen und nicht auf Viren wirken, sollten sich keine Resistenzen bilden, hoffen die Wissenschaftler. Und völlig neu für antivirale Wirkstoffe wäre es, dass sie auch gegen sich künftig bildende gefährliche Virenstämme weiter wirksam blieben. Bis ein solches Medikament auf den Markt kommen kann, werden allerdings noch viele Jahre vergehen. Bis dahin gilt es, sich rechtzeitig impfen zu lassen und die Hände im Winterhalbjahr häufiger zu waschen.