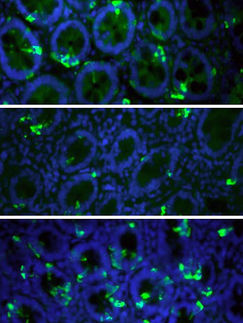
Schilddrüsenzellen aus Stammzellen gewonnen: Endokrinologen fordern dazu weitere Studien
Anzeigen
Forschern aus Belgien und den USA ist es gelungen, aus embryonalen Stammzellen funktionstüchtige Schilddrüsenzellen zu züchten. Die Zellen formierten sich selbstständig zu Schilddrüsengewebe und produzierten im Tierversuch Hormone. Die Deutsche Gesellschaft für Endokrinologie (DGE) betrachtet die Experimente als einen Meilenstein hin zur Entwicklung einer Stammzelltherapie von Schilddrüsenerkrankungen. Vor einer Anwendung beim Menschen müssten allerdings die Effektivität und die Sicherheit in klinischen Studien genau geprüft werden, betont die DGE. Die Bildung der Schilddrüse wird durch die beiden Proteine NKX2-1 und PAX8 gesteuert, die während der Embryonalentwicklung vorübergehend in den Stammzellen gebildet werden. Es handelt sich um Transkriptionsfaktoren, die in der Zelle bestimmen, welche Gene abgelesen werden. Ein Team um Sabine Costagliola von der Université libre de Bruxelles hat diese Entwicklung mit Unterstützung von US-Forschern im Labor an embryonalen Stammzellen nachgestellt. Die Forscher versahen die Stammzellen mit genetischen Schaltern, mit denen sich die Produktion von NKX2-1 und PAX8 an- und wieder ausstellen ließ.
„Eigentlich suchten die Forscher nur eine neue Schilddrüsenzelllinie für weitere Experimente“, berichtet Professor Dr. med. Dr. h. c. Helmut Schatz, Mediensprecher der DGE aus Bochum. „Überraschenderweise formierten sich die Zellen jedoch spontan zu Schilddrüsenfollikeln.“
„Die Follikel sind in der Schilddrüse die Werkstätten für die Hormonproduktion“, erläutert Professor Dr. Dr. med. Dagmar Führer, Vize-Präsidentin der Deutschen Gesellschaft für Endokrinologie und Direktorin der Klinik für Endokrinologie und Stoffwechselerkrankungen am Universitätsklinikum Essen. „Sie sind mikroskopisch kleine Zellkugeln. Die Oberfläche bildet eine Schicht von Deckzellen, die die Hormone herstellen. Sie umgeben einen Innenraum, in dem sowohl das für die Produktion notwendige Jod als auch das Thyreoglobulin, eine Speicherform für die Schilddrüsenhormone, gelagert werden.“
Die von den belgischen Forschern im Labor generierten Zellkugeln sahen nicht nur aus wie Schilddrüsenfollikel. Sie konnten auch von außen durch das die Schilddrüse stimulierende Hormon TSH zur Hormonproduktion angestoßen werden. TSH wird in der Hirnanhangdrüse gebildet. Es ist auch im menschlichen Körper für die Regulierung der Produktion von Schilddrüsenhormonen zuständig. Bei einer Unterfunktion der Schilddrüse steigt im Blut die TSH-Konzentration, bei einer Überfunktion wird die TSH-Bildung gedrosselt oder ganz ausgeschaltet. Mit der Kontrolle durch TSH war eine wichtige Voraussetzung für eine Transplantation geschaffen. Sie vermeide eine schädliche Überproduktion von Schilddrüsenhormonen, die später durch weitere Behandlungen gestoppt werden müsste.
Tatsächlich transplantierten die belgischen Forscher die Follikel anschließend unter die Organkapsel von Mäusenieren und konnten zeigen, dass die Zellen kurze Zeit später begannen, Schilddrüsenhormone zu produzieren. Professor Führer: „Ein künstlich herbeigeführter Ausfall der Schilddrüse konnte bei den Tieren kuriert werden.“ Sofern die Schilddrüse nach einer Erkrankung noch ausreichend durchblutet wird, wäre auch eine Transplantation in die Schilddrüse möglich. Produzieren die Zellen dann wieder Hormone, könnten möglicherweise eines Tages auch Patienten mit einer Unterfunktion der Schilddrüse auf ihre tägliche Einnahme von Hormontabletten verzichten.
Forschungen an embryonalen Stammzellen sind ethisch nicht unproblematisch. Es gibt aber Alternativen, sogenannte induzierte pluripotente Stammzelle (iPS), die aus normalen Zellen gewonnen und dann umprogrammiert werden. „Der nächste Schritt wird darin bestehen, auch iPS zur Bildung von Schilddrüsenfollikeln zu bewegen“, sagt Professor Schatz. Dann wären im Prinzip alle Voraussetzungen für eine Transplantation beim Menschen geschaffen. Dennoch dürfte bis zur ersten Behandlung beim Menschen noch einige Zeit vergehen. „Zunächst muss beispielsweise sichergestellt werden, dass die künstliche Aktivierung der beiden Transkriptionsfaktoren ohne Folgen bleibt“, meint Professor Führer. Umfassende Studien sind also zuvor noch nötig.
Originalveröffentlichung
Francesco Antonica et al: "Generation of functional thyroid from embryonic stem cells."; Nature (2012).