Neuer Krebs-Schalter entdeckt
Biochemiker der Universität Jena klären potenziellen Mechanismus der Krebsentstehung auf
Anzeigen
Jahr für Jahr trifft rund 500.000 Deutsche die Diagnose Krebs. Auch wenn die Chancen auf eine erfolgreiche Therapie für viele von ihnen immer weiter steigen, sind Krebserkrankungen noch immer die zweithäufigste Todesursache hierzulande. „Das Tückische an Tumorerkrankungen ist, dass dabei das Gleichgewicht zwischen Prozessen der Zellerneuerung und dem Absterben von Zellen völlig aus dem Ruder läuft“, erläutert PD Dr. Oliver Krämer von der Friedrich-Schiller-Universität Jena. „Tumorzellen sterben nicht ab, sondern vermehren sich praktisch ungebremst immer weiter“, sagt der Biochemiker vom Centrum für Molekulare Biomedizin (CMB). Krämers Arbeitsgruppe am Lehrstuhl für Biochemie von Prof. Dr. Thorsten Heinzel, dem Forschungsprorektor der Jenaer Universität, arbeitet intensiv daran, die molekularen Mechanismen aufzuklären, die zur Entstehung von Tumorzellen führen können.
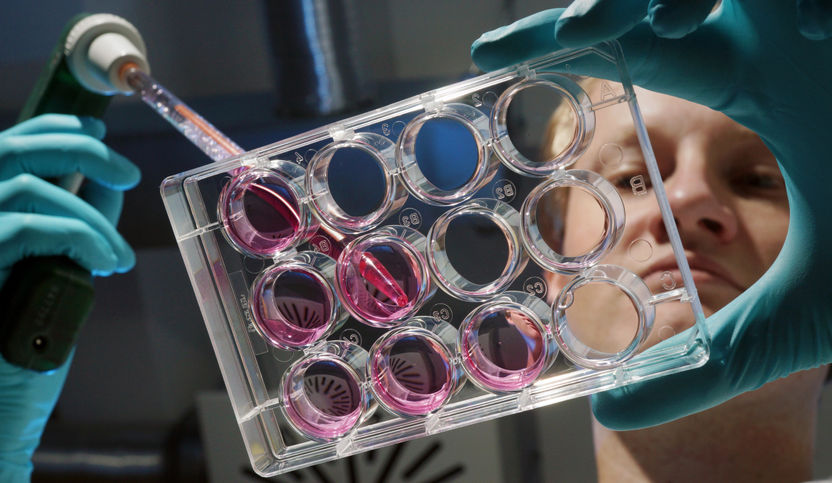
Doktorand Tobias Wagner untersucht in einem Zellkulturlabor der Uni Jena, welche Rolle das Enzym "Histon Deacetylase 2" bei der Entstehung von Tumorzellen spielt
Fotos: Jan-Peter Kasper/FSU
Wie die Jenaer Forscher in der aktuellen Ausgabe der internationalen Fachzeitschrift „Journal of Molecular Cell Biology“ berichten, haben sie jetzt nicht nur einen potenziellen molekularen Mechanismus der Krebsentstehung entschlüsselt, sondern damit auch einen möglichen Ansatzpunkt für die Krebstherapie identifiziert. Die Herausgeber der Zeitschrift würdigen den Aufsatz der Forscher der Uni Jena zudem in besonderer Weise: Er wurde als Titelgeschichte der Printausgabe der Zeitschrift ausgewählt und zusätzlich im Editorial erwähnt.
In ihren aktuellen Untersuchungen haben sich die Forscher auf die Rolle eines Enzyms mit dem Namen „Histon Deacetylase 2“, kurz HDAC2, konzentriert. Dieses kommt in allen menschlichen Zellen vor und hat normalerweise eine wichtige Funktion innerhalb des Zellwachstums. „In Tumorzellen liegt dieses Enzym in stark erhöhten Konzentrationen vor“, sagt Doktorand Tobias Wagner. „Die Vermutung lag daher nahe, dass HDAC2, alleine oder zusammen mit anderen Faktoren, das unkontrollierte Wachstum von Tumorzellen begünstigt“, ergänzt André Brandl, der ebenfalls als Doktorand in Krämers und Heinzels Team an der Studie beteiligt war. Wie die beiden Nachwuchsforscher nun in mehreren Zellkulturmodellen nachweisen konnten, ist HDAC2 nur dann in der Lage seine Funktion innerhalb der Zelle richtig auszuüben, wenn es selbst mit einem Markerprotein namens SUMO versehen ist.
Diese nachträgliche Modifizierung ist es auch, durch die HDAC2 das Tumorwachstum fördert: Sie ermöglicht es dem Enzym an das sogenannte Tumorsuppressor-Protein „p53“ zu binden und bei diesem die funktionell wichtige Acetylierung zu unterbinden. „p53 schützt Zellen normalerweise vor einer Entartung zu Krebszellen, indem es deren Wachstum und Überleben begrenzt“, erläutert Tobias Wagner. Kommt es etwa durch äußere Einflüsse zu Schäden an der DNA (ein potenzieller Auslöser für die Krebsentstehung), so sorgt p53 dafür, dass DNA-Reparaturmechanismen in Gang gesetzt werden oder – falls die Schäden zu gravierend sind – dass die Zelle in den programmierten Zelltod geführt wird. „Durch die Bindung von HDAC2 an p53 wird diese wichtige Funktion von p53 aber gehemmt“, so André Brandl. Die Folge: Die Tumorzellen können ungebremst weiter wachsen.
Das Ausschalten von p53 ist auch der Grund, warum Tumorzellen mit erhöhtem HDAC2-Spiegel nicht mehr auf gängige Chemotherapie-Medikamente ansprechen. Die dabei eingesetzten Substanzen wirken gezielt auf die schnell wachsenden Krebszellen und bringen diese normalerweise zum Absterben. „HDAC2 macht die Tumorzellen allerdings gegen eine solche Behandlung resistent“, so das Resümee der Jenaer Forscher. Ließe sich die Modifizierung von HDAC2 unterbinden, so könnten die Zellen möglicherweise wieder für eine Chemotherapeutika-Behandlung sensibilisiert werden.