Ein Krebsgen bremst sich selbst
Würzburger Wissenschaftler decken Rückkopplungsmechanismus auf
Anzeigen
Krebs entsteht, wenn das Gleichgewicht zwischen Zellteilung, -wachstum und -tod gestört ist. Das macht seine Behandlung so schwierig, weil sie nicht radikal, sondern maßvoll sein muss. Es ist, als wolle man einen Brand nicht vollständig löschen, sondern lediglich eindämmen – so dass es im Kamin brennt und sonst nirgends.
Damit der Balanceakt im Körper gelingen kann, muss zunächst klar sein, wie Zellwachstum grundsätzlich reguliert wird. Auf diesem Gebiet ist nun Martin Eilers, Wissenschaftler am Biozentrum der Universität Würzburg eine wichtige Entdeckung gelungen. Seine Gruppe hat in Zusammenarbeit mit einem internationalen Team einen Rückkopplungsmechanismus gefunden, der das bekannte „Krebsgen“ Myc, bzw. das von ihm kodierte Protein, auf die richtige Menge einpegelt. Wie die Fachzeitschrift „Molecular Cell“ berichtet, ist daran eine Proteinkinase namens MK5 entscheidend beteiligt. Der von Eilers publizierte Rückkopplungsweg könnte eine Rolle bei der Entstehung von Darmkrebs spielen. Die Arbeit wurde im Rahmen des EU-Forschungsprojekts Growthstop durchgeführt, das von der Innsbrucker Projektmanagement-Firma CEMIT koordiniert wird.
Myc ist ein Transkriptionsfaktor. Das heißt, es sorgt dafür, dass eine Vielzahl von anderen Genen reguliert wird und treibt auf diese Weise das Wachstum und die Vermehrung von Zellen voran. Gerät Myc außer Kontrolle, entsteht Krebs. Wie aber „merkt“ eine Zelle, dass genügend Myc vorhanden ist? Um diese Frage zu beantworten, haben Eilers und sein Team sogenannte Proteinkinasen untersucht. Proteinkinasen sind Katalysatoren zellulärer Abläufe und haben eine große Bedeutung in der Krebsmedizin. Für viele Krebsarten sind in jüngster Zeit personalisierte Therapien zugelassen, die auf Proteinkinase-Hemmern basieren.
Die Würzburger Wissenschaftler haben die Gesamtheit aller Kinasen, das sogenannte Kinom, mit einem siRNA-Screen nach Hemmstoffen für Myc durchforstet. siRNAs sind kleine RNA-Moleküle, die die Aktivität von Genen herunterfahren, indem sie deren Übersetzung in Proteine blockieren: Sie fangen die dafür nötigen Botenstoffe, die mRNAs, ab. Mit Hilfe von siRNAs haben die Wissenschaftler alle Kinasen einzeln ausgeschaltet und nachgesehen, welchen Einfluss das auf Myc hatte. So identifizierten sie die Myc hemmende Proteinkinase MK5. Eilers und seine Mitarbeiter konnten im Detail aufklären, wie MK5 Myc hemmt, und welche anderen Gene und MikroRNAs daran beteiligt sind.
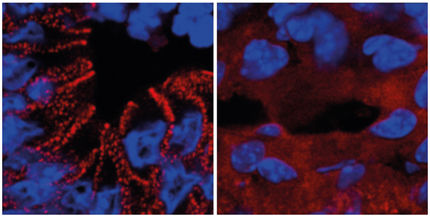
Vor allem aber konnten sie zeigen, dass die Proteinkinase wiederum von Myc aktiviert wird. Hier schließt sich der Rückkopplungs-Kreis: Je mehr Myc da ist, umso mehr wird von dem Hemmstoff für Myc produziert. So bremst Myc sich selbst. Bei einer weiteren Untersuchung stellte sich heraus, dass genau dieser Rückkopplungsmechanismus in Darmkrebszellen außer Kraft gesetzt ist. Hier könnte sich also eine der Ursachen für die Krebsentstehung verbergen – und möglicherweise ein Ansatzpunkt für eine zukünftige Therapieentwicklung.
Originalveröffentlichung
"The MK5/PRAK Kinase and Myc Form a Negative Feedback Loop that Is Disrupted during Colorectal Tumorigenesis", Molecular Cell, Volume 41, Issue 4, 18 February 2011, Pages 445-457