OSCAR detektiert Zellen im Standby-Modus
Mit neuer Fluoreszenzmessungsmethode die Biologie ruhender Stammzellen besser verstehen
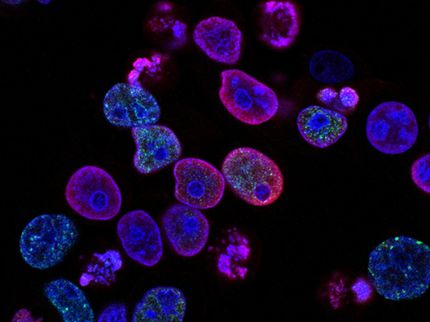
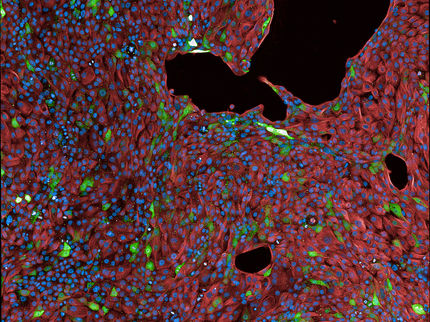
Dormanz ist ein schlafähnlicher Zustand von Zellen, der diese vor genetischen Schäden schützt und so ihr Überleben verlängert. Dieser Zustand ist reversibel und durch eine niedrige Stoffwechselaktivität und Teilungsrate gekennzeichnet. Forscher vom Leibniz-Institut für Alternsforschung (FLI) und der University of Oxford, UK, entwickelten eine Methode, um in Echtzeit Dormanzen nachzuweisen. Mit Hilfe der Fluoreszenzmessung OSCAR (Optical Stem Cell Activity Reporter) konnten im Dünndarm-Modell Zellpopulationen mit unterschiedlichen Dormanz-Werten identifiziert und isoliert werden. OSCAR ist somit ein geeignetes Tool, um die Biologie ruhender Stammzellen besser zu verstehen.
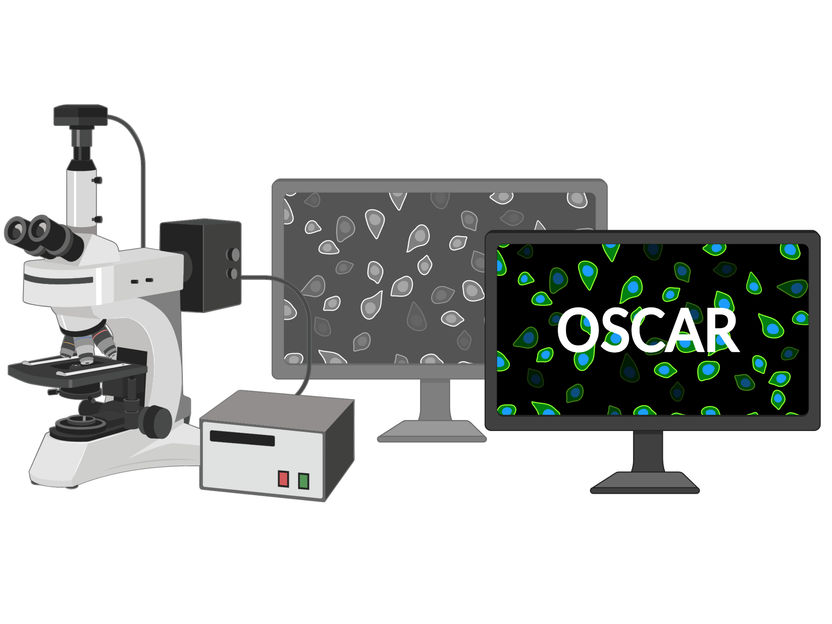
OSCAR (opt. Stem Cell Activity Reporter) kann ruhende Stammzellen im Gewebe nachweisen. Dazu wird ein Peptid in das Rückgrat eines fluoreszierenden Proteins eingebaut. Durch die fehlende Phosphorylierung nimmt in ruhenden Zellen die grüne Fluoreszenz zu.
FLI / Kerstin Wagner & Francesco Neri, created with BioRender.com
Ein wichtiges Beispiel für ruhende Zellen sind somatische Stammzellen, die durch ihr Potenzial zur Differenzierung und Selbsterneuerung gekennzeichnet sind. Sie haben ein hohes Transplantationspotenzial, sind resistenter gegenüber zellulärem Stress und verfügen über ein großes Potenzial, in der regenerativen Medizin eingesetzt zu werden. Hämatopoetische Stammzellen im Knochenmark werden beispielsweise nur bei Verletzungen benötigt und existieren sonst in einem Ruhezustand. In ähnlicher Weise wird bei Krebserkrankungen vermutet, dass ein Rückfall nach einer scheinbar erfolgreichen Therapie, durch die Aktivierung von Langzeit-schlafenden Krebsstammzellen verursacht wird.
Dieser zelluläre Ruhezustand wird als Dormanz bezeichnet. Er ist reversibel und durch eine reduzierte Stoffwechselaktivität, Zellteilung und mRNA-Synthese gekennzeichnet. Dieser schlafähnliche Zustand (Standby-Modus) schützt die Zelle so vor genetischen Schäden, verlängert ihr Überleben und ist entscheidend für die Gewebehomöostase und die zelluläre Reaktion auf Verletzungen oder Transplantationen. Dormante Zellen kommen in zahlreichen Geweben und Organen vor. Ihre Identifizierung, Isolierung und Charakterisierung, unabhängig vom Ursprungsgewebe, ist aber schwierig. Forscher des Leibniz-Instituts für Alternsforschung – Fritz-Lipmann-Institut (FLI) in Jena haben nun in Kooperation mit Partnern der University of Oxford, UK, eine Fluoreszenzmessungsmethode entwickelt, um in Echtzeit in bestimmten Zelltypen dormante Zellen nachweisen und isolieren zu können.
Schwierigkeiten der Detektion von ruhenden Zellen
„Somatische Stammzellen werden für gewöhnlich durch Oberflächenmarker, fluoreszierende Proteine oder über markierungsfähige Zellen identifiziert. Diese Methoden markieren jedoch nur bestimmte Stammzelllinien, gelten nur für eine bestimmte Speziesart und sind technisch sehr anspruchsvoll“, erklärt Dr. Rasmus Freter vom FLI, Erstautor der jüngst in Nature Communications veröffentlichten Studie. „Ein zuverlässiger, spezifischer und vor allem konservierter Marker für ruhende Stammzellen, der ihre Visualisierung und Isolierung ermöglicht, wurde bisher noch nicht gefunden“. Darüber hinaus setzt die Isolierung dieser Zellen mit Hilfe von Oberflächenmarkern ein entsprechendes Vorwissen voraus, was die Charakterisierung bislang unbekannter Stammzellpopulationen von vorn herein ausschließt. Die Jenaer Forscher suchten daher nach einer Methode, um dormante Zellen einfacher nachweisen zu können.
Niedrige RNApII-Ser2-Phosphorylierung ist Merkmal ruhender Stammzellen
„Seit mehr als 10 Jahren ist bekannt, dass ruhende Stammzellen eine geringere Menge an Gesamt-RNA aufweisen“, erläutert Dr. Francesco Neri, Forschungsgruppenleiter am FLI und mittlerweile außerordentlicher Professor an der Universität Turin. mRNA wird von der RNA-Polymerase II (RNApII) umgeschrieben, die phosphoryliert wird, um die mRNA-Transkription zu initiieren. Hohe RNApII-Phosphorylierungen werden in proliferierenden und differenzierten aktiven Zellen nachgewiesen, während die niedrige RNApII-Ser2-Phosphorylierung hochspezifisch für ruhende Zellen ist und diese von anderen Zelltypen unterscheidet.
„Wir untersuchten daraufhin verschiedene Gewebe auf adulte Stammzellen, die niedrige Konzentrationen von RNApII-Ser2-Phosphorylierung aufwiesen“, berichtet Prof. Neri, „und waren so in der Lage, in allen untersuchten Geweben, einschließlich des Gehirns, hämatopoetischen Stammzellen und dem Dünndarm, Zellen ohne eine nachweisbare RNApII-Ser2-Phosphorylierung nachweisen zu können.“
Entwicklung eines fluoreszierenden Kinase-Reporters - OSCAR
„In einem weiteren Schritt nutzten wir diese Beobachtung aus und suchten gezielt nach einem Fluoreszenzreporter, der zwischen Zellen mit hoher oder niedriger RNApII-pSer2-Kinase-Aktivität unterscheiden kann, um ein Werkzeug zur Identifizierung und Isolierung lebender ruhender Zellen aus jedem Gewebe entwickeln zu können“, erläutert Dr. Rasmus Freter das weitere Vorgehen.
Das gelang den Forschern mit einem ratiometrischen, fluoreszierenden optischen Stem Cell Activity Reporter, genannt OSCAR, der darauf basiert, dass die Phosphorylierung von RNApII in ruhenden Stammzellen verschiedener Abstammungslinien weitgehend fehlt. „Die korrekte Visualisierung der Kinase-Aktivität in lebenden Zellen stellt seit langem eine große Herausforderung dar“, betont Dr. Freter. „Die meisten Kinase-Reporter nutzen beispielsweise die FRET-Technologie, die jedoch technisch anspruchsvoll und äußerst anfällig für hohe Hintergrundsignale ist. Darüber hinaus liegen die dynamischen Bereiche für das Signal-Rausch-Verhältnis bei etwa 20-30%, was für die Isolierung von Zellen durch Fluoreszenz-aktivierte Zellsortierung, FACS, viel zu niedrig ist“.
Um diese technischen Barrieren zu überwinden und ein empfindliches, aber auch praktikables Werkzeug zu entwickeln, entwarfen die Forscher um Prof. Neri einen genetisch kodierten Kinase-Reporter der relevanten RNApII-Ser2-Kinase. Sie bauten ein kurzes Peptid, das eine spezifische Phosphorylierungs-Akzeptorstelle enthält, in das Rückgrat eines fluoreszierenden Proteins ein. „In diesem Zusammenhang hatte das Einfügen eines unphosphorylierten Peptids keinen Einfluss auf die Fluoreszenzleistung, während die Phosphorylierung des eingefügten Peptids die Fluoreszenz reduzierte. Folglich zeigt eine hohe Fluoreszenz eine niedrige Kinaseaktivität positiv an und markiert somit ruhende, RNApII-pSer2-niedrige Zellen", berichtet Prof. Neri. Die Massenspektrometrie-Analyse bestätigte die Spezifität der Phosphorylierung.
Der als „OSCAR“ bezeichnet Kinase-Reporter hat im Vergleich zu bisherigen FRET-basierten Systemen einen deutlich verbesserten dynamischen Bereich und kann so auch für die FACS-Sortierung von ruhenden Darmzellen und die Zeitraffer-Mikroskopie verwendet werden. Unter Verwendung der Dünndarmkrypta als Modell, konnte z.B. mit OSCAR in Echtzeit die Dynamik der Dormanzinduktion und der zellulären Differenzierung in vitro detektiert werden. Darüber hinaus gelang mit OSCAR die Identifizierung und Isolierung mehrerer Populationen verschiedener OSCAR-Zustände - von hoch zu niedrig - im lebenden Organismus (in vivo).
Bisher konnten keine toxischen Effekte der OSCAR-Expression in Säugetierzellen und Mäusen festgestellt werden. „Wir gehen daher davon aus, dass sich OSCAR als ein nützliches Werkzeug bei der Charakterisierung ruhender Zellen sowohl in vitro als auch in vivo erweisen könnte“, fasst Prof. Neri die Studienergebnisse zusammen. OSCAR ist somit nicht nur ein geeignetes Tool, um die Biologie ruhender Stammzellen besser zu verstehen. Möglicherweise lassen sich mit dieser neuen Methode auch mutmaßlich schlafende Krebsstammzellen in einer lebenden Zellpopulation leichter detektieren und so frühzeitig entfernen.