Transport nach einfachen Regeln
Max-Planck-Forscher entschlüsseln, wie Zellen die räumliche Verteilung von Proteinen aufrecht erhalten
Anzeigen
Alles Leben auf der Erde ist von Unordnung bedroht. In dieser Hinsicht gleicht eine Zelle einem Schiff, das in einem Meer von Unordnung zu sinken droht: Deshalb muss sie ständig unter Energieaufwand ihren Ordnungsgrad bewahren, um nicht unterzugehen - bildlich gesprochen muss das eindringende Wasser der Unordnung also permanent ausgepumpt werden. Wissenschaftler des Max-Planck-Instituts für molekulare Physiologie in Dortmund haben nun herausgefunden, wie Zellen die korrekte Verteilung von Proteinen in ihrem Innern sicherstellen. Demnach werden viele Proteine, die zur Zellmembran transportiert werden sollen, mit einem Fettsäureanker versehen, der sie in der Zellmembran verankert. Da sie von dort jedoch auch in die Membranen von Zellorganellen gelangen, wird der Anker von diesen Proteinen nach kurzer Zeit wieder entfernt.
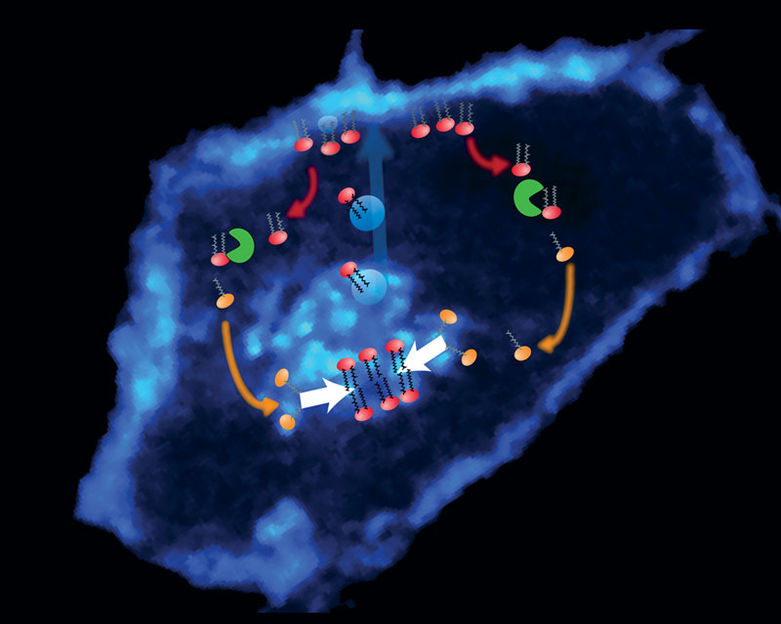
Aufnahme der räumlichen Verteilung von Ras (blau fluoreszierend), das in der Zellmembran (Rand) und im Golgi-Apparat (Zentrum) gehäuft vorkommt. Die Fotomontage zeigt, wie das Verteilungsmuster von Ras im Gleichgewicht gehalten wird: Das mit Fettsäure-Ankern versehene Ras (rot) wird vom Golgi-Apparat in Membranbläschen (blaue Kreise) zur Zellmembran transportiert. Das Enzym APT1 (grün) entfernt den Palmitoylierungsanker von Ras-Molekülen, die von der Zellmembran in andere Membranen gelangt sind. Das depalmitoylierte Ras (orange) kann nun wieder frei in der Zelle schwimmen und in den Golgi-Apparat aufgenommen werden. Der Zyklus beginnt daraufhin von neuem. Zellen nutzen also ein einfaches Prinzip, um Ras und andere palmitoylierte Proteine an ihren Bestimmungsort zu schaffen:ein lokalisiertes Verteilerzentrum (Golgi), gerichteter Transport zum Zielort sowie eine universelle Entfernung der Zielmarkierung (Depalmitoylierung) mit anschließender Wiedereinspeisung in den Transportzyklus.
Philippe Bastiaens
Dieses Leck stopft die Zelle im Gegensatz zum Transport zur Membran also unspezifisch. Die Forscher haben damit ein einfaches Prinzip offengelegt, nach dem Zellen die komplexe räumliche Verteilung von Proteinen steuern und damit einen hohen Ordnungszustand beibehalten. Die Ergebnisse eröffnen zudem möglicherweise neue Wege in der Krebstherapie. Denn in einer weiteren Studie konnten die Wissenschaftler die räumliche Verteilung des Krebsproteins Ras mit einem neuen Hemmstoff erfolgreich durcheinander bringen und so dessen Funktion stören.
Innerhalb einer Zelle müssen eine Vielzahl von Stoffen transportiert werden. Als Rangierbahnhof dient dabei der so genannte Golgi-Apparat. Im Inneren dieses von einer eigenen Membran umgebenen Organells werden Proteine und andere Substanzen funktions- und transportklar gemacht. Aus seiner Membran werden kleine Bläschen (Vesikel) abgeschnürt und zu ihren jeweiligen Zielorten dirigiert. Viele Proteine, die zur Zellmembran transportiert werden sollen, werden dazu mit einem Fettsäure-Molekül versehen. Durch diese so genannte Palmitoylierung erhalten die Membranproteine eine Art Adressaufkleber und werden zur Zellmembran befördert. Die Zelle stemmt sich mit diesem gerichteten Transport vom Golgi-Apparat zur Zellmembran gegen die andauernde "Leckage" in andere Membranen. Denn zusätzlich zur Zellmembran ist die Zelle angefüllt mit Membranen von Organellen, die jeweils über Vesikel miteinander in Verbindung stehen. Dadurch gelangen palmitoylierte Membranproteine, die ursprünglich nur für die Zellmembran vorgesehen waren, auch an andere Orte. Mit der Zeit wären diese Proteine also wahllos innerhalb der Zelle verteilt.
Die Dortmunder Forscher konnten mittels modernster Mikroskopieverfahren maßgeschneiderte molekulare Sonden in lebenden Zellen verfolgen und so den Aufenthaltsort und Transport palmitoylierter Proteine in Echtzeit analysieren. Dabei haben sie herausgefunden, dass die Palmitoylierung vor allem am Golgi-Apparat stattfindet. Von dort erreichen palmitoylierte Proteine an der Oberfläche der abgeschnürten Bläschen die Zellmembran. Damit sich die Proteine nicht in anderen Membranen anreichern, entfernen spezielle Enzyme den Fettsäureanker wahllos von allen palmitoylierten Proteinen. Die Proteine schwimmen dann so lange frei durch die Zelle, bis sie wieder in den Transportmechanismus des Golgi-Apparats eingeschleust werden. So stellt die Zelle sicher, dass fehlgeleitete Proteine kontinuierlich und schnell wieder ins Transportnetz eingespeist und an ihren korrekten Bestimmungsort transportiert werden. "Ein solcher Zustand, der sich nicht im Gleichgewicht befindet und nur unter ständigem Energieaufwand aufrecht erhalten werden kann, zeichnet alles Leben aus - im Gegensatz zu nichtlebenden komplexen Systemen wie Kristallen, die einen Gleichgewichtszustand bei minimaler Energie einnehmen", erklärt Philippe Bastiaens, Leiter der Abteilung Systemische Zellbiologie am Max-Planck-Institut für molekulare Physiologie. Die Forscher haben damit ein grundlegendes Prinzip des Lebens entdeckt.
Einfache Lösung für komplexe Aufgabe
Aber woher weiß die Zelle, welche Proteine im Golgi-Apparat einen Adressaufkleber für die Zellmembran erhalten sollen? Den Wissenschaftlern zufolge kann jedes Protein einen Fettsäureanker bekommen, wenn die Aminosäure Cystein leicht zugänglich an der Oberfläche des Proteins liegt. Es wird dann automatisch zur Zellmembran befördert. Für diese Transportvorgänge sind also keine Rezeptoren nötig, die spezifisch das zu transportierende Protein binden.
Dies ist ein faszinierendes Beispiel dafür, wie komplizierte Vorgänge durch ganz einfache physikalische und chemische Regeln gesteuert werden können. Auf den ersten Blick erscheint es enorm anspruchsvoll, diejenigen Proteine zu identifizieren, die an einen bestimmten Ort transportiert werden müssen sowie Falschtransporte zu erkennen und zu verhindern, dass sie sich vom Zielort weiter verbreiten. Die Zelle schafft dies aber auf ganz einfachem Wege ohne zusätzliche Rezeptoren oder Regulationsmechanismen. Auch andere selbstorganisierende Systeme wie beispielsweise Insektenstaaten funktionieren häufig nach relativ einfachen Prinzipien. Anders könnten sie ihre vielfältigen Aufgaben auch gar nicht bewältigen. "Diese Ergebnisse sind ein Meilenstein. Sie werden die Art verändern, wie künftig in der Zellbiologie geforscht wird. Denn nur wenn wir die Prinzipien kennen, nach denen das Leben funktioniert, werden wir es wirklich verstehen können. Die Fokussierung auf die vielen verschiedenen Signalwege innerhalb der Zelle helfen uns da nicht viel weiter", so Philippe Bastiaens.
Neuer Wirkstoff hemmt Krebs-Protein
Die Forschergruppe ging aber noch einen Schritt weiter und schuf die Grundlage für eine mögliche Anwendung der Erkenntnisse in der Krebstherapie. Ein prominenter Vertreter palmitoylierter Proteine ist das Ras-Protein. Mutationen im ras-Gen finden sich in vielen Tumoren. Es ist allerdings nur dann voll funktionstüchtig, wenn es in der Zellmembran verankert ist und nicht in andere Membranen gelangt. Die Forscher entwickelten daher den Hemmstoff Palmostatin B gegen das Enzym, das für die Abspaltung der Fettsäureanker verantwortlich ist. Wird dieses Enzym ausgeschaltet, bleibt das palmitoylierte Ras in der Zellmembran verankert und gelangt von dort in die Membran anderer Zellorganellen. "Dies war ein völlig neuer Ansatz, der eigentlich dem gesunden Menschenverstand widerspricht. Deswegen hat ihn auch die Pharmaforschung nie weiter verfolgt. Denn wir haben nicht den gerichteten Transport aus dem Golgi-Apparat gehemmt, sondern die wahllose Verteilung in der Zelle gefördert", erklärt Herbert Waldmann, der die Abteilung Chemische Biologie am Dortmunder Max-Planck-Institut leitet.
Mit Palmostatin B konnten die Wissenschaftler das Ras-Protein erstmals hemmen, ohne es gleich vollständig auszuschalten. Ist Ras nämlich völlig inaktiv, sterben auch gesunde Zellen. Die wahllose Verteilung innerhalb der Zelle unterdrückt dagegen nur die unheilvolle Wirkung des mutierten Ras-Proteins. Aus Krebszellen werden so wieder normale Zellen. Dank dieser Entdeckung könnten Ras-abhängige Tumore eines Tages schonend behandelt werden, ohne gesunde Zellen zu schädigen.
Originalveröffentlichungen: Oliver Rocks, Marc Gerauer, Nachiket Vartak, Sebastian Koch, Zhi-Ping Huang, Markos Pechlivanis, Jürgen Kuhlmann, Lucas Brunsveld, Anchal Chandra, Bernhard Ellinger, Herbert Waldmann, and Philippe I.H. Bastiaens; "The Palmitoylation Machinery Is a Spatially Organizing System for Peripheral Membrane Proteins"; Cell 2010.
Frank J. Dekker, Oliver Rocks, Nachiket Vartak, Sascha Menninger, Christian Hedberg, Rengarajan Balamurugan, Stefan Wetzel, Steffen Renner, Marc Gerauer, Beate Schölermann, Marion Rusch, John W. Kramer, Daniel Rauh, Geoffrey J. Coates, Luc Brunsveld, Philippe Bastiaens, Herbert Waldmann; "Small molecule inhibition of acyl protein thioesterase 1 (APT1) affects Ras localization and signaling"; Nature Chemical Biology 2010.
Anzeigen