Ein Hormon nach Pflanzenart
Forscher entwickeln biotechnologisches Herstellungsverfahren
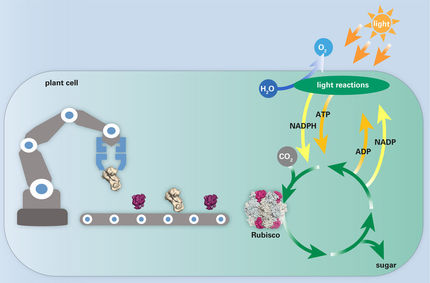
Pflanzen stellen das Hormon Jasmonsäure her, wenn sie angegriffen werden. So sorgen sie dafür, dass ihre Blätter Fraßfeinden nicht mehr schmecken. Biologen wollen erfahren, ob biologische Vorstufen und andere Varianten der Jasmonsäure zu ähnlichen oder abweichenden Effekten führen. Doch für Experimente waren solche Abkömmlinge des Hormons bislang zu teuer und nur schwer zu bekommen. Forscher aus den Fakultäten für Chemie und Biologie der Universität Bielefeld haben jetzt ein Verfahren gefunden, das die Produktion einer biologisch bedeutenden Vorstufe der Jasmonsäure effizienter und günstiger machen könnte. Ihre Innovation: Sie ahmen nach, wie Pflanzen das Hormon herstellen. Das Ergebnis ist 12-OPDA, eine zentrale Vorstufe von Jasmonsäure. Sie könnte langfristig auch als Vorstufe für hochwertiges Parfüm in Frage kommen.

Jasmonsäure bewirkt, dass beschädigte Blätter von Pflanzen für Fraßfeinde unbekömmlich werden. In Bielefeld wurde eine Vorstufe des Hormons erzeugt. Mit ihm lässt sich etwa testen, wie die Fitness von Pflanzen verbessert werden kann.
Universität Bielefeld
„Jasmonsäure kann zum Beispiel die Freisetzung von giftigen Stoffen wie Nikotin in den Blättern anstoßen, die den Angreifern schaden“, erklärt der Biologe Professor Dr. Karl-Josef Dietz. „Tabakpflanzen stoßen eine abgewandelte Form der Jasmonsäure aus und bringen so benachbarte Pflanzen dazu, sich auf Angriffe vorzubereiten“, sagt Dietz. „Jasmonsäure wirkt auch heilend und kann in Gang setzen, dass sich beschädigte Blätter regenerieren.“
Dietz leitet die Arbeitsgruppe Biochemie und Physiologie der Pflanzen der Universität Bielefeld. Er erforscht, wie Pflanzen auf Stress reagieren und arbeitet daran, ihre Reaktion zu verändern und zu optimieren. „Damit können wir Pflanzen zum Beispiel auf die veränderten Umweltbedingungen infolge des Klimawandels vorbereiten.“ Falls das wärmere Klima dazu führt, dass die Käfer-Populationen zunehmen, könnten Pflanzen etwa mit der Fähigkeit ausgestattet werden, diesen An-greifern mit Bitterstoffen zu schaden. „Uns interessiert die Wirkung von Vorformen der Jasmonsäure, wie das 12-OPDA, das nur im Milligramm-Bereich zu bekommen ist und dann mehrere hundert Euro kostet“, sagt Dietz.
„Der hohe Preis kommt durch die arbeitsintensive Herstellung zustande, da auf klassisch-chemischen Wege die Herstellung von 12-OPDA äußerst aufwändig und mit vielen Reaktionsstufen verbunden ist“, sagt der Chemiker Professor Dr. Harald Gröger. Er leitet die Arbeitsgruppe Industrielle Organische Chemie und Biotechnologie an der Universität Bielefeld. Gemeinsam mit Dietz entwickelte er die Idee, 12-OPDA (12-Oxophytodiensäure) als Vorstufe von Jasmonsäure in einem effizienten und synthetisch neuartigen Verfahren herzustellen. Beide Wissenschaftler forschen am Centrum für Biotechnologie (CeBiTec) der Universität Bielefeld.
Das neue Verfahren greift das Prinzip aus den Pflanzenzellen auf: Es nutzt die Enzyme als Katalysatoren der Pflanzen in für synthetische Zwecke optimierter Form. „Wichtig ist, dass diese Enzyme im richtigen Verhältnis eingesetzt werden“, sagt Jana Löwe. Sie ist Erstautorin der neuen Studie und forscht in Grögers Arbeitsgruppe. Der Clou des neuen Verfahrens: Wenn alle Startbedingungen stimmen, läuft es anschließend von selbst.
„Wie die Pflanzen verwenden wir die einfach zugängliche Linolensäure in Kombination mit lediglich drei Enzym-Reaktionen“, erklärt Löwe. Linolensäure kann zum Beispiel aus Rapsöl gewonnen werden. Das erste Enzym baut den Sauerstoff aus der Luft in die Linolensäure ein. Darauf aufbauend erzeugt das zweite Enzym ein hochlabiles Zwischenprodukt, das dann vom dritten Enzym in 12-OPDA umgewandelt wird.
„Das klingt einfach“, sagt Gröger. „Die Schwierigkeit war aber bisher die empfindliche, kurzlebige Zwischenstufe, die durch das zweite Enzym entsteht. Wenn hier nicht sofort das dritte Enzym hinzugefügt wird, entstehen nicht brauchbare Produkte.“
Löwe löst das Problem, indem sie Bakterien als Erzeuger der Enzyme für die zweite und letzte Stufe der Reaktion verwendet – in Verbindung mit einem aus Sojabohnen stammenden kommerziellen Enzym für die erste Reaktionsstufe. Die Bakterien (Escherichia coli) sind genetisch so verändert worden, dass sie die beiden Enzyme in den erforderlichen Mengen bereitstellen. „Sobald die labile Zwischenstufe gebildet wird, ist das benötigte Enzym sofort zur Stelle und sorgt für die Herstellung von 12-OPDA“, sagt Löwe.
Danach kann das 12-OPDA direkt in biologischen Studien eingesetzt oder in weitere Stoffe umgewandelt werden, die zum Beispiel für Dietz‘ Experimente gebraucht werden. Auch dafür hat Löwe ein Verfahren entwickelt. „Damit steht uns eine Bibliothek von Abkömmlingen von 12-OPDA für pflanzenphysiologische Untersuchungen zur Verfügung“, sagt Dietz. „Durch weitere Reaktionen könnte mit dem 12-OPDA darüber hinaus zukünftig in effizienter Weise unter Umständen sogar Methyldihydrojasmonat hergestellt werden“, sagt Gröger. „Das ist eine Substanz, die als Inhaltsstoff für viele bekannte Parfüms benötigt wird.“