Hin zu neuen antiviralen Wirkstoffen und Antibiotika
Schlüsselmechanismus im Prozess der Verformung von Zellmembranen entdeckt
Wissenschaflter der Freien Universität Berlin und des Leibniz-Forschungsinstituts für Molekulare Pharmakologie (FMP) haben einen Schlüsselmechanismus im Prozess der Verformung von Zellmembranen entdeckt.

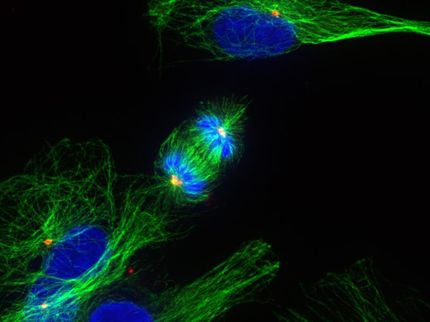
Zellen nehmen Stoffe in ihr Inneres auf, indem sie Einstülpungen produzieren. Die Bildmitte zeigt den Schritt der Verengung der Membraneinstülpung am Rand, der hier hier identifiziert wurde. Clathrinmoleküle, rot dargestellt, können nur eine Einstülpung formen und stabilisieren (links). Um die Einstülpung abzuschneiden, wird die molekulare Schere Dynamin (violett) benötigt. Damit diese Scheren schneiden können, muss der Rand der Einstülpung zunächst verengt werden. SNX9 (grün) wurde nun als das Molekül identifiziert, das diese Einstülpung bewirkt.
Frank Noé und Thomas Splettstößer / scistyle.com.
„Dieser Mechanismus spielt eine fundamentale Rolle in der zellulären Aufnahme von Rezeptoren und Hormonen und wird von Viren und Bakterien gekapert“, erläutert Prof. Dr. Frank Noé, Computerwissenschaftler an der Freien Universität Berlin, der die Studie gemeinsam mit Prof. Dr. Volker Haucke, Biochemiker am FMP, leitete. Der Schlüssel zum Erfolg sei die Kombination aus Hochleistungs-Computersimulationen, hochauflösender Mikroskopie und zellbiologischen Methoden gewesen. Die Arbeit schließe ein wichtiges Kapitel in der Erforschung der Clathrinabhängigen Endozytose (CME) ab und sei von hoher biochemischer und biotechnologischer Relevanz in der Bekämpfung von Diabetes und Krebs sowie für die Entwicklung von antiviralen und antibakteriellen Wirkstoffen.
„Zellen kommunizieren miteinander und mit ihrer Umgebung mithilfe von Rezeptoren auf ihrer Oberfläche“, erklärt Prof. Dr. Frank Noé. Die Veränderung der Anzahl bestimmter Rezeptoren an der Zellmembran beeinflusse die Schwelle, oberhalb derer eine Zelle ein bestimmtes Signal wahrnimmt. Manche Rezeptoren müssten auch ins Zellinnere aufgenommen werden, um die richtige Zellantwort auszulösen. „Die Frage ist, mit welchem Mechanismus solche Rezeptoren von der Zellmembran entfernt und in die Zelle aufgenommen werden können“, sagt Dr. Volker Haucke. Eine Möglichkeit sei, sie in Paketen zu sammeln, die entsprechende Membranstelle einzustülpen und dann in das Zellinnere abzuschnüren. Diesen Prozess nenne man Clathrinabhängige Endozytose (CME).
„Es ist, als würde man einen Ballon aus einem Tuch formen, es entsteht damit ein sogenanntes Vesikel“, erklärt der Pharmakologe. Zunächst müsse eine Einstülpung gebildet werden, dann am Rand verengt und zuletzt abgeschnitten werden. Es sei im Detail bekannt, welche Moleküle die Membranausstülpung bilden und die Abschnürung bewirken; den Wissenschaftlern der Freien Universität Berlin und des Leibniz-Forschungsinstituts für Molekulare Pharmakologie ist es nun gelungen festzustellen, welches Molekül die Membraneinstülpung verengt, bevor sie abgeschnitten werden kann: Es ist SNX9.
In ihrer Untersuchung machten die Wissenschaftler zunächst das Molekül-Signal aus, das die Membranverengung initiiert. „Es stellte sich heraus, dass sich im Prozess der Membraneinstülpung nicht nur die Form der Membran verändert, sondern auch deren Zusammensetzung“, erklärt Dr. Johannes Schöneberg, einer der Erstautoren der Studie. Während die Membraneinstülpung wachse, reicherten sich immer mehr Moleküle eines bestimmten Lipids darin an.
„Man kann sich das wie in einem molekularen Konzert vorstellen, in dem das erste Lied gespielt wird – es entsteht ein ziemliches Gedränge“, sagt Dr. Martin Lehmann, ein weiterer Erstautor. Die Wissenschaftler tetsteten verschiedene „Kandidaten“und stellten fest, dass SNX9 das Schlüsselmolekül ist, das am stärksten auf die Verändung der Membranzusammensetzung reagiert. Sobald SNX9 identifiziert war, konnte das Molekül mit Fluoreszenzfarbstoffen sichtbar gemacht werden, und die Wissenschaftler konnten seine Wege verfolgen, während die Zelle eine Einstülpung produziert. SNX9 erreicht die Membran genau im richtigen Moment und verengt die Einstülpung, bevor sie abgeschnitten wird, sodass schließlich ein Vesikel entsteht.