Neutronen klären Enzymfunktion
Neuer Ansatzpunkt für Medikamente gegen Magen-Bakterium Helicobacter pylori
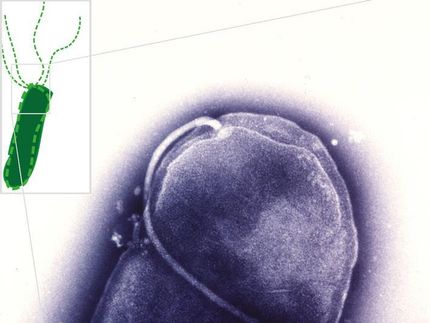
Helicobacter pylori steht unter dringendem Verdacht Magenkrebs auszulösen. Jetzt hat ein internationales Forscherteam um Prof. Donald R. Ronning (University of Toledo, USA) mit Hilfe von Neutronen die Funktionsweise eines wichtigen Enzyms im Stoffwechsel des Bakteriums entschlüsselt. Es gilt als Angriffspunkt für neue Medikamente. Die Messungen hierzu führten sie an der Neutronenquelle in Oak Ridge (USA) und der Forschungs-Neutronenquelle FRM II der Technischen Universität München (TUM) durch.

Montage eines MTAN-Kristalls im Zentrum des Neutronenstrahls im BIODIFF-Instrument
Andreas Ostermann / TUM

Beugungsbild des Proteinkristalls, wie es bei der Neutronenstreuung am Instrument BIODIFF entsteht
Andreas Ostermann / TUM


Weltweit jeder Zweite trägt es in seinem Magen: Helicobacter pylori. Geschwüre und chronische Gastritis sind die häufigsten Krankheitsbilder, die mit diesem Bakterium in Verbindung gebracht werden. Bislang geht die Medizin gegen den Magenkeim mit einer Kombination aus zwei Antibiotika und einem Protonenpumpen-Hemmer vor. Doch nur in 70 Prozent der Fälle wirkt die Behandlung, und es entstehen zunehmend Resistenzen. Schon seit langem sind Wissenschaftler daher auf der Suche nach alternativen Medikamenten gegen das gefährliche Bakterium.
Anders als der Mensch und viele nützliche Bakterien, verwendet H. pylori ein spezielles Enzym für die Synthese von Vitamin K2. Dieses Enzym, die 5‘-Methylthioadenosin Nucleosidase (MTAN), ist daher ein vielversprechender Kandidat zur Entwicklung eines Medikaments, das spezifisch nur gegen H. pylori wirkt, ohne dabei nützliche Bakterien oder gar menschliche Zellen zu schädigen.
Strukturaufklärung mit Neutronen
Das Enzym MTAN ist an einem wichtigen Syntheseschritt für das Vitamin K2 beteiligt. Über Wasserstoffbrückenbindungen wird dabei eine Vorstufe des Vitamins gebunden, um eine Seitengruppe abzutrennen. Die hierfür wichtigen Positionen und Positionswechsel der Wasserstoffatome waren bislang nicht zweifelsfrei bekannt.
Die übliche Methode zur Strukturaufklärung von Enzymen, die Kristallstrukturanalyse mit Röntgenstrahlen, hilft hier nur wenig, da Röntgenstrahlung für Wasserstoff-Atome nahezu blind ist. Die Forscher nutzten daher Neutronen zur Strukturaufklärung. Sie sind für Wasserstoff-Atome besonders empfindlich.
Am Diffraktometer BioDiff, das von der TUM und dem Forschungszentrum Jülich (Jülich Centre for Neutron Science, JCNS) gemeinsam am Heinz Maier-Leibnitz Zentrum in Garching betrieben wird, sowie an der Neutronenquelle des Oak Ridge National Laboratory (USA) untersuchten die Wissenschaftler verschiedene Zustände des Enzyms und konnten so ein genaues Bild seiner Wirkweise ermitteln.
„Da wir nun den genauen Ablauf der Reaktion und die beteiligten Bindungsstellen des Enzyms kennen, ist es nun möglich Moleküle zu entwickeln, die genau diesen Ablauf blockieren“, sagt TUM-Biologe Dr. Andreas Ostermann, der zusammen mit Dr. Tobias Schrader (JCNS) das Instrument am FRM II betreut.
An der Publikation beteiligt waren Forscher der University of Toledo (Toledo, USA), der Victoria University of Wellington (Neuseeland), der Forschungs-Neutronenquelle Heinz-Maier-Leibnitz der TU München, des Ju?lich Centre for Neutron Science und des Oak Ridge National Laboratory (USA). Die Arbeit wurde gefördert mit Mitteln des Center for the Advancement of Science in Space (USA) und des National Institute of Allergy and Infectious Disease (USA). Röntgenstrukturdaten wurden an der Advanced Photon Source des Argonne National Laboratory (USA) gemessen mit Unterstützung der Michigan Economic Development Corporation.