Kräftemessen im Erbgutmolekül
Forscher messen erstmals direkt die Stapelkraft in DNA-Doppelhelix
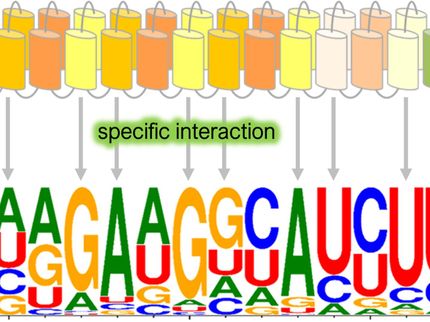
Unser Erbgut, die DNA, hat vereinfacht dargestellt die Struktur einer verdrehten Strickleiter – in der Fachwelt wird diese Struktur als Doppelhelix bezeichnet. Für ihre Stabilität sind unter anderem die sogenannten Basenpaar-Stapelwechselwirkungen verantwortlich. Wissenschaftlern der Technischen Universität München (TUM) ist es zum ersten Mal gelungen, diese Kraft direkt zu messen. Das neue Wissen könnte dabei helfen, präzise molekulare Maschinen aus DNA zu konstruieren.
Illustration der Basenpaar-Stapelwechselwirkungen.
Christoph Hohmann & Hendrik Dietz/ Nano Initiative Munich/ TUM
Vor mehr als 60 Jahren klärten die Forscher Crick und Watson die Struktur der Desoxyribonukleinsäure, vor allem bekannt unter der englischen Abkürzung DNA, auf. Sie verglichen die Doppelhelix mit einer spiralförmig gedrehten Strickleiter. Die Sprossen dieser Leiter bilden dabei die Basenpaare Guanin und Cytosin sowie Thymin und Adenin. Doch was hält die DNA-Stränge in der Spiralform?
Messsystem für Wechselwirkungen zwischen molekularen Oberflächen
Prof. Hendrik Dietz vom Lehrstuhl Experimentelle Biophysik nutzt DNA als Baumaterial, um molekulare Strukturen zu konstruieren. Daher hat er auch ein großes Interesse daran, dieses Material genau zu verstehen. "Es gibt im Grunde zwei Typen von Wechselwirkungen, die Doppelhelices stabilisieren", erklärt er. Zum einen sind in der DNA die sogenannten Wasserstoffbrückenbindungen vorhanden.
Zum anderen gibt es die sogenannten Basenpaar-Stapelwechselwirkungen, die zwischen den aufeinandergestapelten Basenpaaren entlang der Spiralachse wirken. Die Kräfte der Wasserstoffbrückenbindungen wirken dagegen senkrecht zur Achse. "Bisher ist eigentlich nicht klar, mit welchen Anteil diese beiden Kräfte jeweils zur gesamten Stabilität der DNA-Doppelhelix beitragen", erklärt Dietz.
Die sehr schwache Stapelkraft zwischen einzelnen Basenpaaren direkt zu messen, war eine große technische Herausforderung für die Forscher, an der sie sechs Jahre lang arbeiteten. Gemeinsam mit dem TUM-Lehrstuhl für Molekulare Biophysik (Prof. Matthias Rief) und dem TUM-Lehrstuhl für Theoretische Biophysik - Molekulardynamik (Prof. Martin Zacharias) gelang es ihnen, ein spezielles Messsystem zu entwickeln, das es zum ersten Mal möglich macht, ultraschwache Kontakt-Wechselwirkungen zwischen einzelnen Molekülen zu messen.
Der billionste Teil einer Tafel Schokolade
Vereinfacht dargestellt handelt es sich bei dem hierarchisch aufgebauten Messsystem um mikroskopische Balken, an deren Spitze sich eine oder mehrere parallel verlaufende Doppelhelix-Strukturen befinden. Diese sind so modifiziert, dass sie am Ende jeweils ein Basenpaar tragen. Zwei dieser mikroskopischen Balkeneinheiten sind durch ein Polymer miteinander verbunden.
Auf der anderen Seite sind die Balken an mikroskopische Kügelchen gekoppelt, die wiederum mit einer optischen Laserpinzette auseinandergezogen werden können. In Lösung können nun die Basenpaare am Ende der einen Balkeneinheit mit den Basenpaaren am Ende der anderen Balkeneinheit interagieren. Und es lässt sich messen, wie lange eine Stapelbindung zwischen ihnen anhält, bevor sie sich durch eine Fluktuation wieder trennen, und natürlich auch die Kraft, die zwischen den Basenpaaren wirkt.
Die von den Forschern gemessenen Kräfte liegen im Bereich Piconewton. "Ein Newton ist die Gewichtskraft einer Tafel Schokolade", erklärt Dietz. "Wir reden von einem 1000-Millardstel Anteil davon, das ist wirklich wenig." Kräfte im Bereich von zwei Piconewton reichen aus, um die durch Stapelwechselwirkungen erzeugte Bindung zu trennen. Die Wissenschaftler konnten außerdem beobachten, dass die Bindungen innerhalb weniger Millisekunden spontan zerfallen und sich wieder bilden. Wie stark die Bindungen sind und wie lange sie halten, hängt dabei stark davon ab, welche Basenpaare aufeinander gestapelt sind.
Hin zu DNA Maschinen
Die Ergebnisse aus den Messungen helfen dabei, mechanische Aspekte von grundlegenden biologischen Prozessen wie etwa die DNA-Replikation, also die Vervielfältigung des Erbguts, besser zu verstehen. Die geringe Lebensdauer der Stapelwechselwirkung könnte beispielsweise bedeuten, dass ein Enzym, das die Aufgabe hat, bei diesem Prozess die Basenpaare zu trennen, eigentlich nur darauf warten muss, dass die Stapelbindungen von alleine aufgehen – anstatt Kraft aufzuwenden, um sie zu trennen.
Dietz will die Daten aber auch direkt auf seine aktuellen Forschung anwenden: Er nutzt DNA als programmierbares Konstruktionsmaterial, um Maschinen auf Nanoebene zu bauen. Dabei orientiert er sich als Inspiration an den komplexen Strukturen, die etwa in den Zellen zu finden sind und unter anderem als molekulare Fabriken wichtige Verbindungen wie den Energiespeicher ATP synthetisieren. "Wir wissen also, was alles möglich wäre, wenn wir in der Lage wären, ausreichend komplizierte Strukturen zu bauen", sagt Dietz. "Und wenn wir ein besseres Verständnis der molekularen Wechselwirkungen haben, können wir natürlich besser mit den Molekülen bauen."
Momentan konstruiert die Arbeitsgruppe einen molekularen Rotations-Motor aus DNA, dessen Komponenten über Stapelbindungen ineinandergreifen und zusammenhalten. Ziel ist es, eine gerichtete Rotation durch chemische oder thermische Impulse steuern zu können.